Indice
Introduzione……… pag. 1
L’ablazione transcatetere della fibrillazione atriale………… pag. 24
Rimodellamento strutturale dell’atrio………... pag. 37
Il nostro studio
o Ipotesi……… pag. 47
o Il rapporto LA/RAo………... pag. 50
o Selezione dei pazienti……… pag. 51
o Metodi……… pag. 56
o Risultati……….. pag. 61
o Discussione……… pag. 69
o Conclusioni……… pag. 74
La fibrillazione atriale
La fibrillazione atriale è l’aritmia più comune e clinicamente rilevante
nei paesi occidentali. All’inizio del XXI secolo essa rappresenta uno
degli argomenti più caldi della cardiologia. La fibrillazione atriale si
configura, oggi, come una vera e propria epidemia. Si stima che più di
due milioni di americani e tre milioni di europei ne siano affetti ed il
trend è in continuo aumento. La vera e propria esplosione della letteratura scientifica sull’argomento che abbiamo osservato nel corso
degli ultimi anni è testimone di tutto questo. Basti pensare che negli
ultimi dieci anni sono stati pubblicati più studi sulla fibrillazione atriale
che nel resto della storia della medicina. Nel deliniare in maniera chiara
Introduzione
2
presentare appare necessaria una trattazione delle basi patologiche ed
epidemiologiche della malattia che prenda in considerazione le opzioni oggi disponibili per il trattamento dell’aritmia, il successo ed il profilo di
rischio di tali metodiche. Scopo della nostra trattazione e della nostra
ricerca è individuare un parametro clinico, semplice da ottenere,
disponibile ovunque ed a basso costo, che sia in grado di fornire
indicazioni sulle possibilità di successo del trattamento ablativo per la
fibrillazione atriale.
Basi epidemiologiche
La fibrillazione atriale si configura, come accennato sopra, come una
vera e propria epidemia. Questo principalmente per due ragioni. In primo
luogo per il fatto che la prevalenza dell’ aritmia aumenta con l’età e, dato l’invecchiamento della popolazione che osserviamo su scala planetaria,
l’incremento del numero dei pazienti affetti da fibrillazione atriale è
inevitabile. L’altra principale ragione dell’aumento di prevalenza atteso
nei prossimi anni è risiede nell’ aumento di sopravvivenza dei soggetti
affetti da malattie cardiovascolari, in special modo ipertensione arteriosa
3
responsabili dello sviluppo di fibrillazione atriale. Numerosi studi
epidemiologici, da quaranta anni a questa parte, sono stati condotti per stabilire l’esatta incidenza della malattia, la sua prevalenza nelle diverse
fasce di età della popolazione e non ultime la morbilità e la mortalità che
essa comporta. Un altro dato rilevante analizzato sempre più spesso
riguarda i costi sociali della malattia che, considerati i numeri con cui abbiamo a che fare, sono tutt’altro che trascurabili. Secondo un recente e
autorevole studio condotto negli Stati Uniti la prevalenza generale della fibrillazione atriale nell’intera popolazione è dello 0.95%. La prevalenza
aumenta con l’età passando dallo 0,1% nei soggetti di età inferiore a 55
anni al 9% nei pazienti di età > 80 anni. Essa risulta essere del 3,8% nei pazienti di età superiore a 65 anni. La prevalenza dell’aritmia è risultata
essere superiore nei maschi rispetto alle femmine in tutti i gruppi di età
Introduzione
4
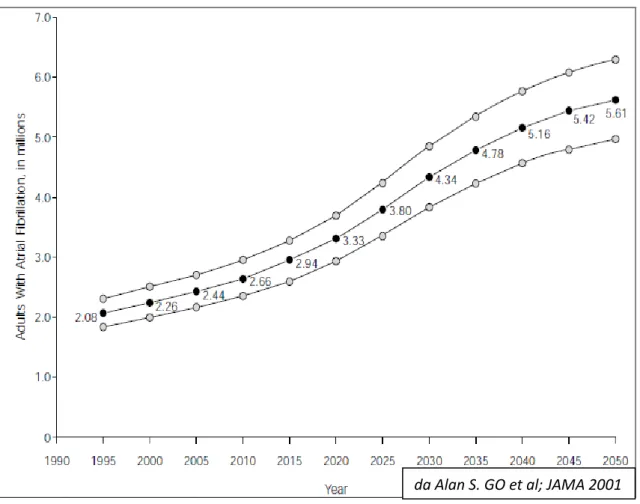
Figura 1. Prevalenza della FA stratificata per età e sesso
Dallo studio risulta che circa 2.3 milioni di americani sono affetti da
fibrillazione atriale. Incrociando i dati di prevalenza con quelli relativi
alla crescita attesa della popolazione ed al suo invecchiamento si stima
che per il 2050 tali numeri sono destinati ad aumentare di 2.5 volte
arrivando a 5.6 milioni di americani affetti. Negli altri studi di
prevalenza condotti negli USA ed in Europa troviamo numeri simili. Per l’Europa la stima del numero di pazienti affetto nel 2050 ammonta a 7
milioni.
5
Figura 2. Proiezione del numero di pazienti affetti da FA al 2050
L’incidenza della fibrillazione atriale è stimata essere di circa 2,4 nuovi
casi ogni mille persone per anno. Secondo lo studio di Framingham l’incidenza cresce con l’età con valori di 3,1 negli uomini e 1,9 nelle
donne di età compresa tra 55 e 64 anni arrivando fino a 38 e 31,4 nuovi
casi per mille persone per anno nei soggetti di età superiore agli 85 anni.
Numerosi altri studi epidemiologici condotti confermano questi dati.
Sempre dai dati del Framingham Heart Study viene fuori che il rischio di
sviluppare fibrillazione atriale dai 40 ai 95 anni è pari a 26% per gli
Introduzione
6
uomini e 23% per le donne. Altri aspetti epidemiologici fondamentali da considerare sono la morbilità e la mortalità associate all’aritmia. Da tutti
gli studi su larga scale effettuati sull’argomento si evince chiaramente
che le conseguenze della fibrillazione atriale sono tutt’altro che
trascurabili. La mortalità per tutte le cause, nei pazienti affetti da
fibrillazione atriale, è aumentata di 1,3-1,8 volte per gli uomini e 1,9-2,8 volte per le donne. Uno studio clinico condotto sull’argomento ha
mostrato un rischio di morte superiore di 2,4 volte anche aggiustando i
dati per età, sesso e altri fattori di rischio cardiovascolare. La
complicanza legata alla fibrillazione atriale che pesa di più da un punto
di vista epidemiologico è lo stroke tromboembolico. Nello studio di
Framingham il rischio di sviluppare un ictus ischemico nei paziente con
fibrillazione atriale ammonta a 1,5% nei pazienti di età compresa tra i 50
ei 59 anni fino ad arrivare al 23% nei pazienti con età superiore ad 80
anni. Oltre a ciò bisogna sottolineare che gli stroke associati a
fibrillazione atriale sono mediamente più gravi ed associati ad un più elevato grado di disabilità. I pazienti afferri dall’aritmia, inoltre, tendono
ad avere stroke recidivanti e più frequentemente fatali anche aggiustando
i dati per gli altri fattori di rischio di stroke. Un’altra conseguenza della
7
sviluppare insufficienza cardiaca. Nello studio Manitoba la presenza di
fibrillazione atriale è stata associata ad un aumento del rischio di
sviluppare insufficienza cardiaca di 3 volte. Naturalmente le terapie
disponibili attualmente per il controllo del ritmo e della frequenza e l’uso
estensivo della terapia anticoagulante hanno ridotto notevolmente tali
conseguenze. C’è da dire comunque che la fibrillazione atriale è
responsabile di un numero ragguardevole di stroke che ammonta, negli
USA, al 15-25% del totale. Nei pazienti di età superiore a 75 anni la
fibrillazione atriale è la prima causa di stroke.
Data la morbilità ad essa associata la fibrillazione atriale ha un notevole
impatto sui costi di assistenza sanitaria. Essa rappresenta un grosso
problema di costi data la prevalenza in costante aumento e quindi il
crescente bisogno di cura. Da studi europei ed americani risulta che il
costo medio per anno di un paziente affetto da fibrillazione atriale è di
circa 3000 Euro. Il numero di ospedalizzazioni per fibrillazione atriale è
triplicato rispetto a venti anni fa. Il trattamento della fibrillazione atriale
negli USA ha un costo annuale di circa 6,65 miliardi di dollari. Ai costi
di ospedalizzazione vanno aggiunti i costi di gestione domiciliare del
paziente e quindi di farmaci, presidi e monitoraggio della terapia
Introduzione
8
Fattori di rischio
La fibrillazione atriale mostra numerosi fattori di rischio. In linea generale qualsiasi condizione emodinamica provochi l’aumento delle
pressioni atriali sinistre, l’aumento di dimensioni dell’atrio sinistro, un
danno al miocardio atriale o una modifica delle proprietà
elettrofisiologiche dei miocardiociti atriali può causare fibrillazione
atriale. Possiamo dividere fattori di rischio in due principali categorie:
fattori di rischio cardiovascolari e non cardiovascolari.
Tra i fattori di rischio cardiovascolari il più importante è sicuramente l’ipertensione arteriosa. Il danno al cuore causato dall’ipertensione con
conseguente riduzione della compliance del ventricolo sinistro ed
aumento delle pressioni atriali sinistre è responsabile della maggior parte
dei casi di fibrillazione atriale legati ad ipertensione arteriosa. Un altro
fattore di rischio cardiovascolare importante nella pratica clinica è la cardiopatia ischemica. L’ischemia atriale e le modificazioni
emodinamiche indotte dalla cardiopatia ischemica sono un forte fattore di rischio per lo sviluppo di fibrillazione atriale. L’altro importante
9
L’aumento delle pressioni atriali sinistre e destre a causa dell’aumento
della pressione polmonare portano in una percentuale elevata i pazienti
affetti da scompenso cardiaco a sviluppare fibrillazione atriale. Possiamo
includere nei fattori di rishio cardiovascolare le valvulopatie mitraliche e
soprattutto la stenosi che, causando nel tempo un notevole aumento di
dimensioni atriali sinistre, porta quasi invariabilmente a fibrillazione
atriale. Anche se più rara la cardiomiopatia ipertrofica è un potente fattore di rischio per l’aritmia data la compromissione della funzione
diastolica del ventricolo sinistro ad essa attribuibile ed il sovvertimento dell’architettura cellulare miocardica con la presenza di fibrosi, potente
coadiuvante nel mantenimento della fibrillazione atriale. Altri fattori di
rischio cardiovascolari sono la disfunzione del nodo del seno, la pericardite, l’elettrostimolazione ventricolare destra, le cardiopatie
congenite ed altre cardiomiopatie.
Tra i fattori di rischio non cardiovascolari il più importante è sicuramente l’età e, connessa ad essa, l’aspettativa di vita alla nascita.
L’invecchiamento porta a fibrillazione atriale attraverso svariati
meccanismi. Sicuramente il rimodellamento strutturale ed elettrico dell’atrio giocano un ruolo fondamentale. Con l’età sopraggiungono
Introduzione
10
comparsa di fibrosi e la perdita di cellule specializzate, la diminuzione
delle cellule del nodo del seno, la fibrosi a livello del nodo AV. A livello
del miocardio compaiono diffuse aree a basso voltaggio con
rallentamento della conduzione regionale. Un altro fattore di rischio non
cardiovascolare importante soprattutto nei paesi mediterranei sono le
patologie tiroidee. Gli ormoni tiroidei predispongono alla fibrillazione
atriale mediante la modificazione delle proprietà elettrofisiologiche della
cellula cardiaca. Altri fattori di rischio non cardiovascolari che assumono
importanza nella pratica clinica sono il diabete, l’obesità e le malattie
polmonari. Anche la stimolazione adrenergica e vagale possono portare a
fibrillazione atriale mediante le modificazioni indotte sul periodo
refrattario cellulare atriale. I disturbi elettrolitici possono agire da cause scatenanti. Nei paesi occidentali anche l’abuso di alcool, soprattutto tra i
giovani, può essere una causa scatenante di fibrillazione atriale.
Meccanismi fisiopatologici
La storia della ricerca sui meccanismi fisiopatologici della fibrillazione
atriale possiamo considerarla relativamente recente. Se possiamo far risalire la descrizione della fibrillazione atriale come “irregolarità” del
11
polso a circa mille anni fa è solo con la invenzione dell’elettrocardiogramma da parte di Einthoven che la ricerca sul ritmo
atriale ha avuto in impulso decisivo. Nel corso del secolo scorso si sono
succedute numerose teorie che individuavano il meccanismo
patogenetico fondamentale della fibrillazione atriale in fenomeni di
rientro o di aumentato automatismo. Negli anni venti gli studi di Lewis
individuarono come meccanismo fondamentale il rientro. Queste teorie
furono abbandonate negli anni cinquanta grazie agli studi di Sherf e
Prinzmetal. Questi studi dimostrarono che la fibrillazione atriale può
essere indotta mediante la stimolazione con aconitina o acetilcoline del
miocardio atriale ed interrotta mediante il successivo raffreddamento di
queste aree. Sherf concluse che la fibrillazione atriale poteva essere
dovuta a un focus ectopico e che si sosteneva mediante una propagazione peculiare delle onde di attivazione che egli chiamò “conduzione
fibrillatoria”. Questa teorie fu abbandonata a favore della ipotesi del
rientro e delle onde di attivazione multiple, ipotesi venute alla ribalta grazie agli studi di Moe e di Alessie. Quest’ultimo ha potuto
documentare in modelli animali la modalità di attivazione degli atri
durante la fibrillazione atriale. Dai suoi studi è emerso che l’aritmia è
Introduzione
12
e direzione. Questi circuiti non avrebbero una base anatomica ma
funzionale legata alla refrattarietà di aree contigue di miocardio. La
formazione di tali circuiti sarebbe favorita dal rallentamento della
conduzione in aree specifiche di miocardio e dalla brevità della
refrattarietà cellulare. Secondo altri autori in accordo con questa teoria
esisterebbero aree preferenziali di formazione di questi circuiti soprattutto in corrispondenza della parete posteriore dell’atriosinistro ed
intorno allo sbocco delle vene polmonari. In queste sedi si formerebbero i cosiddetti “rotors” responsabili del perpetuarsi dell’aritmia. Un altro
concetto fondamentale per la pratica clinica che emerge dagli studi sperimentali sull’aritmia è il concetto che la fibrillazione atriale favorisce
la fibrillazione: la cosiddetta teoria “atrial fibrillation begets atrial
fibrillazion”. Secondo tale teoria la persistenza dell’atrio in fibrillazione
atriale favorisce la comparsa di cambiamento patologici a livello del
miocardio. Uno dei principali è quello che riguarda i meccanismi intracellulari di scambio del calcio. L’elevata frequenza atriale presente
durante la fibrillazione atriale provoca un accumulo intracellulare di
calcio che porterebbe alla morte cellulare. Numerose modificazioni del
metabolismo cellulare, alcune istantanee ed alcune dopo giorni, vengono
13
gran parte di questi meccanismi porta ad una riduzione del periodo
refrattario cellulare e come conseguenza favoriscono il mantenimento
della fibrillazione atriale. Alla fine degli anni novanta del secolo scorso
una svolta decisiva alla comprensione dei meccanismi patogenetici della
fibrillazione atriale insieme con una svolta terapeutica è stata data dagli
studi di Haisseguerre e del gruppo di Bordeaux. Da tali studi è emerso
chiaramente il ruolo innescante delle vene polmonari nella genesi della
fibrillazione atriale. Queste strutture, infatti, possono contenere foci
automatici capaci scariche rapide. Tali scariche de sincronizzano l’attività elettrica degli atri portandoli a fibrillare. In questo contesto le
alterazioni strutturali e funzionali della muscolatura atriale giocano un
ruolo fondamentale nel mantenimento della fibrillazione atriale. Tali teorie hanno dato un grosso impulso all’aritmologia nel corso delle
ultime due decadi ed hanno costituito la base dello sviluppo delle
tecniche interventistiche di trattamento della fibrillazione atriale. Da un
punto di vista clinico dobbiamo considerare la fibrillazione atriale non
come il risultato di un unico meccanismo patogenetico, ma come il
risultato finale di diversi meccanismi fisiopatologici la cui importanza
varia da paziente a paziente. In accordo con le teorie di Alessie
Introduzione
14
initiator e i perpetuator. I trigger sono variabili e possono essere rappresentati da foci ectopici all’interno delle vene polmonari o da altre
tachicardie. Perché i trigger possano innescare la fibrillazione atriale
hanno bisogno di un substrato elettrofisiologico in grado di favorire il
rientro: gli initiator. Spesso essi sono costituiti da aree di refrattarietà
breve o bassa velocità di conduzione. Infine perché la fibrillazione atriale possa sostenersi c’è bisogno dei perpetuator. Questi sono costituiti dalla
dilatazione degli atri e dalla modificazioni strutturali ed
elettrofisiologiche del substrato anatomico. Nei diversi pazienti il peso di
ognuno degli elementi patogenetici è diverso. Infatti nella fibrillazione
atriale parossistica ha un peso maggiore il trigger, mentre nella
permanente assume una importanza fondamentale il perpetuator.
Trattamento
Fino a poche decadi fa il trattamento della fibrillazione atriale e
soprattutto quello volto al controllo del ritmo non veniva nemmeno preso
in considerazione. Veniva raccomandata la CVE o farmacologica con
chinidina o più spesso il controllo della frequenza cardiaca mediante la digitale o più raramente mediante l’uso di antagonisti del sistema
15
adrenergico. La terapia anticoagulante veniva consigliata soltanto nel
breve periodo che precedeva la cardioversione. La prima cardioversione
elettrica fu effettuata nel 1962. Da allora le strategie terapeutiche per la
fibrillazione atriale hanno subito una notevole evoluzione. Non solo le
strategie per il controllo della frequenza, ma soprattutto quelle rivolte al controllo del ritmo sono cambiate notevolmente con l’avvento di nuovi
farmaci antiaritmici e soprattutto dell’ablazione transcatetere. Si è
discusso molto sul significato prognostico del mantenimento del ritmo
sinusale. Sono state espresse numerose e discordanti opinioni a riguardo
e molti studi randomizzati sono stati condotti per arrivare ad una
conclusione scientificamente accettabile. Il più importante di questi studi
è stato lo studio AFFIRM. Questo studio ha mostrato che, se la terapia viene applicata correttamente, non c’è una differenza significativa dal
punto di vista prognostico tra controllo del ritmo e controllo della
frequenza. Il controllo dl ritmo sarebbe da preferire soltanto nei pazienti
in cui non si riesce ad ottenere un buon controllo dei sintomi mediante il
controllo della frequenza cardiaca. Questo studio però è stato condotto in
pazienti mediamente molto anziani e ad elevato rischio di stroke e per
tale motivo i risultati non possono essere applicati a tutti i pazienti affetti
Introduzione
16
attuale è quella di ottenere il controllo del ritmo quando possibile e
soprattutto un buon controllo dei sintomi. Per quello che riguarda il
rischio tromboembolico le linee guida internazionali sono molto chiare
suggerendo di effettuare la scelta tra terapia antiaggregante ed
anticoagulante in base al punteggio di rischio tromboembolico del
singolo paziente ottenuto mediante uno score calculator semplice da
applicare. Una svolta nella gestione del rischio tromboembolico è
arrivata nel corso degli ultimi due anni. Essa deriva dalla possibilità di occludere l’auricola sinistra mediante un dispositivo impiantabile per via
percutanea. L’efficacia della procedura, relativamente semplice e scevra
da rischi, è stata validata mediante uno studio randomizzato che ha
messo a confronto tale strategia con la terapia anticoagulante orale
tradizionale ottenendo risultati in termini di prevenzione degli eventi
tromboembolici del tutto sovrapponibili. La procedura, però, è possibile
solo in un gruppo selezionato di pazienti con fibrillazione atriale che non
abbiano malattie valvolari.
Strategie di trattamento rivolte al controllo della frequenza cardiaca.
Attualmente le strategie rivolte al controllo della frequenza cardiaca
17
controllo del ritmo è fallito o non è possibile. Per il controllo della
frequenza abbiamo a disposizione sia terapie farmacologiche che non
farmacologiche. Lo scopo della terapia farmacologica è quella di
rallentare la conduzione dell’impulso a livello del nodo atrio-ventricolare e quindi di abbassare la risposta ventricolare durante l’aritmia. Per
ottenere ciò vengono in genere usate diverse classi di farmaci, tutte con
un effetto intrinseco dromotropo negativo. I farmaci maggiormente usati
sono i beta bloccanti ed i calcio antagonisti ad azione cardiaca. Un altro
farmaco molto usato in passato per ottenere il controllo della frequenza
ventricolare durante fibrillazione atriale è la digitale, oggi meno usata a
causa degli effetti avversi. Quando non è possibile ottenere il controllo
della frequenza cardiaca mediante i farmaci può essere attuata una strategia cosiddetta “ablate and pace”. Essa consiste nell’impianto di un
pacemaker definitivo per la stimolazione ventricolare e della successiva
ablazione, in genere mediante radiofrequenza, della porzione compatta
del nodo atrio-ventricolare. Tale strategia consente un perfetto controllo della frequenza cardiaca anche se è gravata dai rischi legati all’impianto
del dispositivo ed alla conseguente ablazione. Le strategie appena descritte funzionano bene nell’alleviare i sintomi legati alla fibrillazione
Introduzione
18
ventricolare, che l’elevata frequenza può comportare nel tempo. Appare
ovvio rimarcare il fatto che tale strategia non risolve in alcun modo né le
conseguenze emodinamiche della fibrillazione atriale (perdita del
contributo atriale), né il rischio tromboembolico legato all’aritmia
configurandosi come una opzione terapeutica rivolta ai soggetti più
anziani ed a quelli che comunque hanno indicazione ad assumere terapia
anticoagulante per altre ragioni.
Strategie di trattamento rivolte al controllo del ritmo cardiaco
Le terapie rivolte al controllo del ritmo cardiaco sono un argomento di estrema attualità nell’odierna cardiologia e, nel corso degli ultimi dieci
anni, sono diventate argomento di accese discussioni tra esperti oltre che
di un fiorire di letteratura scientifica. Indicazioni e linee guida
internazionali sono state più volte modificate a seconda dei risultati dell’ingente numero di trials sull’argomento. Sul versante della terapia
farmacologica ed ancora di più su quello della terapia non farmacologica
si sono avute innovazioni che hanno cambiato radicalmente il modo di approcciare i pazienti con fibrillazione atriale. L’obiettivo attuale è
quello di fornire al singolo paziente l’opzione di trattamento più efficace
19
rischi. Cominciamo col dire che esistono due approcci terapeutici, quello
farmacologico e quello non farmacologico. Nella pratica clinica, in
realtà, non esiste questa netta distinzione e per lo stesso paziente in
genere si usano entrambi gli approcci terapeutici, spesso anche
contemporaneamente. Diciamo quindi che il trattamento della fibrillazione atriale si avvale di una strategia “integrata” rivolta al
controllo del ritmo avvalendosi di farmaci e di procedure interventistiche complesse quale l’ablazione.
La terapia farmacologica
I farmaci usati per il controllo del ritmo appartengono essenzialmente
alla classe I ed alla classe III. Della classe I fanno parte i farmaci che
agiscono sui canale del sodio. I farmaci di questa classe utilizzati nella
pratica clinica sono quelli della sottoclasse Ic (flecainide e propafenone).
Essi sono potenti inibitori della corrente rapida del sodio e quindi agiscono sulla fase iniziale del potenziale d’azione rallentando l’onset
della depolarizzazione. Essi, inoltre, prolungano la durata del potenziale d’azione agendo sulla corrente lenta del sodio. Tali farmaci si sono
rivelati relativamente efficaci nel controllo degli episodi di fibrillazione
Introduzione
20
soggetti con cuore sano dati gli effetti proaritmici ed inotropi negativi ad
essi correlati. Effetti pro aritmici per la flecacainide sono stati dimostrati
nello studio CAST e per il propafenone nello studio CASH. Essi includono l’induzione e l’esacerbazione di tachicardie ventricolari oltre a
casi di morte improvvisa. Questi farmaci, inoltre, in presenza di blocchi
atrio-ventricolari preesistenti possono peggiorarne il grado fino ad
indurre blocchi avanzati soprattutto in associazione con altri farmaci
come i beta-bloccanti ed i calcio-antagonisti. Gli altri farmaci molto usati nella pratica clinica sono gli antiaritmici di classe III come l’amiodarone,
il recente dronedarone ed il sotalolo. Entrambi agiscono sui canali del
potassio prolungando il potenziale d’azione ed il periodo refrattario
assoluto. Essi non sono antiaritmici di classe II puri dato che l’amiodarone è anche un inibitore dei canali del sodio mentre il sotalolo
ha anche un effetto beta-bloccante. Il più recente dronedarone ha effetti elettrofisiologici simili a quelli dell’amiodarone, ma non contiene Iodio,
responsabile degli effetti avversi dell’amiodarone sulla tiroide. Questi
farmaci si sono dimostrati più efficaci di quelli di classe I, ma sono
gravati da effetti collaterali importanti. Essi, prolungando il potenziale d’azione causano inevitabilmente un allungamento dell’intervallo QT e
21
elettrolitici, predispongono a torsione di punta. L’amiodarone inoltre ha
effetti collaterali sistemici importanti, soprattutto a carico dei polmoni e
della tiroide, che spesso causano la sospensione del farmaco da parte del
paziente. Il Dronedarone ha mostrato di aumentare la mortalità nei
pazienti con grado avanzato di scompenso cardiaco e, malgrado l’impiego ancora limitato, ha mostrato alterazioni anche importanti della
funzione renale. Gli altri farmaci disponibili per il controllo del ritmo
sono usati in maniera molto limitata e sono di fatto scomparsi dalla pratica clinica. Veniamo ora all’argomento che ci interessa di più e cioè
quello dell’efficacia di questa strategia terapeutica. Una recente
metanalisi (2009) condotta su tutti gli studi effettuati allo stato dell’arte
sulla terapia farmacologica antiaritmica ha documentato una efficacia
generale del 52%. È importante considerare il fatto che la percentuale di
successo, intesa come assenza di aritmia, risultava del 24,9% nei pazienti trattati con placebo. Il farmaco più efficace è risultato l’amiodarone con
una efficacia sei volte superiore a quella del placebo e due volte
superiore a quella del propafenone. È doveroso sottolineare il tasso di
complicanze che è venuto fuori da questi studi. Più del 10% dei pazienti
è stato costretto a sospendere la terapia per eventi avversi e più del 13%
Introduzione
22
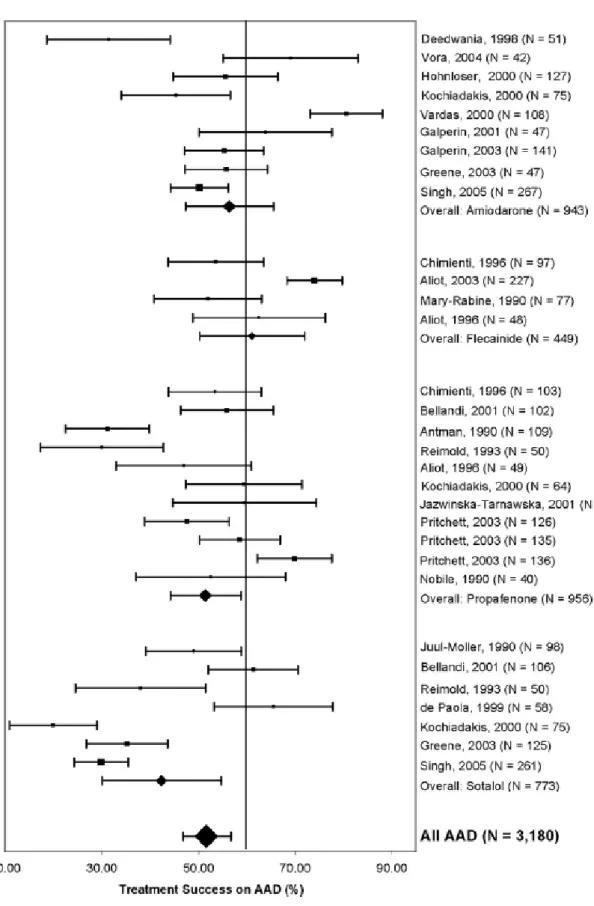
Figura 3. L'immagine mostra i risultati in termini di % di successo degli studi effettuati sulla terapia farmacologica antiaritmica per la fibrillazione atriale.
da H. Calkins et al; Circulation 2009
23
Dalla nostra trattazione si evince che la terapia farmacologica ha una
efficacia sicuramente limitata (di poco superiore al 50%) a fronte di
effetti collaterali significativi. Un argomento fondamentale nella pratica
clinica quotidiana è la scarsa maneggevolezza di questi farmaci. Essi
hanno tutti controindicazioni importanti e spesso è difficile a trovare l’antiaritmico che dia un buon profilo di sicurezza nello specifico
paziente. Queste limitazioni portano spesso i medici ad “accontentarsi”
di una strategia terapeutica rivolta al controllo del ritmo anche quando il
controllo della frequenza risulta perseguibile o sottodosare la terapia nel tentativo di “arginare” gli effetti avversi. Questo bisogno di terapie più
sicure ed efficaci ha portato, soprattutto nel corso degli ultimi quindici
anni, la ricerca a spingere verso soluzioni “curative” definitive per la
fibrillazione atriale e quindi allo sviluppo delle terapie interventistiche
che discuteremo di seguito e che assumono una importanza
fondamentale per lo studio che ci accingiamo a presentare in queste
L’ablazione transcatetere della fibrillazione atriale
Storia
Storicamente il primo approccio non farmacologico diretto al trattamento della fibrillazione atriale è stato l’ablazione del nodo atrio-ventricolare
nell’ambito della strategia ablate and pace menzionata in precedenza. Il
primo tentativo di trattare la fibrillazione atriale mediante la creazione di lesioni all’interno degli atri risale agli inizi degli anni novanta con gli
studi condotti dal cardiochirurgo americano Cox. Questo approccio
terapeutico prevedeva la creazione di lesioni lineari all’interno dell’atrio sinistro e dell’atrio destro. Tali lesione dividevano gli atri, da un punto di
25
“sentiero” di attivazione preferenziale tra il nodo del seno ed il nodo
atrio-ventricolare. Tale procedura venne denominata MAZE e si
dimostrò efficace nel prevenire le recidive di fibrillazione atriale anche
grazie al fatto che, giudicando con le conoscenze attuali, portava
inevitabilmente all’isolamento elettrico delle vene polmonari.
Naturalmente, essendo una procedura altamente invasiva, essa non è
stata mai accettata come terapia di prima linea per il trattamento della
fibrillazione atriale. La vera svolta, in realtà, si ebbe alla fine degli anni
novanta grazie agli studi condotti dal gruppo di Bordeaux guidati dall’elettrofisiologo francese Michel Haissaguerre. Essi dimostrarono il
ruolo causale svolto da foci presenti all’interno delle vene polmonari
nell’innesco della fibrillazione atriale. I loro studi aprirono la strada alla
strategia terapeutica ampiamente accettata ai giorni nostri che prevede l’isolamento elettrico delle vene polmonari come il caposaldo della
terapia non farmacologica della fibrillazione atriale. Da allora molti
progressi in questo campo sono stati fatti e nuove teorie si sono affacciate all’orizzonte. Le vene polmonari sembrano avere il ruolo di
“initiator” dell’aritmia. Appare chiaro oggi, in accordo con i
numerosissimi studi clinici effettuati sull’argomento, che l’isolamento
L’ablazione della fibrillazione atriale
26
procedura di ablazione e che altri approcci sono solo complementari
senza poter sostituire questa tecnica. Questa tecnica, nel corso dell’ultimo decennio, ha avuto un successo senza precedenti vedendo
moltiplicare il numero di pazienti sottoposti ad ablazione. Oltre all’isolamento delle vene polmonari ulteriori tecniche e tipi di lesione
sono stati proposti per migliorare la percentuale di successo della
procedura anche se ad oggi non esistono evidenze veramente forti per
nessuna di queste. Le ricerche si sono concentrate soprattutto sulla
possibilità di agire, oltre che sugli initiator, anche sui perpetuator dell’aritmia e quindi sulla possibilità di modificare elettricamente il
substrato che consente all’aritmia di autosostenersi. Sono state proposte
a riguardo numerose teorie che esamineremo in dettaglio nel capitolo
successivo. Ora, come abbiamo fatto nel corso della trattazione relativa
alla terapia farmacologica, ci preme discutere le tecniche utilizzate, l’efficacia di questa procedura e le eventuali complicanze a cui il
27
Tecnica
Abbiamo accennato precedentemente al fatto che le vene polmonari
costituiscono il trigger maggiore per lo sviluppo di fibrillazione atriale. I
battiti prematuri originati da queste strutture interagiscono con il substrato atriale a livello dell’antro delle vene polmonari, cioè il luogo di
congiunzione anatomica tra queste e l’atrio. Le vene polmonari, oltre a
svolgere la funzione di triggers, sono implicate, in accordo con le
evidenze di numerosi studi, anche nel mantenimento della fibrillazione
atriale, cioè come perpetuators. Lo scopo dell’ablazione della
fibrillazione atriale è proprio quello di interrompere la connessione tra le vene polmonari e l’atrio sinistro. La connessione può essere interrotta a
vari livelli, ma le evidenze attuali suggeriscono che essa deve essere
interrotta a livello antrale, cioè creando una lesione sufficientemente
ampia e prossimale allo sbocco della vena. Questo perché è stato
dimostrato che la massima anisotropia delle fibre muscolari si trova non
solo a livello della parte prossimale della vena, ma soprattutto è distribuita intorno all’area di sbocco in atrio di quest’ultima. Grazie al
rapido sviluppo delle tecnologie applicate a questa metodica esistono diversi sistemi deputati a localizzare i cateteri all’interno dell’atrio
L’ablazione della fibrillazione atriale
28
sinistro e di conseguenza a posizionare con esattezza le lesioni effettuate all’interno dello spazio tridimensionale. Inizialmente veniva usata la
semplice fluoroscopia che dava, però, una informazione solo
bidimensionale. Successivamente sono stati introdotti sistemi di
mappaggio elettroanatomici che, sfruttando un campo elettrico o
magnetico creato intorno al paziente e più recentemente con l’ausilio
della ecografia intracardiaca, riescono a ricostruire in maniera
tridimensionale le strutture cardiache ed a localizzare i cateteri e le lesioni effettuate con una precisione millimetrica. L’utilizzo di questi
sistemi ha accresciuto notevolmente la percentuale di successo ed il
profilo di sicurezza delle procedure riducendo in maniera significativa i
tempi di esposizione radioscopica del paziente. Per quello che riguarda le
fonti di energia utilizzate per creare le lesioni la più usata è sicuramente la radiofrequenza. Un’altra fonte energetica usata con successo è la
crioablazione. L’endpoint della procedura è quella di ottenere un blocco
completo della conduzione bidirezionale tra atrio sinistro e vene
polmonari in modo da avere una attività elettrica nelle vene dissociata da quella dell’atrio. All’isolamento delle vene polmonari è possibile
aggiungere, anche se con evidenze scientifiche discutibili, l’isolamento
29
fibrillazione atriale e la de connessione del seno coronaria ottenuta
mediante una lesione circolare intorno al suo sbocco in atrio destro. Oltre all’isolamento delle vene polmonari esistono altre tecniche
proposte per incrementare le possibilità di successo della procedura. Una
di queste, molto utilizzata anche se accettata con molte riserve dagli esperti, è la creazione di lesioni lineari all’interno dell’atrio sinistro per
scongiurare la possibilità di formazione di aritmie da macrorientro. Tali
linee di lesione vengono create più frequentemente a livello del tetto dell’atrio sinistro, tra le vene polmonari superiori, ed a livello dell’istmo
mitralico, tra l’anello e la vena polmonare inferiore di sinistra.
L’efficacia di questa tecnica non è stata ancora ben dimostrata e, in
alcuni trials, essa è risultata addirittura aritmogena. Alcuni studi
randomizzati sono tuttora in corso per chiarire il ruolo di questa tecnica come adiuvante all’isolamento delle vene polmonari. Un altro grosso
capitolo relativo alle tecniche di ablazione della fibrillazione atriale è
quello che riguarda il tentativo di modificare i perpetuators, cioè il substrato responsabile del mantenersi dell’aritmia. Nell’ipotesi
attualmente accettata il substrato sarebbe costituito da zone di tessuto a
bassa velocità di conduzione. Queste zone favorirebbero i meccanismi di microrientro dell’impulso e di conseguenza la formazione dei cosiddetti
L’ablazione della fibrillazione atriale
30
“rotors”. Nel tentativo di intercettare queste zone nel 2004
l’elettrofisiologo americano Nademanee propose una tecnica di
ablazione basata sul mappaggio e la successiva ablazione di zone a
potenziale molto veloce, di bassa ampiezza e frammentato che lui
chiamò CFAEs. Usando questo approccio riuscì, verificando i risultati
con uno studio randomizzato, ad ottenere le stesse percentuali di successo dell’ablazione tradizionale senza effettuare l’isolamento delle
vene polmonari. Da allora nessun altro gruppo è riuscito ad emulare i
suoi risultati. Alcuni studi hanno testato questa tecnica come
complementare all’isolamento delle vene polmonari riconoscendole la
capacità di aumentare il successo della procedura soprattutto nei pazienti
con fibrillazione atriale persistente e permanente. Oltre a questa altre
tecniche sono state proposte, ma esse sono di quasi nessun impiego nella
pratica clinica e per tale motivo consideriamo superflua la loro
trattazione ai fini del nostro studio.
Efficacia
La capacità dell’ablazione transcatere di “guarire” i pazienti dalla
31
precisare subito che le percentuali di successo che vengono attribuite alla procedura variano notevolmente da un trial all’altro a seconda della
tecnica utilizzata, del tipo di fibrillazione atriale, dell’esperienza del
centro e, soprattutto, in base al metodo utilizzato per eseguire il
follow-up. Quest’ultimo, infatti, assume una importanza fondamentale dato che
le recidive di aritmia possono essere asintomatiche e di breve durata e
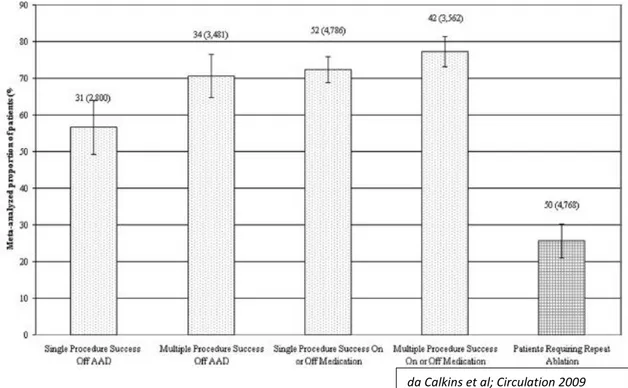
quindi difficili da diagnosticare. Una recente meta-analisi sull’argomento ha mostrato che la percentuale di successo generale dell’ablazione dopo
una singola procedura ed in assenza di farmaci antiaritmici è del 57%
riferendosi a 31 braccia di studi clinici e 2800 pazienti trattati. La
percentuale di successo sale notevolmente dopo procedure multiple
arrivando a 71%. Con procedure multiple e terapia antiaritmica in corso
la percentuale di successo è risultata del 77% e dopo singola procedura del 72%. La tecnica utilizzate per l’ablazione nei trial presi in
considerazione prevedeva l’utilizzo di un sistema elettroanatomico solo
nel 30% dei casi. L’uso di questi sistemi ha mostrato ridurre i tempi di
fluoroscopia in maniera significativa. Un’altra meta-analisi effettuata su
grandi numeri ha mostrato che la percentuale di successo in assenza di farmaci antiaritmici era del 52% e saliva a 76% con l’uso dei farmaci.
L’ablazione della fibrillazione atriale
32
significativa nell’outcome clinico tra i diversi tipi di fibrillazione atriale.
I pazienti con fibrillazione atriale parossistica sono quelli che hanno
mostrato i risultati migliori con una percentuale di successo che è
arrivata anche al 90% in alcuni studi. A seguire i pazienti con
fibrillazione atriale persistente. Il risultato peggiore si è ottenuto nei
pazienti con fibrillazione atriale permanente. In questi pazienti la
percentuale di successo supera di poco il 50%.
Figura 4. Efficacia dell'ablazione di FA
Da questi dati emerge un concetto fondamentale per la pratica clinica: l’ablazione transcatetere è più efficace della terapia farmacologica nel
33
prevenire le recidive di fibrillazione atriale ed è una opzione clinica valida. Le attuali linee guida suggeriscono di considerare l’ablazione nei
pazienti sintomatici che siano stati refrattari ad almeno un farmaco
antiaritmico. Il razionale è quello di provare con la terapia
farmacologica, a basso costo e relativamente efficace, e passare poi subito all’ablazione nel caso in cui l’aritmia non venga controllata.
Complicanze
Le complicanze legate all’ablazione transcatetere sono un argomento
spinoso della cardiologia. Dimostrata comunque la buona percentuale di
successo, i detrattori la prendono scarsamente in considerazione nella
pratica clinica adducendo la motivazione che essa rappresenta una procedura a rischio elevato. Il concetto fondamentale è che l’ablazione è
una valida alternativa ai farmaci, ma è risolutiva in una percentuale dei casi che non arriva all’80%. Possiamo considerarla una alternativa valida
solamente se siamo in grado di offrire al paziente una percentuale di
complicanze accettabile se paragonata ai rischio di vivere con la
fibrillazione atriale. Il tasso di complicanze riportato in letteratura varia
L’ablazione della fibrillazione atriale
34
alle metodiche utilizzate. Una recente meta-analisi internazionale
condotta tra i centri a più alto volume dal dott. Cappato ha riportato una percentuale generale di complicanze legate all’ablazione transcatetere
del 4,5%.
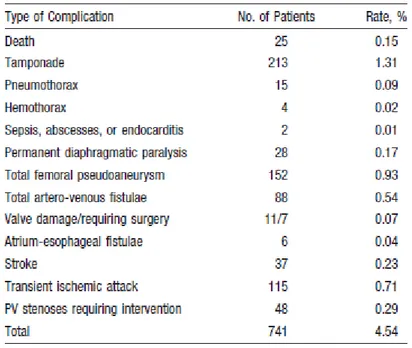
Figura 5. Complicanze osservate durante ablazione di FA e loro frequenza.
La complicanze più comune è risultata essere il tamponamento cardiaco
che si è verificata nell’ 1,3% dei casi. Altre complicanze comuni sono
risultate essere quelle legate agli accessi venosi come le fistole
artero-venose e gli pseudoaneurismi. I TIA si noso verificati nello 0,71% dei
da Cappato et al.; Circulation2010
35
casi e gli stroke nello 0,23%. Stenosi delle vene polmonari che hanno
richiesto un intervento si sono verificate nello 0,29% dei casi. Nello
studio si sono osservate 25 morti legate alla procedura che rappresentano
una percentuale dello 0,15%. Questi numero sono in accorso con altri
studi effettuati sulle complicanze ed è doveroso osservare che la
percentuale di eventi avversi non è risultata inferiore nei centri a
maggiore esperienza. Se paragonata agli effetti avversi della terapia
farmacologica, questa percentuale di complicanze appare del tutto
accettabile.
Conclusioni
Dai dati presentati fino ad ora si evince chiaramente che l’ablazione
transcatetere rappresenta una valida strategia di trattamento nei pazienti con fibrillazione atriale. Uno dei problemi maggiori nell’uso di questa
metodica nella pratica clinica è la scarsa disponibilità di elementi e dati
clinici che abbiano valore predittivo di successo o insuccesso della procedura. Sicuramente l’eliminazione dei triggers rappresenta il
“cornerstone” di ogni procedura di ablazione e questo si è ottenuto in
maniera efficace mediante lo sviluppo delle tecniche di isolamento delle
L’ablazione della fibrillazione atriale
36
nell’insuccesso della procedura e come cercare di modificare questa
situazione. Noi crediamo che la maggiore causa di insuccesso sia legata
non all’inefficace eliminazione dei triggers, ma all’alterazione strutturale
del miocardio atriale, alterazione contro la quale le tecniche di ablazione possono fare ben poco. Una delle alterazioni fondamentali nell’ambito
del rimodellamento atriale è la comparsa di fibrosi. Il nostro scopo è
presentare un metodo semplice ed efficace che dia una stima del grado di
rimodellamento atriale e verificare sperimentalmente se esso sia in grado
di essere usato come predittore di successo della procedura di ablazione.
Nel prossimo capitolo analizzeremo nel dettaglio le alterazioni ultrastrutturali che portano al rimodellamento dell’atrio e la loro
Rimodellamento strutturale dell’atrio e suo ruolo nel successo dell’ablazione della fibrillazione atriale.
Tra i meccanismi che stanno alla base della genesi e del mantenimento
della fibrillazione atriale uno dei più importanti è senza dubbio il
rimodellamento degli atri. Questo si espleta a vari livelli ed in diverse
forme. Possiamo distinguere un rimodellamento elettrico, che avviene poco dopo l’instaurarsi della fibrillazione atriale, un rimodellamento
contrattile, che impiega più tempo ad instaurarsi ed infine un rimodellamento strutturale che comporta profonde modifiche all’architettura istologica degli atri. Quest’ultimo tipo di rimodellamento
impiega un tempo abbastanza lungo per attuarsi e comporta
Il rimodellamento atriale
38
soffermeremo sui meccanismi che stanno alla base del rimodellamento
strutturale e sul ruolo di tale rimodellamento nella genesi e nel
mantenimento della fibrillazione atriale oltre che sulla sua importanza
nel determinare il successo della procedura di ablazione transcatetere.
La fibrosi atriale.
La fibrosi è il meccanismo principale del rimodellamento strutturale
nella fibrillazione atriale. Essa deriva da un accumulo di fibre collagene.
Tale accumulo deriva in parte dalla sostituzione fibrotica di miocardio
andato in necrosi ed in parte da processi reattivi che causano espansione
interstiziale. La fibrosi è il processo terminale di differenti insulti al miocardio come l’invecchiamento, lo scompenso cardiaco, le malattie
valvolari e la cardiopatia ischemica. La fibrosi assume un ruolo
determinante nella patogenesi della fibrillazione atriale. Un aumento
della deposizione delle fibre collagene a livello atriale è stato riscontrato
in pazienti con fibrillazione atriale e cuore sano ed inpazienti con
malattie valvolari e fibrillazione atriale. Un altro studio ha mostrato la
correlazione tra il volume della matrice extracellulare e la persistenza
39
aiutato a chiarire il ruolo della fibrosi nella fibrillazione atriale. In alcuni
studi effettuati sui cani la stimolazione ventricolare cronica a frequenza
elevata produce sviluppo di fibrillazione atriale ed un pattern di fibrosi
interstiziale comparabile a quella osservata in clinica. Lo studio di questi
atri ha rivelato zone di miocardio a conduzione rallentata che
costituiscono la base elettrofisiologica per fenomeni di rientro e blocchi
di conduzione. Anche la stimolazione atriale ad elevata frequenza, in
presenza di normale frequenza ventricolare, è stato dimostrato aumentare
il volume della matrice extracellulare confermando il fatto che anche la
fibrillazione atriale da sola, in assenza di patologia cardiaca, induce il rimodellamento strutturale dell’atrio.
Meccanismi cellulari di fibrosi atriale.
Molti studi sono stati effettuati anche per chiarire quali siano i
meccanismi alla base della formazione di fibrosi a livello del miocardio
atriale. La perdita di miocardiociti, sia per necrosi che per apoptosi, è
stata osservata procedere di pari passo con lo sviluppo di fibrosi.
Possiamo distinguere una fibrosi ripartiva, che è quella che si sviluppa
Il rimodellamento atriale
40
caratterizzata da una deposizione di fibre collagene tra i fasci di
miocardiociti . Tale tessuto fibrotico costituisce una barriera di separazione fisica tra i miociti ed altera la propagazione dell’impulso
elettrico. È stato osservato che tale deposizione fibrotica altera anche la
funzione e la distribuzione delle connexine che sono proteine localizzate
a livello delle gap-junctions tra i miociti e garantiscono la connessione elettrica a bassa resistenza tra una cellula e l’altra. La fibrosi è il risultato
di numerosi segnali ormonali con effetto profibrotico che spesso
agiscono in contemporanea. Uno di questi, molto ben caratterizzato, è l’Angiotensina II. Il sistema renina-angiotensina-aldosterone è implicato
nella fibrosi miocardiaca nell’ipertensione arteriosa, lo scompenso
cardiaco, la cardiopatia ischemica e le cardiomiopatie. L’angiotensina II
prodotta a livello del miocardio atriale si è dimostrata associata con l’apoptosi dei miociti e los viluppo di fibrosi. In topi transgenici
l’iperespressione dell’ enzima ACE a livello cardiaco ha determinato la
dilatazione dell’atrio e lo sviluppo di fibrillazione atriale. Inoltre
l’angiotensina II promuove la formazione delle specie reattive
dell’ossigeno attraverso l’attivazione dell’enzima NADPH ossidasi.
41
atriale dell’enzima ACE e l’attivazione dei segnali intracellulari di
trasmissione dell’angiotensina II in tessuti umani fibrillanti.
Anche l’Aldosterone sembra giocare un ruolo importante nel
promuovere lo sviluppo di fibrosi atriale. L’infusione di aldosterone
genera fibrosi atriale indipendentemente dallo stress di parete o dalla
presenza di ipertensione arteriosa in studi condotti su modelli animali.
Un'altra forte evidenza deriva dal fatto che i pazienti affetti da
iperaldosteronismo primitivo hanno un rischio di sviluppare fibrillazione
atriale pari a 12 volte il rischio dei soggetti sani. Un altro mediatore che
assume una importanza significativa nel promuover lo sviluppo di fibrosi
a livello atriale è il TGFB1. Esso è fortemente profibrotico data la
capacità di promuovere la differenziazione dei fibroblasti e la sintesi di
collagene. Il TGFB1 inoltre promuove la formazione delle specie reattive
da Burstein e Nattel, JACC 2008
Il rimodellamento atriale
42
dell’ossigeno. In modelli animali transgenici la iperespressione di
TGFB1 causa fibrosi atriale selettiva, disomogeneità di conduzione ed
una propensione allo sviluppo di fibrillazione atriale. Anche l’infiammazione e lo stress ossidativo promuovono la formazione di
fibrosi a livello atriale. Infiltrati infiammatori sono stati dimostrati in
molto modelli animali di fibrillazione atriale. Anche biopsie ottenute da
pazienti affetti da fibrillazione atriale hanno mostrato la presenza di
infiammazione e danni da stress ossidativo. Alcuni studi hanno mostrato
una correlazione positiva tra i livelli di proteina C reattiva, un potente
marker di infiammazione, e la persistenza di fibrillazione atriale.
da Burstein e Nattel, JACC 2008
43
Tutti questi fattori agiscono nella cellula in maniera sinergica e
differente a seconda della patologia cardiaca che è alla base sel
rimodellamento. La fibrosi si genera quando i fattori profibrotici
circolanti e quelli prodotti localmente alterano l’equilibrio tra produzione
e degradazione di fibre collagene. Esiste una complessa interazione tra i diversi tipi cellulari ed al centro di questa c’è il fibroblasto.
L’esposizione all’angiotensina II ed al TGFB1 influenza in maniera
significativa le funzioni del fibroblasto aumentando la secrezione di
proteine della matrice extracellulare. Anche lo stress meccanico di parete
aumenta la sintesi di collagene agendo sui fibroblasti. Questi ultimi,
inoltre, possono influenzare direttamente le funzioni elettriche dei
miocardiociti in risposta allo stress di parete. Tutte queste considerazioni
sul ruolo del sistema renina-angiotensina-aldosterone e del TGFB1 nello sviluppo della fibrosi atriale hanno portato all’esecuzione di diversi studi
clinici diretti a capire se una terapia appropriata (con ACE inibitori, sartani ecc.) potesse influenzare l’outcome clinico nei pazienti affetti da
fibrillazione atriale. Purtroppo questi studi sulla cosiddetta “upstream
therapy” hanno dato risultati contrastanti e siamo lontani da una risposta
Il rimodellamento atriale
44
Metodiche cliniche per valutare la presenza di fibrosi atriale e loro valore come predittori di successo dell’ablazione transcatetere.
La correlazione tra dilatazione dell’atrio sinistro e fibrillazione atriale è
conosciuta in clinica da più di 50 anni. La presenza di dilatazione dell’atrio sinistro di è rivelata un buon predittore di successo a lungo
termine della cardioversione elettrica. Quanto la causa della dilatazione
sia imputabile al rimodellamento strutturale ed alla comparsa di fibrosi è
stato indagato solo recentemente. Con un elegante studio pubblicato nel
2007 Knackstedt ed i suoi colleghi dimostrarono la correlazione tra
dilatazione atriale misurata con l’ecocardiografia e la presenza di fibrosi
allo studio autoptico in auricole di cani. Da un punto di vista clinico le
dimensioni atriali aumentate sono un fattore di rischio per recidiva di
fibrillazione atriale dopo il trattamento di ablazione. Questo si è
dimostrato vero, però, soltanto per gli atri fortemente dilatati , mentre per
gli atri moderatamente dilatati i dati in letteratura risultano contrastanti.
Quello che si è dimostrato sicuramente un fattore di rischio per recidiva
di aritmia dopo RFCA è la presenza di fibrosi. Mappando in modo invasivo le aree di fibrosi all’interno dell’atrio sinistro, nel 2005 Verma
et al. dimostrarono che l’estensione delle aree di scar è un predittore
45
sono state proposte diverse metodiche, utilizzabili in clinica, per “misurare” la quantità di fibrosi a livello dell’atrio sinistro nei pazienti
da sottoporre ad ablazione della fibrillazione atriale. Gli studi effettuati
con la risonanza magnetica usando la metodica del late-enhancement per
visualizzare le aree di cicatrice a livello atriale hanno mostrato una
chiara correlazione tra estensione delle aree fibrotiche ed outcome
clinico dei pazienti sottoposti ad ablazione della fibrillazione atriale.
Studi effettuati dallo stesso gruppo di ricercatori hanno mostrato anche la
relazione inversa tra la fibrosi misurata con la risonanza magnetica e lo
strain-rate atriale misurato all’ecocardiografia. Altri ricercatori hanno
proposto metodiche ecocardiografiche per quantificare la fibrosi atriale.
Un gruppo olandese di Leiden ha proposto recentemente una tecnica
basata sulla reflettività agli ultrasuoni della parete atriale. Secondo la
loro ipotesi un indice chiamato IBS (calibrated integrated backscatter) è in grado di dare una stima della presenza di fibrosi all’interno dell’atrio
sinistro e può essere usato come predittore di successo nell’ablazione
della fibrillazione atriale. Ulteriori studi sono stati effettuati con la
tomografia computerizzata. Nedios e colleghi hanno messo a punto una
metodica basata sulla TC che si basa sulla ricostruzione tridimensionale dell’atrio sinistro e la successiva divisione di questo in due porzioni, una
Il rimodellamento atriale
46
anteriore e una posteriore. Il rapporto tra il volume della porzione anteriore ed il volume totale dell’atrio è stato definito “asymmetry
index”(ASI) e messo in relazione al successo della procedura di
ablazione. Un altro studio effettuato con la TC ha dimostrato la superiorità di questa nella stima dell’effettiva dilatazione atriale e la
capacità, soprattutto negli atri più dilatati, di predire il successo della
procedura di ablazione. Dalla nostra trattazione emerge il concetto che la presenza di rimodellamento strutturale dell’atrio, comunque esso venga
misurato, condiziona in maniera significativa le possibilità di successo dell’ablazione della fibrillazione atriale. Sicuramente non esiste ad oggi
una metodica accettata su larga scala e soprattutto prontamente
disponibile in clinica che dia una stima della gravità del rimodellamento
atriale. La possibilità di disporre di una metodica del genere derebbe la
possibilità di scegliere in maniera più oculata i possibili candidati all’ablazione ed in ultima analisi di migliorare l’outcome della
Il nostro studio
Ipotesi
Come abbiamo visto nelle pagine precedenti la fibrillazione atriale
costituisce un problema della medicina moderna data la morbilità e la
mortalità che essa comporta. Abbiamo anche discusso del fatto che il
trattamento farmacologico si è dimostrato scarsamente efficace nel prevenire le recidive di aritmia e che l’ablazione transcatetere costituisce
una alternativa terapeutica valida. Dalla nostra trattazione dell’ablazione
sono venuti fuori alcuni concetti a mio avviso significativi. Il primo è
sicuramente il fatto che la procedura di ablazione ha un buon profilo di
sicurezza, soprattutto se effettuata con le tecniche più moderne ed in
mani esperte. Il secondo è che, purtroppo, le percentuali di successo della procedura restano “incollate” agli stessi numeri da più di dieci anni
Il nostro studio
48
ogni angolo del pianeta. Questo deriva in gran parte dalla nostra scarsa
conoscenza dei meccanismi di base, che sono poi quelli determinanti,
sulla genesi e sul mantenimento della fibrillazione atriale. Nel campo della ricerca sull’ablazione, paradossalmente, stiamo procedendo a
“tentoni”; corretto sarebbe seguire una ipotesi ben precisa e cercare di
dimostrarla per via sperimentale. Un luminare dell’aritmologia mondiale
ha definito questo atteggiamento “learning while burning” e io penso che
ciò descriva benissimo quello che sta accadendo. Tale atteggiamento ha
generato una enorme confusione tra gli addetti al settore e, ancora di più,
tra i non addetti. Oggi la corretta selezione dei pazienti da sottoporre ad
ablazione è la chiave del successo del trattamento clinico. I pazienti con
cuore sano, atrio lievemente dilatato e fibrillazione atriale parossistica
non generano alcun dubbio nel medico curante: essi sono i candidati
ideali date le altissime probabilità di successo della procedura. Tolti
questi pazienti si apre una immensa zona grigia. È veramente difficile,
stando alle conoscenze attuali, prevedere le possibilità di successo dell’ablazione in un paziente che abbia una fibrillazione atriale
persistente, atrio dilatato e qualche patologia cardiaca. In questi pazienti
il successo del trattamento, più che basso, è imprevedibile ed è questo che genera l’imbarazzo nella decisione clinica. Abbiamo cercato di
49
spiegare, nelle pagine precedenti, che i pazienti della “zona grigia” sono
quelli in cui il rimodellamento atriale assume un ruolo di primo ordine
nel determinare il successo della procedura di ablazione. È stato
dimostrato che tale processo di rimodellamento stravolge profondamente le funzioni meccaniche ed elettriche dell’atrio portando al circolo vizioso
“atrial fibrillation begets atrial fibrillation” che è deleterio per le
possibilità di mantenimento del ritmo sinusale. Ad oggi esistono tecniche
per quantificare la presenza di fibrosi all’interno dell’atrio, ma, quelle
più affidabili come la risonanza magnetica, sono molto costose e non prontamente disponibili sul territorio. L’indice a cui i medici si affidano
maggiormente è il calcolo delle dimensioni dell’atrio sinistro all’ecocardiografia transtoracica, metodica semplice e prontamente
disponibile. Questo indice ha dato buoni risultati come predittore di
successo della procedura di ablazione negli atri normali o in quelli
severamente dilatati, mentre appare di scarso valore in presenza di
dimensioni atriali moderatamente aumentate. Lo scopo del nostro studio
è quello di fornire un indice semplice, a basso costo e prontamente disponibile che aiuti il cardiologo nel “quantificare” la presenza di
rimodellamento atriale e quindi nella scelta dei pazienti da sottoporre ad
Il nostro studio
50
convinti che il rimodellamento atriale sia strettamente correlato con le dimensioni dell’atrio sinistro crediamo che esista un modo più accurato
per determinare “quanto” l’atrio sia dilatato.
Il rapporto LA /RAo
Nel nostro studio abbiamo considerato, come indice di dilatazione e quindi rimodellamento dell’atrio sinistro, non solo le sue dimensioni
effettive, ma il rapporto tra questo e la radice aortica. Abbiamo scelto
una popolazione di pazienti con cuore sano, affetti da fibrillazione atriale
persistente. In tale popolazione sarebbe difficile immaginare una
dilatazione della radice aortica in assenza di patologia cardiaca specifica.
Abbiamo considerato la radice aortica, quindi, come un marker delle “dimensioni” del cuore ed abbiamo stabilito quanto l’atrio sinistro fosse
dilatato rispetto ad essa. In assenza di una patologia cardiaca o valvolare,
una eccessiva dilatazione dell’atrio sinistro significa la presenza di una
malattia che coinvolge in maniera specifica gli atri e ne determina il
rimodellamento. Nel gruppo di pazienti considerato questa patologia è la
fibrillazione atriale che, essendosi sviluppata in forma persistente, ha
51
atriale di cui discutevamo sopra. In questo modo siamo riusciti ad avere
una stima delle dimensioni atriali non condizionata dalle classiche
formule di indicizzazione per superficie corporea che, in presenza di
distribuzioni fuori dalla norma della massa magra e grassa, generano sovrastime o sottostime delle dimensioni dell’atrio. Abbiamo osservato,
in poche parole, quanto l’atrio è grande rispetto al resto del cuore.
L’indice Atrio/Aorta era stato già studiato in precedenza da altri
ricercatori. Nel 2008 Kimura e coll. dimostrarono la validità di questo indice nel dare una stima reale dell’ingrandimento atriale e quindi di
rivelare patologie cardiache sottostanti. La nostra ipotesi è che, nel
gruppo di pazienti preso in considerazione e sottoposto ad ablazione di FA, l’indice Atrio/Aorta correli con il successo della procedura e,
soprattutto, correli con esso meglio della semplice misurazione delle dimensioni dell’atrio sinistro.
Selezione dei pazienti
La nostra ipotesi si basa sul fatto che le dimensioni dell’atrio sinistro,
misurate tramite il rapporto atrio/aorta, possano essere espressione del rimodellamento strutturale dell’atrio e di conseguenza del grado di
Il nostro studio
52
fibrosi presente a livello miocardico. Come abbiamo accennato in precedenza il rimodellamento strutturale dell’atrio è un processo che
impiega tempo ad attuarsi. Per tale motivo abbiamo incluso nel nostro
studio pazienti affetti da fibrillazione atriale persistente, intesa come
episodi di aritmia di durata maggiore di 7 giorni o che abbiano richiesto
un intervento esterno per il ripristino del ritmo sinusale che avessero
indicazione ad effettuare la procedura di ablazione perché sintomatici e
dopo che avesse fallito almeno un farmaco antiaritmico. Dato il ruolo di
riferimento delle dimensioni della radice aortica nel nostro studio i
pazienti con dilatazione della radice aortica sono stati esclusi. Sono stati
esclusi anche i pazienti con ipertensione arteriosa severa non controllata
dalla terapia farmacologica. Il processo di rimodellamento e la conseguente dilatazione dell’atrio sinistro possono essere causati da vari
agenti eziologici ed uno dei più importanti tra questi è rappresentato
dalle patologie della valvola mitrale. Dato che compito del nostro studio
era quello di identificare una metodica capace di dare una stima del rimodellamento dell’atrio dovuto a fibrillazione atriale abbiamo preferito
escludere i pazienti affetti da valvulopatia mitralica significativa che
avrebbe determinato recidive di aritmia non strettamente correlate solo al
53
l’aumento di pressione nell’atrio sinistro e lo stress di parete. Sono stati
anche esclusi i pazienti sottoposti a chirurgia cardiaca. I pazienti andati
incontro ad intervento cardiochirurgico successivamente
all’arruolamento nello studio sono stati esclusi in una fase successiva. I
pazienti con frazione di eiezione inferiore al 50% sono stati esclusi dato
il rischio elevato di recidive di aritmia legato alla patologia di base. I
pazienti con dimensioni antero-posteriori dell’atrio sinistro superiori a 55
mm sono stati esclusi perché abitualmente non trattati con ablazione
della fibrillazione atriale nel nostro centro. Sono stati esclusi anche i
pazienti con ipertrofia ventricolare sinistra significativa data la scarsa probabilità di successo dell’ablazione già dimostrata in questi pazienti.
I. Criteri di inclusione
Fibrillazione atriale persistente Frazione di eiezione >50%
Diametro A-P atrio sinistro <55 mm SIVd <16 mm
Assenza di valvulopatia mitralica significativa Assenza di ipertensione arteriosa di grado severo Assenza di dilatazione significativa della radice aortica Nessun precedente intervento cardiochirurgico