1
INDICE
INTRODUZIONE
CLASSIFICAZIONE E RUOLO PROGNOSTICO DEI
BIOMARCATORI
pag. 5BIOMARCATORI DI STRESS CARDIOMIOCITARIO
Peptidi natriuretici pag. 8 St-2 pag. 19
Fattore di crescita e differenziazione 15 (GDF15) pag. 20
DANNO MIOCITARIO ED APOPTOSI
Troponine pag. 21
INFIAMMAZIONE
TNF-alfa, sTNF-alfaR1, sTNF-alfaR2, CRP, IL-6 e PTX-3 pag. 24
STRESS OSSIDATIVO
Mieloperossidasi pag. 35
BIOMARCATORI DI RIMODELLAMENTO DELLA MATRICE EXTRACELLULARE
MMPs ed inibitori tissutali delle metalloproteinasi (TIMPs) pag. 37
2
BIOMARCATORI:
CONFRONTO
DEL
VALORE
PROGNOSTICO
Metalloproteinasi della matrice extracellulare e peptidi natriuretici pag. 43 St-2 e Galectin-3 pag. 45 TNF-alfa, sTNF-alfaR1, sTNF-alfaR2 e MMPs pag. 46
RAZIONALE
DELL’UTILIZZO
COMBINATO
DI
BIOMARCATORI E PARAMETRI ECOCARDIOGRAFICI
. . . .
pag. 48STUDIO SPERIMENTALE
Materiali e metodi pag. 62
Ecocardiogramma Doppler pag. 63 Analisi biomarcatori pag. 64 Analisi statistica pag. 65
Risultati pag. 66
Discussione pag. 72 Conclusioni pag. 74
3
INTRODUZIONE
L'identificazione dei pazienti ad alto rischio di outcome prognostico negativo, nonostante tutti i progressi fatti nella gestione dell’insufficienza cardiaca (IC), rimane una sfida.
L’IC è divenuta un peso importante nella sanità moderna, non solo in termini di morbilità e mortalità per i diretti interessati, ma anche per la società nel suo complesso, a causa dell’aumento dei costi di cura per questa categoria di pazienti.
Per una valutazione accurata di malattia, è importante sottolineare il ruolo clinico dei biomarcatori e delle alterazioni ecocardiografiche presenti in questa categoria di pazienti.
La determinazione dei biomarcatori nell’IC è stata vista, fino a poco tempo fa, come un supplemento elettivo per la valutazione diagnostica dei pazienti affetti da tale condizione. E' in questo contesto che l'interesse per i biomarcatori è in forte aumento.
I biomarcatori, che possono oggettivamente misurare e valutare un processo normale o patologico, od anche una risposta farmacologica ad un intervento terapeutico, sono validi strumenti in grado di quantificare i fenomeni fisiopatologici alla base della fenomenologia clinica.
Inoltre, per la valutazione diagnostica e prognostica dei pazienti con IC, un ruolo chiave è attribuito all’ecocardiografia, che, come indicato dalle linee guida, è la singola metodica più utile in questa patologia.
4
dell’IC attraverso informazioni sulla struttura e funzionalità delle camere cardiache e degli apparati valvolari (vedi volume e funzione sistolica e diastolica), e si è dimostrata non solo in grado di ridurre il rischio di mortalità, ma di fornire anche informazioni utili a migliorare la gestione clinica ed ottimizzare la terapia medica nel singolo paziente, considerando la variabilità interindividuale in termini funzionali ed emodinamici.
5
CLASSIFICAZIONE E RUOLO PROGNOSTICO DEI
BIOMARCATORI
I biomarcatori possono essere suddivisi in:
biomarcatori molecolari o di laboratorio;
biomarcatori funzionali, se correlati ad analisi del segnale, imaging o test funzionali;
biomarcatori genetici;
Perché un biomarcatore possa essere utile deve soddisfare alcune condizioni:
approfondimento del metodo con cui viene giudicato il biomarcatore attraverso mezzi statistici rigorosi e standardizzati;
misurazione dei valori facilmente eseguibile entro un breve periodo di tempo con sufficiente precisione;
riflettere il processo fisiopatologico coinvolto in presenza di IC e la sua progressione;
Dal punto di vista, invece, del significato clinico un biomarcatore può assumere il ruolo di fattore di rischio, marcatore di screening, indice diagnostico, staging index, indice prognostico, indice di risposta alla terapia. Infine, da un punto di vista più strettamente fisiopatologico, i diversi biomarcatori potranno indicare stress cardiomiocitario, attivazione neurormonale, danno cardiomiocitario, attivazione flogistica, rimodellamento ventricolare.
6
Un biomarcatore permette idealmente di individuare le eventuali sottostanti e potenzialmente reversibili cause di IC e di stimare la severità ed il rischio di progressione della malattia.
Saranno qui presi in considerazione, tra i numerosi biomarcatori che la letteratura ci propone, i peptidi natriuretici (PN), espressione della funzione endocrina cardiaca e biomarcatori dello stress sul cardiomiocita e, tra i biomarcatori neurormonali, quelli del sistema adrenergico e del sistema renina-angiotensina, i marcatori di infiammazione, di danno cardiomiocitario, di rimodellamento ventricolare, anche se altri test, in particolare di stress ossidativo, genetici ed indicatori di comorbilità assumono crescente interesse e significato per la valutazione del fenotipo individuale (1-5).
7
Tabella I Biomarcatori studiati nell’insufficienza cardiaca Neurormoni
Peptidi natriuretici (ANP, BNP, CNP e peptidi correlati) Marcatori di attività del sistema renina-angiotensina-aldosterone Catecolamine
Endoteline Cromogranina A e B
Arginina vasopressina e copeptina Adrenomedullina
Cortisolo Leptina Adiponectina Resistina
Marcatori di danno cardiaco (necrosi e apoptosi)
Troponina cardiaca (cTnI e cTnT)
Proteina legante gli acidi grassi cardiaci (H-FABP) Fas (APO-1)
Marcatori di rimodellamento della matrice, disfunzione endoteliale ed infiammazione
Metalloproteinasi della matrice e inibitori tissutali delle metalloproteinasi Propeptidi del collagene
Propeptide del collagene di tipo I e tipo III Molecole di adesione (ICAM, P-selectina) Proteina C-reattiva
Citochine e recettori correlati (IL-1, IL-2, IL-6, IL-8, IL-18, TNF-alfa, osteoprotegerina, ST2, GDF-15) Osteopontina
Galectina 3 Pentraxina 3
Marcatori di stress ossidativo
Lipoproteine a bassa densità ossidate Mieloperossidasi
Bioperine urinarie Isoprostani
Malondialdeide plasmatica Acido urico sierico Gamma-glutamiltransferasi
Marcatori ormonali e altri marcatori di cachessia
Alterazioni dell’asse adreno-ipofisario Triiodiotironina
IGF-1 e GH Colesterolo
8
BIOMARCATORI DI STRESS CARDIOMIOCITARIO
Tra i biomarcatori attualmente disponibili, il ruolo dei peptidi natriuretici in IC è oggetto di continui studi.
Peptidi natriuretici
Fin dalla metà del secolo scorso erano stati descritti dei granuli di secrezione nelle cellule atriali dei mammiferi (6). Nel 1981 de Bold (7-8) e collaboratori hanno osservato che l’infusione di estratti di tessuto atriale nei ratti provoca una rapida e consistente diuresi e natriuresi. Successivamente numerosi studi hanno portato rapidamente all’isolamento, la purificazione e l’identificazione di una famiglia di peptidi, denominata Atrial Natriuretic Peptides (ANP), mediatori dell’azione natriuretica e vasorilassante. Nel 1988 è stato dimostrato che non solo il tessuto atriale, ma anche i cardiomiociti ventricolari sono in grado di produrre dei peptidi con attività natriuretica: il Brain Natriuretic Peptide (BNP) (9), che prende questo nome in quanto inizialmente è stato isolato dal tessuto cerebrale di suino.
Altri peptidi appartenenti a questa famiglia sono stati descritti in seguito, come il C-type Natriuretic Peptide (CNP), l’urodilatina ed il Dendroaspis Natriuretic Peptide (DNP) (10).
Negli ultimi anni è stato evidenziato il ruolo dei peptidi natriuretici che vengono attivati e secreti in circolo nei pazienti con IC.
9
La funzione del miocardio, quindi, deve essere rivista, considerando anche le interazioni con altri organi ed apparati attraverso la trasmissione di segnali di tipo ormonale, paracrino e autocrino (9).
Struttura chimica
Dal punto di vista chimico tutti i peptidi natriuretici sono caratterizzati da un anello, formato da 17 residui aminoacidici, chiuso da un ponte disolfuro intramolecolare tra due residui di cistina. La lunghezza delle estremità amino- e carbossi- terminali variano tra le differenti classi di peptidi: ANP 28 aminoacidi, BNP 32, CNP 22 e DNP 38. Tutte le forme esistono sotto forma di un pre-ormone di peso molecolare relativamente elevato che viene scisso prima di essere immesso in circolo.
La struttura proteica dei peptidi natriuretici è molto ben conservata nel corso dell’evoluzione, soprattutto la porzione all’interno dell’anello cisteinico presenta in tutti gli iso-ormoni un’omologia di sequenza di 11 aminoacidi su 17; solo nel DNP l’omologia riguarda 10 aminoacidi su 17. La struttura ad anello risulta fondamentale nel mantenimento della funzione biologica e tale attività è più sensibile a modificazioni a carico dell’estremità amino-terminale, rispetto a quelle dell’estremità carbossi-terminale della molecola. I peptidi natriuretici potrebbero derivare tutti da un gene comune ancestrale, che era molto più simile al CNP che all’ANP ed al BNP. Il fatto che i peptidi natriuretici siano stati conservati nel corso dell’evoluzione e che il gene codificante si sia duplicato più volte, generando una famiglia di
iso-10
ormoni correlati dal punto di vista conformazionale, indica che essi sono necessari per la vita ed anche che possano svolgere (od abbiano svolto) differenti funzioni. È stata dimostrata la presenza di alcuni peptidi natriuretici non solo negli organismi eucarioti, sia del regno animale, che vegetale, ma anche in alcuni organismi unicellulari.
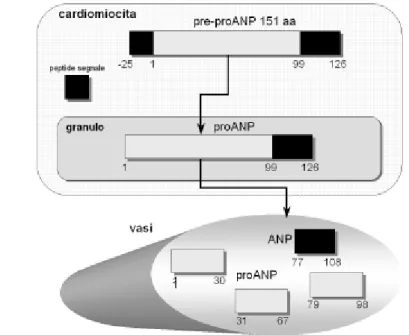
Nel genoma umano è conosciuta la localizzazione dei geni che codificano i precursori dell’ANP e del BNP (cromosoma 1) e del CNP (cromosoma 2). Dalla trascrizione del gene codificante l’ANP origina una molecola di RNA messaggero della dimensione di 1 chilobasi, su cui viene sintetizzato un peptide precursore (pro-ANP) costituito da 126 aminoacidi. Nell’uomo il pro-peptide subisce una scissione proteolitica in due frammenti: uno,
amino-terminale, di 98 aminoacidi ed un frammento carbossi-terminale di 28 aminoacidi che rappresenta la molecola biologicamente attiva (11-13) (Figura A).
11
Figura A: Sintesi e secrezione dell’ANP. Da un precursore preproANP
viene eliminata una sequenza segnale di 25 aminoacidi e la molecola di proANP che ne deriva si accumula in granuli di secrezione. In conseguenza alla stimolazione la molecola di proANP è scissa in un frammento carbossi-terminale (ANP, molecola attiva) ed una porzione aminocarbossi-terminale (Nt-proANP) che successivamente viene ulteriormente degradata.
Il BNP è immagazzinato come pro-ormone con una catena di 108 aminoacidi (pro-BNP) che al momento del rilascio è scisso enzimaticamente in un frammento inattivo amino-terminale di 76 aminoacidi e nella forma attiva, peptide carbossi-terminale, di 32 aminoacidi (Figura B).
12
Figura B: Sintesi e secrezione del BNP; Da un precursore preproBNP viene
eliminata una sequenza segnale di 26 aminoacidi. In conseguenza alla stimolazione la molecola di proBNP è scissa in un frammento carbossi-terminale (BNP, molecola attiva) ed una porzione aminocarbossi-terminale (Nt-proBNP).
Sia l’ANP che il BNP sono sintetizzati prevalentemente a livello dei cardiomiociti, il primo in prevalenza a livello degli atrii ed il secondo a livello dei ventricoli; questa caratteristica permette di attribuire ai livelli di concentrazione plasmatici di questi parametri una significativa cardiospecificità.
L’urodilatina è costituita da una molecola di ANP alla cui estremità amino-terminale sono aggiunti quattro aminoacidi e, sia l’ANP che l’urodilatina, derivano dallo stesso precursore costituito da 126 aminoacidi. Questo
13
peptide è sintetizzato nelle cellule tubulari del rene e viene secreto direttamente nel lume, infatti l’urodilatina è riscontrabile solo nelle urine e non risulta presente in circolo.
Regolazione della produzione e secrezione
I peptidi ANP e BNP sono entrambi sintetizzati e secreti, sia a livello dell’atrio, che del ventricolo, anche se in modo quantitativo differente: l’ANP prevale a livello dell’atrio, mentre il BNP nel ventricolo. Considerando la differenza di massa tra atrio e ventricolo è facilmente comprensibile la ragione per cui, in risposta ad uno stimolo, la quantità di molecole di BNP immesse in circolo è molto superiore a quelle di ANP. Nella secrezione di ANP e BNP è stata riscontrata una differenza sostanziale in quanto per l’ANP la secrezione sembra essere collegata al rilascio del pro-ormone da granuli di accumulo, evidenziabili con la microscopia elettronica a livello dei cardiomiociti atriali, mentre per il BNP la regolazione sembra localizzata a livello dell’espressione genica. La secrezione dei peptidi natriuretici è principalmente stimolata dalla distensione delle pareti, quindi situazioni in cui vi è un aumento del ritorno venoso, per esempio l’attività fisica o le variazioni di postura che determinano un incremento del volume atriale, determinano una secrezione prevalente di ANP. Al contrario, lo stimolo trascrizionale principale per la sintesi dei PN di tipo B, in particolare, è rappresentato dallo stress parietale in presenza di sovraccarico volumetrico e/o pressorio in stretta correlazione
14
con la dimensione della camera ventricolare sinistra e la pressione telediastolica. Altri stimoli riconosciuti risultano l’ipossia, il danno ischemico, l’endotelina-1, l’angiotensina II e l’IL-1. Sia il sistema neuro-ormonale che il sistema immunitario intervengono, attraverso un complesso meccanismo di interazioni, nella regolazione della sintesi e rilascio dei peptidi natriuretici. I principali fattori (Tabella II) che agiscono sul sistema dei peptidi natriuretici cardiaci come stimolatori sono: la noradrenalina, l’endotelina, l’angiotensina II, i glucorticoidi, gli estrogeni, gli ormoni tiroidei, alcuni fattori di crescita, ed anche alcune citochine (come il α Tumor Necrosis Factor, l’IL-1 e IL-6).
Tabella II. Sostanze che inducono sintesi e/o secrezione dei peptidi
natriuretici
Angiotensina II
Endoteline
Simpaticomimetici (alfa-adrenergici)
Citochine (IL-1, IL-6, TNF)
Fattori di crescita e/o della coagulazione
Insulina
Ormoni tiroidei
Corticosteroidi
15
D’altra parte, il sistema dei peptidi natriuretici cardiaci svolge un’azione inibente sul sistema neuroendocrino ed immunitario. Molti autori hanno dimostrato che il sistema dei peptidi natriuretici cardiaci, oltre a svolgere una potente azione diuretica, natriuretica, vasodilatatrice e controregolatrice nei confronti del sistema neuro-ormonale, possiede anche un’azione che contrasta i fenomeni del rimodellamento ventricolare e vascolare, compresa la ri-stenosi post-angioplastica.
Un sistema di relazioni intercorre tra il sistema neuro-endocrino ed i peptidi natriuretici, che quindi hanno un ruolo fondamentale non solo nel regolare l’omeostasi cardiovascolare (ANP e BNP) ma, associati all’azione paracrina dell’urodilatina (14), concorrono nella regolazione del tono della muscolatura liscia dei vasi, del bilancio elettrolitico e della morfologia del miocardio.
Meccanismo d’azione dei peptidi natriuretici
L’attività biologica dei peptidi natriuretici è mediata da specifici recettori di membrana: NPR-A e NPR-B che sono attivati selettivamente da ANP e BNP.
I recettori di tipo A e B hanno una struttura molto simile, si riscontra circa il 44% di omologia nel dominio di legame extracellulare, entrambi sono presenti nelle cellule renali e del surrene ma il recettore di tipo A si riscontra prevalentemente nei grossi vasi mentre il recettore di tipo B è più diffuso a livello del sistema nervoso centrale. Le funzioni biologiche innescate da
16
questi recettori sono mediate da un sistema di trasmissione del segnale a cascata che coinvolge molecole di guanil-monofosfato ciclico (cGMP). Entrambi i recettori, in seguito al legame con i peptidi natriuretici con il loro dominio extracellulare, sono rapidamente inattivati attraverso un processo di defosforilazione.
Sono i recettori di peptidi natriuretici maggiormente diffusi e sono presenti in molti tessuti tra cui l’endotelio vascolare, la muscolatura liscia, il cuore, il surrene ed il rene.
Quando ANP e BNP si legano a questi recettori, sono internalizzati e degradati enzimaticamente, quindi il recettore torna sulla superficie cellulare. Oltre a questo meccanismo, la rimozione dei peptidi natriuretici dal circolo è ottenuta tramite una degradazione enzimatica ad opera di una endopeptidasi neutra (una zinco metallo peptidasi) che è molto diffusa sulla membrana delle cellule di molti tessuti.
Azioni dei peptidi natriuretici
ANP e BNP, agendo tramite gli stessi recettori, producono effetti biologici simili: provocano natriuresi, diuresi, vasodilatazione, inibizione della sintesi dell’aldosterone ed hanno un effetto anti-mitogenico sulle cellule dell’endotelio e della muscolatura liscia.
L’effetto ipotensivo di questi peptidi è dovuta anche ad un’azione a livello centrale, dove inibiscono la secrezione di ADH e ACTH ed hanno un effetto simpatolitico.
17
La concentrazione dei peptidi natriuretici aumenta costantemente con l’età, in modo particolare dopo i 50 anni, sia nelle donne, che negli uomini. Questa tendenza all’aumento potrebbe rispecchiare un adattamento conseguente alle modifiche che si riscontrano, anche in soggetti non portatori di patologie, nel muscolo cardiaco e nell’emodinamica cardiovascolare con l’aumentare dell’età.
La sintesi e la secrezione dei peptidi cardiaci sono stimolate sia da fattori emodinamici che da meccanismi neuro-ormonali.
La valutazione della concentrazione delle molecole ad azione ormonale ed i relativi pro-ormoni può essere di notevole utilità nella valutazione clinica della funzione cardiaca: l’ANP riflette maggiormente le patologiche cardiache che inducono lo stiramento della parete striale, mentre il BNP, o il peptide NT-proBNP, evidenzia le alterazioni delle pareti ventricolari.
I peptidi natriuretici possono essere, quindi, considerati degli indicatori della funzionalità cardiaca e possono contribuire nella formulazione della diagnosi, ma anche nella valutazione dell’efficacia dei trattamenti terapeutici.
I peptidi natriuretici di tipo B (BNP e NT-proBNP) sono generalmente considerati utili per la valutazione diagnostica dei pazienti con dispnea acuta ed anche per confermare o escludere, grazie al loro elevato potere predittivo negativo, la diagnosi di IC. Il loro incremento è associato ad un aumento del rischio cardiovascolare.
18
Possono risultare utili come strumento di screening nei pazienti asintomatici e così anche nella stratificazione del rischio in tutto lo spettro dello scompenso clinico in stadio C-D.
Sono inoltre di grande utilità nella predizione delle modificazioni ecocardiografiche nel corso della storia clinica del paziente e nella predizione prognostica, anche in pazienti con funzione ventricolare lievemente ridotta.
Infine il valore prognostico del BNP e NT-proBNP, insieme alla constatazione che la terapia per IC modula le concentrazioni di questi biomarcatori, ha portato alla loro indagine come bersagli per la terapia dell’IC, con il concetto che la gestione dell’IC "guidata" dai valori dei peptidi natriuretici sarebbe superiore alla gestione di questa in loro assenza, con una conseguente significativa riduzione della mortalità (15-16).
Tabella III. Valori di cut-off per il peptide natriuretico cerebrale
(BNP) e per la porzione N-terminale del proBNP (NT-proBNP) nella diagnosi di IC acuta.
Improbabile Dubbio Alta probabilità BNP <100 100-400 >400 NT-proBNP <50 anni <300 300-450 >450 50-75 anni <300 300-900 >900 >75 anni <300 300-1800 >1800 I valori sono espressi in pg/ml.
19
ST2
Altro biomarcatore di stress cardiomiocitario, non ancora entrato nell’impiego clinico corrente, è ST2, membro della famiglia di recettori per l’interleuchina-1, che ha come ligando endogeno l’interleuchina-33, rilasciata a seguito dello stress miocitario e i cui livelli correlano con severità clinica e prognosi. Presenta una forma legata alla membrana (ST2-L) ed una forma solubile (sst2),la cui produzione è stimolata dalla deformazione miocardica. Il ligando funzionale per sst2 e ST2L è IL-33, che stimola effetti anti-ipertrofici, antifibrotici ed antiapoptotici. Gli effetti benefici di IL-33 sono mediati da ST2-L, che provoca resistenza all'apoptosi e riduzione della fibrosi. In contrasto, sst2, agisce come un recettore decoy, neutralizzando i vantaggi di IL-33.
Aumenti di sst2 possono essere osservati in proporzione alla gravità di IC, anche se, poiché tali aumenti non risultano universali, rendono sst2 meno adatto come strumento diagnostico per IC. In ogni caso è importante sottolineare come valori aumentati di sst2 siano biologicamente e clinicamente associati al rimodellamento ventricolare e possano essere utilizzati in maniera addizionale ai peptidi natriuretici e alla troponina per estrapolare un outcome prognostico (17-20).
20
Fattore di crescita e differenziazione 15
(GDF15)Recentemente, il fattore di crescita e differenziazione 15 (GDF-15) ha guadagnato interesse come biomarcatore nell’IC.
GDF-15 è solo debolmente espresso in circostanze fisiologiche, ma la sua espressione è significativamente aumentata in risposta all'infiammazione e al danno tissutale. Il suo aumento è stato osservato nel miocardio in IC e sovraccarico di pressione in modo analogo a quello del BNP. Poiché GDF-15 è anche up-regulated nell'ateroscelrosi, può essere meglio considerato come marker di malattia cardiovascolare, piuttosto che puramente cardiaco. Aumenta inoltre in alcuni tumori, in gravidanza ed anche in numerosi tessuti extracardiaci danneggiati. In ogni caso, nonostante non sia cardio-specifico, quando la causa della sua aumentata produzione è cardiaca, ha un valore maggiore rispetto ad altri marcatori come la proteina C-reattiva (PCR) (21-22).
21
DANNO MIOCITARIO ED APOPTOSI
Troponine
La necrosi dei miociti è prevalente nell’IC e può derivare da ischemia tissutale correlata a malattia coronarica così come da una iperstimolazione neurormonale, infiammazione ed apoptosi.
I cardiomiociti danneggiati, in modo reversibile o non, rilasciano le proteine intracellulari, meccanismo che costituisce la premessa per una valutazione quantitativa del danno cardiaco mediante il dosaggio di queste molecole circolanti.
Le troponine cardiache sono proteine che regolano l’interazione fra actina e miosina durante la contrazione muscolare e possono essere misurate nel sangue di soggetti in assenza dei tipici sintomi delle sindromi coronariche acute.
L'aumento dei marcatori di necrosi miocardica, quindi, in particolare le troponine (I e T), nell’IC sono un fenomeno comune, anche se ancora poco conosciuto. Inoltre le concentrazioni di troponina possono essere dinamiche: molti pazienti con bassi valori di troponina sviluppano successivamente, durante il follow-up, un aumento dei valori nonostantre l'assenza di sintomi, e questo correla con i più alti tassi di eventi cardiovascolari.
La concentrazione delle troponine cardiache circolanti aumenta con la gravità dell’IC. Il valore prognostico delle troponine cardiache è stato recentemente stabilito dallo studio Val-HeFT, che ha arruolato più di 5000 pazienti con IC cronica sintomatica lieve-moderata. Il rischio di eventi
22
clinici avversi (decesso o ricovero in ospedale per peggioramento dell’IC) aumentava progressivamente a partire da concentrazioni di troponina T circolante molto basse. Le troponine possono essere, inoltre, confrontate con i PN, che mostrano un valore prognostico elevato in pazienti con patologie cardiovascolari, a concentrazioni molto al di sotto delle soglie diagnostiche di esclusione dell’IC. La stratificazione prognostica della troponina T ad alta sensibilità è paragonabile a quella dei PN.
I meccanismi responsabili del rilascio di troponine dai cardiomiociti riflettono probabilmente un fenomeno continuo di morte cellulare per necrosi, morte per apoptosi, stiramento dei cardiomiociti (sovraccarico) e ischemia.
Ci sono però altre cause di innalzamento dei livelli circolanti delle troponine cardiache, come ad esempio patologie cardiopolmonari, insufficienza renale cronica, fenomeni di infiammazione o di attivazione di alcuni sistemi neuroendocrini, riscontrati nei pazienti affetti da IC.
Le troponine cardiache circolanti hanno dimostrato un valore prognostico molto elevato nell’IC; in ogni caso, il valore aggiunto rispetto ai PN, marcatori di riferimento nella prognosi, dovrà essere meglio definito.
In conclusione, il ruolo prognostico delle troponine, è stato osservato in aggiunta alla presenza di altri biomarcatori come BNP, st2 ecc.
Clinicamente la perdita dei cardiomiociti, che si riflette in un aumento della troponina, è associato ad un profilo clinico non compensato e, durante il follow-up, i pazienti con aumentati livelli di troponina hanno un maggior
23
rischio di andare incontro ad un rimodellamento ventricolare avverso. Quindi le troponine possono essere incluse nella lista dei biomarcatori associati a rimodellamento ventricolare e fibrosi (23-25).
24
INFIAMMAZIONE
Fattore di necrosi tumorale alfa (
TNF-alfa), suoi recettori
solubili (s
TNF-alfa
R1, s
TNF-alfa
R2),
CRP, IL-6e
PTX-3Negli ultimi trent’anni si sono accumulate molte evidenze sul ruolo dell’attivazione della risposta infiammatoria nella patogenesi di differenti tipi di cardiopatia, tra cui l’IC.
Le citochine comprendono una numerosa famiglia di proteine e sono sintetizzate e rilasciate da differenti tipi cellulari, mostrando proprietà autocrine o paracrine e solo in alcuni casi posseggono anche un’azione simil-endocrina, in quanto possono anche essere trasportate dal torrente sanguigno e così raggiungere recettori specifici in tessuti periferici. Hanno, inoltre, azioni biologiche pleiotropiche, in quanto agiscono su differenti tipologie di tessuti o cellule.
In generale le citochine si differenziano in due gruppi a seconda che mostrino proprieta pro-infiammatorie od antiinfiammatorie (Tab. IV).
25
Tabella IV Agenti citochine-simili con attivita pro-infiammatoria o
antiinfiammatoria che sono stati descritti essere aumentati in pazienti con IC. Attività pro-infiammatoria • TNF-α • sTNFR1 • sTNFR2 • sFas • CD40L • TRAIL • Activina A • Mieloperossidasi • Pentrassina-3 • RANTES • CRP • IL-6 • Cardiotrofina-1 • IL-8 • MCP-1 • MIP-1a Attività anti-infiammatoria • IL-10 • IL-13 • IL-18
Entrambi gli effetti
• Adiponectina • Resistina
La risposta delle citochine pro-infiammatorie è regolata dalle citochine anti-infiammatorie, che agiscono dunque come agenti immuno-modulatori (26-27).
26
uno studio nel 1956, ha mostrato come le concentrazioni di CRP (proteina C reattiva) sono aumentate in pazienti con IC cronica e che le concentrazioni assolute erano indicative della gravità della malattia. CRP media diversi processi di protezione, ma può anche avere effetti deleteri in IC, come la sovraregolazione del fattore di necrosi tumorale alfa (TNFalfa) e IL-6. Sebbene studi recenti abbiano confermato un ruolo prognostico per CRP nell’IC, potrebbe essere meno adatto come biomarcatore per IC causa del suo ruolo promiscuo nei processi infiammatori e per la mancanza di un imperativo terapeutico associato con il suo aumento. Inoltre, CRP può perdere significato prognostico nei modelli che esaminano biomarcatori multipli (28).
Le più importanti citochine con proprietà pro-infiammatoria sono il fattore di necrosi tumorale (Tumor Necrosis Factor, TNF), e le citochine 6 e IL-1, mentre quelle con proprietà modulatrice (anti-ifiammatoria) sono le citochine IL-1ra (Interleukin-1 receptor antagonist), IL-10, IL-11, e
IL-13 (30-32).
TNF-alfa contribuisce alla progressione dell'insufficienza cardiaca attraverso diversi meccanismi che modulano le proteine esistenti, ad esempio attraverso la stimolazione dello stress ossidativo, e diminuisce anche la contrattilità cardiaca attraverso sottoregolazione di proteine del reticolo sarcoplasmatico quali la catena pesante dell'alfa-miosina. La misurazione del TNF-alfa predice lo sviluppo di IC in individui asintomatici, nonché la progressione di malattia, soprattutto nel sesso
27
maschile. Purtroppo la terapia specifica anti-TNFalfa non ha portato ad un migliore outcome nei pz con scompenso cardiaco.
IL-6 colpisce direttamente la comunicazione cellula-cellula tra i miociti cardiaci e i fibroblasti, e le alterazioni nella concentrazione di IL-6 sono associati con disfunzione cardiaca ed alterazione della matrice extracellulare cardiaca. A causa di queste caratteristiche, IL-6 è talvolta discusso come biomarker "rimodellamento", molto simile a sst2 o troponina. Il valore predittivo di IL-6 per l'outcome prognostico nell’IC può essere indipendente da altri biomarcatori di infiammazione, ma IL-6 manca anche di specificità diagnostica (32).
Un biomarker infiammatorio promettente è pentraxina-3 (PTX3), che sembra giocar un ruolo cardioprotettivo in IC. Studi in letteratura hanno dimostrato che le concentrazioni di PTX3 sono aumentate in pz con IC con frazione di eiezione preservata, e il campionamento dal seno coronarico mostra che la sua produzione avviene nel miocardio (29).
Da recenti studi è stato visto come l’insufficienza cardiaca cronica non possa più essere considerata una malattia dovuta solamente ad una disfunzione della attività cardiaca, ma piuttosto una sindrome clinica caratterizzata da una alterata funzionalità di praticamente tutti gli organi e sistemi del nostro organismo, compresi il sistema neuro-ormonale, il sistema escretore renale, la funzionalità epatica, il sistema locomotore muscolo-scheletrico, ed anche il sistema immuno-competente (40). Le citochine sono implicate sia nello sviluppo che nella progressione dell’IC
28
cronica. E’ stato, infatti, dimostrato che le citochine pro-infiammatorie sono attivate fin dalle prime fasi della insufficienza cardiaca. La causa principale di questo meccanismo sembra essere l’attivazione del sistema neuro-ormonale, soprattutto dai sistemi simpatico e renina-angiotensina, la cui azione è considerata attualmente il principale meccanismo di progressione della disfunzione cardiaca, così come dello squilibrio emodinamico e del bilancio dei fluidi ed elettroliti (Fig. C).
29
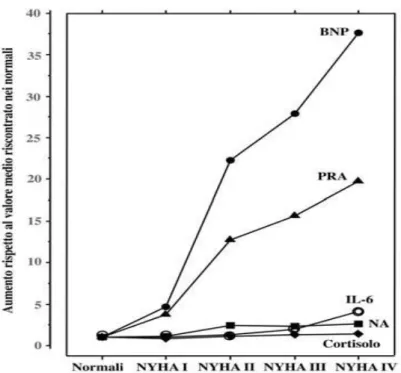
Figura C. Livelli circolanti di differenti indici di attivazione del sistema
neurormonale e della citochina IL-6.
I parametri sono riferiti a soggetti adulti sani e pazienti con differenti gradi di scompenso cardiaco (in ascissa), secondo la classe funzionale NYHA (New York Heart Association). I valori in ordinata sono espressi come aumenti rispetto al valore medio trovato nei soggetti sani.
In particolare, i dati riportati in figura indicano che i livelli circolanti di IL-6 aumentano mediamente di circa 2,5 volte nei soggetti con scompenso cardiaco rispetto ai valori riscontrati nei soggetti normale, risultando gia elevati nei pazienti in classe NYHA II, cioe nelle prime fasi della malattia. I dati riportati nella figura indicano inoltre che i livelli di IL-6 aumentano rispetto al valore medio dei soggetti normali piu di quelli del cortisolo e della NA, ma meno della PRA (indice di attivazione del sistema renina-angiontensina) e del BNP.
L’insufficienza cardiaca cronica è caratterizzata da una risposta infiammatoria che correla con la severità della malattia e con la prognosi. Il legame fra l’IC e la risposta infiammatoria è stato messo in evidenza nel 1990 dallo studio di Levine e collaboratori (30), che indicarono in modo
30
chiaro che nel paziente con IC grave i livelli circolanti di fattore di necrosi tumorale (TNF) erano molto elevati rispetto alla norma. Dopo questo primo studio, moltissimi altri Autori hanno confermato il coinvolgimento non solo del TNF, ma anche di altre citochine pro-infiammatorie e chemochine nella progressione dell’IC. Ulteriore sostegno all’eziologia infiammatoria dell’IC è venuto dalla dimostrazione che le citochine infiammatorie possono essere prodotte anche dai cardiomiociti, a seguito di stimoli ischemici o meccanici. Non solo le citochine, ma anche la risposta immunitaria innata, rappresentata da recettori Toll-like, pentraxine, come la proteina C-reattiva e la pentraxina 3, è stata trovata anormale nel paziente scompensato (28-29). Nel complesso queste evidenze suggeriscono che nell’IC esiste una condizione di alterata attivazione non solo infiammatoria, ma anche immunitaria.
Numerosi studi hanno dimostrato che i livelli circolanti delle citochine TNF, IL-6, IL-1 e IL-18 sono elevati nei pazienti con insufficienza cardiaca e che le citochine pro-infiammatorie sono attivate anche nei pazienti con disfunzione ventricolare ancora asintomatica. Livelli aumentati delle citochine si riscontrano quindi nelle prime fasi dello scompenso cardiaco (come nei pazienti in classe funzionale NYHA II) e questi livelli tendono ad aumentare progressivamente con l’aggravarsi delle condizioni del paziente, qualunque sia la causa primitiva di insufficienza cardiaca.
Nei pazienti con insufficienza cardiaca, si riscontrano livelli circolanti progressivamente aumentati, in accordo con la severità di malattia, oltre che
31
delle citochine pro-infiammatorie, anche della parte solubile dei loro recettori specifici. In particolare, si evidenzia nei tessuti e nei fluidi biologici un aumento della porzione solubile del recettore, che include solo la parte del recettore che si stacca dalla membrana citoplasmatica e che quindi ha perso le porzioni transmembrana ed intra-citoplasmatica della catena peptidica. Il recettore solubile possiede ancora l’estensione extra-cellulare del peptide originale che contiene il sito legante specifico. Per questa ragione, il recettore solubile è in grado di legare ad alta affinità la citochina (come il recettore completo), in questo modo inibendone l’attività pro-infiammatoria sia in vivo che in vitro.
In particolare, sono stati anche riscontrati livelli aumentati dei recettori solubili specifici del TNF (soluble TNF receptors: sTNF-R1 e sTNF-R2). E’ importante sottolineare che il miocardio non contiene normalmente TNF-α, ma esprime solo i due recettori. Per contro, nel miocardio scompensato si riscontra un’aumentata espressione della citochina ed una regolazione tramite inibizione (down-regulation) dei suoi recettori. I recettori solubili possono legare il TNF-α ad alta affinità (soprattutto il sTNFR1) e quindi modularne l’attività (33-35).
D’altra parte, nei pazienti con IC sono stati riscontrati livelli circolanti aumentati anche di citochine con azione prevalentemente anti-infiammatoria, come le citochine IL-10 e TGF-β1(Transforming Growth Factor) (35). Considerati tutti insieme, questi dati suggeriscono che nell’insufficienza cardiaca è presente una rete costituita da complesse
inter-32
relazioni fra agenti pro- ed anti-infiammatori e proteine solubili leganti le differenti citochine. La risposta complessiva del sistema delle citochine, quindi, è determinata dalla inter-relazione che si instaura di volta in volta per ogni specifica condizione clinica in ogni singolo paziente. Pertanto, tale risposta risulta assai variabile nel tempo, anche nello stesso paziente.
Oltre che presentare una associazione stretta con la severità di malattia, i livelli circolanti delle citochine pro-infiammatorie correlano positivamente con la mortalità nei pazienti con insufficienza cardiaca cronica. Soprattutto i livelli circolanti di TNF-α, IL-6 e dei recettori solubili del TNF-α (sTNFR1 e sTNFR2) sono in grado di predire un aumento significativo di mortalità nei pazienti con insufficienza cardiaca. La maggior parte degli autori ha studiato pazienti con IC conclamata, ma uno studio più recente, basato su una larga popolazione di soggetti esaminati ha riportato come aumentati livelli di TNF sono indipendentemente associati con un più elevato rischio di mortalità anche in pazienti asintomatici e con frazione di eiezione del ventricolo sinistro non compromessa (≥ 50%).
Questi studi di correlazione non possono di per sé dimostrare una effettiva relazione di causa-effetto tra gli aumentati livelli di citochine, la progressione dell’IC e l’aumento della mortalità in pazienti con IC, ma soltanto suggerire questa relazione. Inoltre, in questi studi, i valori di sensibilità, specificità e valori predittivi delle citochine, in quanto possibili biomarcatori indicatori di prognosi in pazienti con IC, non sono stati ancora ben determinati. Ancora, non è ben conosciuto l’apporto che questi
33
biomarcatori infiammatori possono fornire in aggiunta ad altri biomarcatori (analisi multimarkers), il cui valore predittivo nei pazienti con IC è ormai stato ben accertato come il BNP o le troponine cardiache.
Studi più recenti hanno dimostrano che i pazienti che rispondono al trattamento con una riduzione significativa dei livelli circolanti di biomarcatori di attivazione neuro-ormonale hanno una prognosi migliore rispetto ai pazienti che non rispondono al trattamento senza una diminuzione significativa di tali livelli. Un intenso programma di attività fisica è in grado di ridurre sia i livelli di alcune citochine pro-infiammatorie ed i loro recettori solubili (come TNF-α, IL-6, sTNFR1, sTNFR2, e sIL-6R), sia svariati indici di attivazione neuro-ormonale. Anche in questo caso, l’attività fisica, che è in grado di migliorare da una parte il benessere (fitness) cardio-respiratorio e dall’altra di ridurre i livelli circolanti di citochine e/o neuro-ormoni, migliora nel contempo anche la sopravvivenza dei pazienti. Infine, in pazienti con IC in stadio avanzato (classe funzionale NYHA III o IV) l’assistenza meccanica per alcune settimane con pompe che aiutano l’eiezione del sangue dal ventricolo sinistro (ventricular assist device) è in grado di ridurre l’espressione miocardica di TNF-α.
Questi dati indicano che è presente una stretta inter-relazione fra i vari sistemi regolatori del nostro organismo, che sono tutti insieme attivati nell’IC e sono in grado di essere, sempre insieme, influenzati dal trattamento terapeutico. Su questa evidenza sperimentale si fonda, quindi, il
34
concetto di biomarcatore in grado di guidare e graduare il trattamento nel singolo paziente a seconda della risposta alla terapia (36-39).
35
STRESS OSSIDATIVO
Mieloperossidasi
(MPO)L'aumento dello stress ossidativo e il conseguente disequilibrio tra agenti ossidanti e meccanismi endogeni antiossidanti di protezione, può diminuire, attraverso meccanismi di necrosi ed apoptosi, direttamente la funzionalità miocardica.
Questa riduzione può avvenire attraverso effetti nocivi sulla funzione endoteliale, dalla attivazione del sistema renina-angiotensina-aldosterone e del sistema nervoso simpatico, o tramite incremento dell'infiammazione. Il biomarcatore più interessante di stress ossidativo è la mieloperossidasi (MPO). MPO è un enzima che viene rilasciato da neutrofili e leucociti attivati, e catalizza la formazione di specie reattive dell'ossigeno, radicali liberi e ossido nitrico derivati, che favoriscono i danni ai tessuti. Studi hanno mostrato come i pazienti con IC acuta con concentrazioni di MPO >99 pmol/L hanno un tasso di mortalità ad 1 anno superiore. Un altro studio ha suggerito che MPO predice lo sviluppo di IC in 7 anni in individui con fascia di età tra 65 e 75 anni, soprattutto in quelli senza una storia di fattori di rischio tradizionali per IC (41-42) (Tab. V).
36
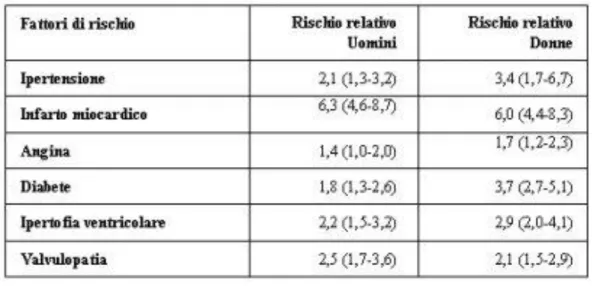
Tabella V. L'ipertensione è il fattore di rischio più importante per lo
sviluppo di insufficienza cardiaca. Numerosi studi documentano che circa 2/3 dei pazienti con insufficienza (IC) hanno sofferto di ipertensione. Framingham ha dimostrato che i maschi ipertesi avevano il doppio del rischio di sviluppare insufficienza, e che le donne ipertese avevano un rischio 3 volte più elevato.
37
BIOMARCATORI DI RIMODELLAMENTO DELLA MATRICE EXTRACELLULARE VENTRICOLARE
Metalloproteinasi della matrice extracellulare (
MMPs) e
inibitori tissutali delle metalloproteinasi (
TIMPs)
La matrice extracellulare del miocardio è composta soprattutto da una complessa rete di fibrille di collagene, che offre sia un supporto fisico per l’organizzazione spaziale delle cellule in tessuti funzionali, sia un microambiente dinamico per lo scambio di segnali fra le cellule (43).
Il rimodellamento ventricolare con modificazione di forma, dimensione e funzione del cuore inizialmente in termini di ipertrofia compensatoria, si rivela maladattativo conducendo ad ipertrofia decompensata, disfunzione contrattile ed, infine, IC. Tale fenomeno di rimodellamento prefigura l’ipertrofia miocitaria, la proliferazione dei fibroblasti, l’alterazione dell’espressione e della distribuzione sia delle componenti intracellulari, che delle più importanti proteine strutturali della matrice extracellulare. In condizioni normali, abbiamo una perfetta omeostasi nell’azione di metalloproteinasi della matrice (MMP) (enzimi proteolitici che degradano il collagene fibrillare) e dei loro inibitori tissutali (TIMP). Il passaggio da un’ipertrofia compensatoria ad una dilatazione francamente patologica è uno dei momenti più importanti nella storia naturale dell’IC. La distruzione diretta della matrice extracellulare da parte delle MMP è correlata con la dilatazione ventricolare e con la conseguente disfunzione; inoltre ne segue parallelamente il decorso temporale.
38
Nel Framingham Heart Study, in pazienti sani fu dimostrato come aumentati livelli plasmatici di MMP-9 fossero associati ad un rischio raddoppiato di rimodellamento patologico.
La matrice extracellulare del cuore è, quindi, sempre più riconosciuta per essere importante nella fisiopatologia della progressione dell’insufficienza cardiaca. Il deleterio rimodellamento della matrice extracellulare è un processo importante, che si svolge attraverso la degradazione del collagene e di altre proteine della matrice ad opera di collagenasi, metalloproteinasi (MMP) e inibitori tissutali delle metalloproteinasi (TIMP). La misurazione dei prodotti di degradazione del collagene fornisce una finestra delle attività di scomposizione degli elementi della matrice extracellulare. Le concentrazioni sia del pro-peptide terminale, sia del telo-peptide C-terminale del collagene di tipo I, così come anche il peptide N-C-terminale del pro-collagene di tipo III possono identificare la presenza di fibrosi nell’IC (43-45).
Le proteine coinvolte nella degradazione della matrice, ovvero MMP e TIMP, possono essere altrettanto utili per la valutazione dei pazienti con insufficienza cardiaca. Sono stati descritti almeno 25 tipi di metalloproteinasi ed in particolare MMP2, MMP3 ed MMP9 sembrano giocare il ruolo più importante per lo sviluppo dell’IC. Anche se un aumento delle concentrazioni di MMP3 e MMP9 sono associate a tassi di mortalità più elevati nei pazienti con insufficienza cardiaca dovuta a disfunzione sistolica ventricolare sinistra, MMP9 è risultata essere un indicatore
39
prognostico del tutto indipendente. Al contrario, altri studi hanno mostrato come, in pazienti con insufficienza cardiaca cronica, sia in realtà TIMP1, ma non MMP9, a fornire un più adeguato outcome prognostico in termini di mortalità.
Inoltre, MMP-8 e MMP-9, possono essere sintetizzate da cellule infiammatorie sotto lo stimolo di citochine come il TNF-alfa.
Il TNF-alfa mostra un’azione bifasica, che si esplica mediante uno sbilanciamento dei meccanismi contrastanti che possono indurre da una parte la sintesi della matrice extracellulare e dall’altra la sua degradazione. Questo effetto bifasico è influenzato dalla durata dell’esposizione ed è, quindi, tempo-dipendente. Nel breve periodo, il TNF-alfa induce un’attivazione delle MMPs che porta ad una aumento della degradazione della matrice extracellulare e che promuove, a sua volta, la progressiva dilatazione ventricolare.
Una stimolazione più prolungata produce, invece, un’eccessiva deposizione di collagene con un aumento dello spessore del ventricolo sinistro. Questo effetto è dovuto sia ad un’azione diretta della citochina, sia ad una sua azione indiretta, che risulta mediata dall’attivazione del sistema renina-angiotensina e del fattore tissutale TGF-β. In particolare, un aumento (up-regulation) dei recettori specifici di tipo 1 (AT1) dell’angiotensina induce un più elevato stato di attivazione del sistema renina-angiotensina che è responsabile, a sua volta, dell’aumentata sintesi di collagene, che porta alla fibrosi miocardica.
40
Infine, un ruolo chiave in questo meccanismo patogenetico è anche svolto dai fattori di trascrizione NF-κB e AP-1 (Activator Protein-1), che sembrano modulare l’espressione a livello di trascrizione genica di molte MMPs, come anche di TIMP-1 e -2.
Altra molecola di interesse è Galectin-3 (Gal-3) (46), individuata essere un importante legame tra infiammazione e fibrosi ed è secreta da macrofagi attivati. E' stato, inoltre, osservato in vitro come Gal-3 stimoli la proliferazione e la produzione di collagene da parte dei fibroblasti cardiaci e come le sue concentrazioni correlino con quelle di MMP2 e TIMP. Infine, Gal-3 risulta essere aumentata in pazienti con IC e, sebbene il suo ruolo diagnostico in IC abbia un valore limitato rispetto a quello dei peptidi natriuretici, Gal-3 è un ragionevole predittore prognostico.
41
ALTRI MARCATORI NEURORMONALI
L’iperattivazione del sistema adrenergico rappresenta uno dei meccanismi più importanti e precoci di risposta ad una diminuita performance cardiaca con concomitante decremento del tono parasimpatico-vagale. Per la prima volta all’inizio degli anni ’60 fu riportata una correlazione tra classi NYHA e livelli plasmatici di noradrenalina. Nel 1984 Cohn et al. (47) dimostrarono come la noradrenalina plasmatica fosse un indicatore prognostico indipendente di mortalità. Pochi studi hanno evidenziato il ruolo dell’attività reninica plasmatica in popolazioni di pazienti in stadio C, anche sotto trattamento ottimale, seppure questo ambito sia di estremo interesse
L'endotelina-1 (ET-1)è prodotta dall'endotelio in risposta all'angiotensina II, a mediatori infiammatori e allo shear stress vascolare ed è responsabile di vasocostrizione, attivazione di specie reattive dell'ossigeno e rimodellamento ventricolare.
Recentemente Tang e al. (48) hanno recentemente confermato che le concentrazioni di ET-1 sono associate con parametri di disfunzione diastolica ad alla prognosi nell’IC dovuta a disfunzione ventricolare sinistra sistolica.
La arginina vasopressina (AVP) (49) è un ormone antidiuretico e vasocostrittore che viene rilasciato dall'ipotalamo in risposta ai cambiamenti di osmolarità plasmatica ed ipovolemia. La produzione di AVP risulta essere sovraregolata nei pazienti con IC e gioca un ruolo nel comportare
42
iponatriemia, fattore prognosticamente significativo nei pazienti con IC.
Le emergenti applicazioni in ambito clinico di biomarcatori stabiliti sono promettenti e potranno modificare l'impatto gestionale e terapeutico dei pazienti con scompenso cardiaco, personalizzando in maniera sempre più ottimale la cura.
43
BIOMARKERS:
CONFRONTO
DEL
VALORE
PROGNOSTICO
Metalloproteinasi della matrice extracellulare e peptidi
natriuretici
I livelli di peptide natriuretico così come del peptide natriuretico N-terminale protipo-B (NT-proBNP), correlano con informazioni prognostiche circa la morbilità e la mortalità dei pazienti con IC, e sono divenuti punti chiave nella gestione e terapia dell’IC. Ulteriori informazioni, riguardo la stratificazione del rischio dei pazienti con IC, però, nonostante pareri discordanti, potrebbero essere aggiunte da altri biomarcatori come le metalloproteinasi della matrice extracellulare. Confrontando il valore prognostico in IC, secondario a disfunzione sistolica, dei livelli di MMP-3 e MMP-9 con NT-proBNP ed aggiungendo la valutazione ecocardiografica è stato osservato che i parametri clinici, biochimici e Doppler ecocardiografici sono indicatori univariati di eventi in pazienti con IC sistolica e con un'elevata prevalenza di malattia coronarica. Tra i biomarcatori cardiaci, la MMP-9, ma non NT-proBNP, è emerso essere un potente indicatore indipendente dell'outcome prognostico. Il rimodellamento del ventricolo sinistro è il fattore chiave nello scompenso cardiaco ed è direttamente connesso al futuro deterioramento della performance ventricolare sinistra ed ad un outcome meno favorevole. Per questo il rimodellamento del ventricolo sinistro può contribuire alla
44
progressione della malattia indipendentemente dallo stato neurormonale del paziente.
Diversi studi hanno mostrato l'importanza delle MMPs nello sviluppo e progressione dell’insufficienza cardiaca. Infatti, elevati livelli circolanti di MMP-9 sono stati associati con una maggiore compromissione della funzione del ventricolo sinistro e in avanzato processo di rimodellamento sui pazienti con pregresso infarto del miocardio. Dobbiamo, però, rilevare che mentre alcuni studi mostrano un valore prognostico indipendente delle MMPs nello stratificare il rischio di pazienti con IC, altri non mostrano alcun contributo rilevante da parte di questi enzimi proteolitici nel predire l'outcome prognostico di tali pazienti.
E’ stato visto, comunque, che la MMP-9, la MMP-3 e NT-proBNP hanno predetto l’outcome dei pazienti con insufficienza cardiaca, ma che MMP-9 è l'unico biomarcatore con valore prognostico indipendente, soprattutto qualora la causa dell’IC sia di natura ischemica. Quindi, l'importante valore prognostico della MMP-9 in pazienti con IC con elevata prevalenza di malattia coronarica è una probabile implicazione del ruolo svolto da questi biomarcatori nel processo di rimodellamento e disfunzione nella malattia ischemica cardiaca.
Concludendo, sebbene NT-proBNP sia il comune marcatore prognostico utilizzato nella pratica clinica, assieme alla valutazione dei parametri ecocardiografici e Doppler della funzione sistolica e diastolica, nello stratificare il rischio dei pazienti con IC sistolica, sembra che altri
45
biomarcatori, come le MMPs, siano atrettanto, se non più, importanti per il follow-up di tali pazienti, in particolare di quelli con elevata prevalenza di malattia coronarica (50).
ST-2 e Galectin-3
Recenti biomarkers quali ST2 e Gal-3, sono stati confrontati nella stratificazione del rischio a lungo termine nei pazienti con IC. ST2 e Gal-3 sono, infatti, promettenti biomarcatori di fibrosi miocardica e rimodellamento in IC. Lo studio di Bayes-Genis et al., includeva 876 pazienti di età media 70 anni e frazione di eiezione ventricolare sinistra media del 34% e prendeva come endpoints tutte le cause di mortalità a 5 anni e eventuali ospedalizzazioni per IC. Durante un follow-up della durata media di due anni, 392 pazienti sono deceduti. Il confronto fra questi due biomarcatori nell’IC cronico ha mostrato la superiorità di ST2 su Gal-3 nella stratificazione del rischio. Il contributo aggiuntivo di Gal-3 si è mostrato irrilevante (51).
46
Fattore di necrosi tumorale alfa (TNF-alfa), suoi recettori solubili (sTNFR1 e 2) e metalloproteinasi della matrice extracellulare
Recenti studi clinici e sperimentali indicano che la up regulation del sistema del TNF può contribuire alla progressione del rimodellamento cardiaco e dell’IC, promuovendo alterazioni nella biologia dei cardiomiociti e nel metabolismo della matrice extracellulare. Aumentati livelli di TNF-alfa in pazienti con IC si sono mostrati statisticamente significativi nella stratificazione della prognosi. Assente nel miocardio normale e prodotto nel miocardio come risposta ad un sovraccarico di volume, TNF-alfa può deprimere la funzione cardiaca direttamente ed indirettamente mediante l’induzione della ossido nitrico sintetasi prodotta dai macrofagi, dai miociti cardiaci e da altre cellule. La maggior parte degli effetti del TNF-alfa sono svolti da due recettori presenti sulla superficie di varie cellule, i cui domini extracellulari, staccandosi dalla superficie, possono essere misurati come forme solubili (sTNFR1 e 2) sia nel sangue, che nelle urine e risultano aumentati in pazienti con IC.
Il turnover della matrice extracellulare è regolato dalle metalloproteinasi della matrice (MMPs), che sono enzimi endogeni responsabili della degradazione del collagene extracellulare.
Studi hanno valutato la fluttuazione dei livelli sierici di TNF-alfa e dei suoi recettori solubili di tipo 1 e 2 (sTNFR1 e 2) in pazienti con IC cronica sia durante la fase acuta, che durante periodo di stabilità clinica. Inoltre, è stata
47
valutata la relazione esistente tra i profili sierici di MMPs (MMP-1, MMP-2, MMP-3) e i livelli circolanti di TNF-alfa e dei suoi recettori solubili, ed è stato osservato come i sTNFR siano elevati sia nella fase acuta di malattia, che nella fase di stabilità. Sono stati riscontrati livelli più elevati di sTNFR2 durante la fase stabile di malattia, suggerendo come questo possa stabilizzare la citochina e quindi prolungare la sua emivita e le sue funzioni biologiche.
Infine, è stato osservato come il rimodellamento cardiaco, mediato dal sistema TNF, possa avvenire attraverso l’attivazione del pathway di segnalazione di MMP-3 (52-54).
48
RAZIONALE
DELL’UTILIZZO
COMBINATO
DI
BIOMARCATORI
E
PARAMETRI
ECOCARDIOGRAFICI
L’insufficienza cardiaca è ancora un problema di salute pubblica mondiale e, nonostante gli enormi progressi compiuti nella sua diagnosi e trattamento, è frequentemente associata ad una prognosi infausta. Evidentemente, i sintomi clinici da soli non sono una guida sufficientemente affidabile per il trattamento dell’IC, quindi, eventuali parametri in grado di identificare una prognosi sfavorevole sono utili per adattare i regimi terapeutici ai singoli pazienti.
Ecocardiografia e peptidi natriuretici (NP) hanno dimostrato le loro capacità nel dare informazioni indipendenti sia diagnostiche, che prognostiche per quanto riguarda i pazienti con insufficienza cardiaca. Anche se la sola alterazione ecocardiografica della funzione ventricolare sinistra, o quella di un NP, denotano un aumento del rischio di mortalità, il rischio maggiore deriva da anomalie compresenti della funzione ventricolare sinistra e dei livelli di NP.
L’insufficienza cardiaca rappresenta la principale causa di ricovero ospedaliero nella fascia di età sopra i 65 anni. L'ecocardiografia rappresenta la più utile indagine strumentale nella valutazione dei pazienti con IC. Gli indici ecocardiografici della struttura e funzione cardiaca sono, inoltre, affidabili indicatori prognostici di mortalità in pazienti con IC. Negli ultimi anni le tecniche ecocardiografiche applicabili ai pazienti con IC si sono rapidamente evolute. Nuove tecniche
49
come il Doppler tissutale ecocardiografico (TDI) sono state sviluppate per mostrare i meccanismi emodinamici e miocardici, che aiutino gli specialisti negli obiettivi diagnostici e prognostici. Sebbene gli indici Doppler convenzionali e i parametri TDI correlino con lo stato funzionale in pazienti con una significativa disfunzione ventricolare sinistra o IC avanzata, la valutazione combinata della velocità di flusso transmitralica all'ecocardiografia Doppler e delle velocità anulari mitraliche al TDI (E/Ea), che probabilmente riflette un'elevata pressione di riempimento ventricolare sinistro, si è dimostrata essere una dei migliori parametri ecocardiografici diagnostici e prognostici.
D'altra parte, nuovi biomarcatori plasmatici si sono mostrati essere importanti indicatori del rischio nei pazienti con insufficienza cardiaca. Tra questi, i peptidi natriuretici, in particolar modo il BNP e il suo frammento N-terminale (NT-proBNP), sono facilmente e routinariamente accessibili. Questi biomarcatori, aumentati in conseguenza di sovraccarichi di volume o pressione, sono strettamente associati con la presenza e la severità delle anomalie della struttura e funzione cardiovascolare. Inoltre, in pazienti sia con IC acuta che cronica, i livelli di NP sono tra i più potenti indicatori del rischio e la loro misurazione è utile per la stratificazione prognostica nell'ambito dell'intero spettro di gravità di malattia. Diversi studi hanno valutato il ruolo del NT-proBNP plasmatico e delle variabili Doppler ed ecocardiografiche per la stratificazione del rischio di pazienti stabilizzati dalla terapia medica.
50
Dokainish et al., hanno mostrato il valore predittivo aggiuntivo di BNP e Doppler ecocardiografico nella stratificazione della prognosi dei pazienti con IC cronica e con un ampio range di frazione di eiezione del ventricolo sinistro.
Altri studi hanno dimostrato che un tempo di decelerazione dell’onda E<150 ms, Doppler tissutale Em <8 cm/s e valori di NT-proBNP > 1129 pg/ml, sono risultati essere tutti fattori predittivi indipendenti di morte o di ospedalizzazione in pazienti con insufficienza cardiaca. Hanno anche fornito informazioni aggiuntive utili nella stratificazione del rischio di pazienti stabilizzati dalla terapia medica.
Sebbene sia BNP che NT-proBNP siano marcatori promettenti nell’IC ed entrambe le valutazioni siano affidabili dando buone performance analitiche, i valori del loro cut-off diagnostico è variabile e popolazione dipendente. Il più ampio range di rilevazione e la più stabile struttura di NT-proBNP rispetto a quella di BNP suggeriscono che NT-NT-proBNP potrebbe giocare un ruolo addizionale nella valutazione dei pazienti con disfunzione ventricolare sinistra, sebbene questo possa essere valutabile tenendo in mente fattori confondenti, come la funzione renale o l'obesità. D'altro canto, nei sopravvissuti ad IC acuta, i livelli di BNP si riducono più rapidamente rispetto a quelli di NT-proBNP, per cui questo potrebbe permettere una valutazione più precoce dell'efficacia del trattamento.
Dato il fatto che sia l'ecocardiografia che i valori di NP forniscono valutazioni aggiuntive sulla struttura e sulla funzione cardiaca, e che
51
entrambi sono importanti indicatori prognostici, indipendenti da altre variabili nei pazienti con IC acuta e cronica stabilizzata, sono entrambi parametri utili nella gestione dei pazienti con IC. Inoltre, esiste una significativa correlazione tra i livelli di NP circolanti e alcuni parametri ecocardiografici inerenti la funzione ventricolare destra e sinistra. In ultima istanza, i NP possono fornire un potere predittivo aggiuntivo all'ecocardiografia nei pazienti con IC e viceversa.
Ci sono 4 ragioni per usare in combinazione l'ecocardiografia e i NP per la stratificazione del rischio dei pazienti con IC. In primo luogo, indici ecocardiografici, come il rapporto E/Ea mitralico, e BNP sono stati correlati con le pressioni di riempimento ventricolare sinistro e hanno mostrato una elevata sensibilità per la pressione di incuneamento capillare polmonare (PCWP) maggiore di 15 mmHg, mentre il rapporto E/Ea mitralico mostra una migliore correlazione rispetto al BNP con la pressione di riempimento ventricolare sinistra e questo appare più preciso ed accurato nei pazienti con cardiopatia. Comunque, il rapporto E/Ea mitralico ha una significativa "zona grigia" e non è ben convalidato in caso di ritmo non sinusale o di valvulopatia, mentre i valori di NP possono essere utili nella valutazione delle pressioni di riempimento ventricolare sinistre nei pazienti in cui gli indici di Doppler tissutale sono risultati non conclusivi. In secondo luogo, i NP sono proteine rilasciate dal ventricolo in presenza di stiramento dei miociti, e i livelli di NP riflettono un insieme della funzione sistolica, diastolica, così come la funzione valvolare del ventricolo destro.
52
Per cui, sebbene i valori di NP correlino con la pressione di riempimento ventricolare sinistra, essi possono anche fornire informazioni cliniche indipendentemente rispetto ad altre anomalie morfologiche cardiache. Infatti, è stato già osservato come i NP siano già assodati indicatori a lungo termine di mortalità e ri-ospedalizzazione per IC indipendentemente dai parametri ecocardiografici.
In terzo luogo, i NP sono significativamente influenzati dall'età, dal sesso, dalla funzione renale e dall’obesità, per cui possono presentare una variabilità interindividuale nel tempo. Quindi i NP, sono caratterizzati dall'avere una elevata sensibilità, ma una bassa specificità nell'individuare elevate pressioni di riempimento ventricolari sinistre, mentre l'ecocardiografia può migliorare l'accuratezza della diagnosi e la prognosi di IC nel contesto dei valori di BNP o NT-proBNP. Quarta ragione è data dal fatto che il trattamento per i pazienti con IC può causare cambiamenti nel rapporto E/Ea mitralico e sui livelli di NP. Sebbene sia i livelli di NP che il rapporto E/Ea mitralico siano variabili utili nella gestione del paziente con IC, potrebbero essere non intercambiabili e rispondere differentemente durante il trattamento.
Avendo preso in considerazione pregi e difetti degli NP e del rapporto E/Ea mitralico, algoritmi derivati dalla loro combinazione possono essere utilizzati per stimare più accuratamente le pressioni di riempimento in pazienti che si presentano con dispnea. Inoltre, l’applicazione combinata degli indici ecocardiografici (rapporto E/Ea mitralico) e dei livelli di NP può
53
essere utile nel fornire informazioni prognostiche addizionali nei pazienti con IC, indipendentemente da altre variabili cliniche. Altri indici ecocardiografici della struttura e funzione cardiaca indicatori di prognosi sono la dimensione e la funzione del ventricolo sinistro, le variabili diastoliche Doppler del ventricolo sinistro e le dimensioni degli atrii destro e sinistro.
L’utilizzo combinato ,quindi, dell’ecocardiografia e degli NP mostra una migliore stratificazione del rischio attraverso tutti gli stadi dello IC cronica, compresa la classe NYHA I e II. In pazienti con IC sistolica stabilizzata dal trattamento medico, tale combinazione fornisce contributi indipendenti ed aggiuntivi alla stratificazione prognostica.
Nella gestione dei pazienti con IC acuta, la misura della pressione di riempimento del ventricolo sinistro rimane un aspetto critico. Sebbene la cateterizzazione cardiaca rimanga il gold standard, diversi parametri non invasivi, inclusi la valutazione clinica, il BNP, e l’ecocardiografia, sono stati utilizzati per approssimare la pressione di riempimento del ventricolo sinistro. Goonewardena et al. hanno cercato di utilizzare una combinazione di queste misure per predire non invasivamente le pressioni di riempimento del ventricolo sinistro in pazienti con IC acuta ed hanno comparato i loro risultati con la cateterizzazione del cuore destro. Hanno trovato che tutti i parametri hanno ben funzionato nel determinare una PCWP di 15 mmHg o maggiore, e che la pressione venosa giugulare, in combinazione con i parametri derivati dall’ecocardiografia e il BNP offrivano le migliori