INDICE Pagina RIASSUNTO 3 1. INTRODUZIONE 5 1.1 Definizioni 5 1.1.1 Crioglobulinemia e crioglobuline 5
Il fenomeno della crioprecipitazione 6
1.1.2 Crioglobulinemia Mista 8 1.2 Epidemiologia 9 1.3 Eziopatogenesi 10 1.4 Quadro clinico 12 1.4.1 Porpora 13 1.4.2 Fenomeno di Raynaud 15 1.4.3 Artralgie e artrite 16 1.4.4 Interessamento renale 17
1.4.5 Interessamento del sistema nervoso periferico 22
1.4.6 Interessamento epatico 23 1.4.7 Malattia linfoproliferativa 23 1.4.8 Sindrome di Sjogren 24 1.4.9 Altre manifestazioni 26 1.5 Diagnosi 30 1.6 Prognosi 32 1.7 Trattamento 33 1.7.1 Terapia di supporto 34 1.7.2 Terapia eziologica 34 1.7.3 Terapia immunosoppressiva 36 1.7.4 Terapia antiproliferativa 38 1.7.5 Terapia ipoantigenica 39
1.7.6 Terapia per la rimozione degli immunocomplessi circolanti (plasmaferesi)
40
1.7.7 Terapia antinfiammatoria 41
1.8 L’alfa-enolasi e gli anticorpi specifici per essa 43
SCOPO DELLA TESI 45
2.2 Estrazione dell’alfa-enolasi 47
2.3 Elettroforesi 49
2.4 Immunoblotting 51
2.5 Chemiluminescenza 52
3. RISULTATI 53
3.1 Analisi della casistica clinica 53
3.2 Ricerca di anticorpi anti-enolasi 57
4. DISCUSSIONE 60
Riassunto
La crioglobulinemia mista (CM) è una vasculite dei piccoli vasi
associata a infezione da virus dell'epatite C. In questa tesi sono stati
esaminati 100 pazienti affetti da CM seguiti presso la Reumatologia e la
Immuno-Allergologia dell'Università di Pisa.
La porpora rappresenta il segno d’esordio più frequente assieme alle
artralgie e all’astenia, configurando la classica triade nella metà dei
pazienti. In 70% dei pazienti è presente interessamento epatico e nel
65% dei casi interessamento del sistema nervoso periferico, clinicamente
evidente con parestesie agli arti e documentato dalla compromissione
della velocità di conduzione del nervo. In 22 pazienti si riscontra
interessamento renale, con valori di creatininemia e proteinuria nelle 24
ore alterati; in 4 casi sottoposti a biopsia renale è stata riscontrata una
glomerulonefrite membrano-proliferativa.
La sindrome sicca si presenta in una buona percentuale (46%) di pazienti
mentre il fenomeno di Raynaud è più scarsamente rappresentato (23%).
Da un punto di vista sierologico, la totalità dei pazienti presenta
positività del fattore reumatoide e marcata riduzione della componente
È stata recentemente descritta la presenza nei soggetti con CM di una
nuova specificità anticorpale, gli anticorpi anti-alfa enolasi.
Abbiamo misurato gli anticorpi anti-alfa enolasi nei sieri di 22 dei 100
pazienti mediante immunoblot su un estratto di rene umano e su enolasi
ricombinante. Complessivamente sono risultati positivi 10/22 sieri (1
con entrambe le enolasi, 4 solo su enolasi da rene, 5 solo su enolasi
ricombinante). In 6/22 pazienti era presente interessamento renale; 4/6
pazienti hanno anticorpi anti-alfa enolasi. Questi anticorpi sono presenti
in 6 dei 16 senza interessamento renale. Di interesse appare anche la
possibile associazione con forme linfoproliferative: 3/22 pazienti sono
affetti da linfoma e tutti hanno anticorpi anti-alfa enolasi.
Questi autoanticorpi possono quindi costituire un utile marker nel
Introduzione
1.1 Definizioni
1.1.1 Crioglobulinemia e crioglobuline
Con il termine crioglobulinemia si indica la presenza in circolo di
immunoglobuline (crioglobuline) che precipitano reversibilmente in
vitro a temperature inferiori a 37°C [1].
Il fenomeno è stato descritto per la prima volta nel 1933 da Wintrobe e
Buell in un caso di mieloma multiplo [2]. Nel 1947 Lerner e Watson
sono stati i primi ad usare il termine di “crioglobuline”, successivamente
distinte da altri autori in monoclonali (o solo IgG o solo IgM) e miste
(sia IgG che IgM in forma di immunocomplessi).
Questo fenomeno è stato osservato in un ampio spettro di malattie
infettive acute e croniche, stati infiammatori, disordini immunologici e
neoplastici.
La crioglobulinemia è classificata, a seconda della composizione del
crioprecipitato, in tre sottotipi:
- Tipo I : caratterizzata da un unico tipo di immunoglobulina monoclonale (IgG o IgM);
- Tipo II : caratterizzata da immunocomplessi formati da immunoglobuline policlonali di tipo IgG e immunoglobuline
monoclonali di tipo IgM con attività di fattore reumatoide;
- Tipo III : caratterizzata dagli stessi immunocomplessi del tipo II con la differenza che le IgM con attività di fattore reumatoide sono
policlonali.
La crioglobulinemia di tipo I o monoclonale è associata spesso a
disordini di tipo ematologico come la macroglobulinemia di
Waldestrom, il Mieloma Multiplo e altre affezioni
mielodisplastiche/linfoproliferative.
La crioglobulinemia di tipo II o III può presentarsi in corso di malattie
infettive o autoimmuni o costituire un’entità a se stante denominata
Crioglobulinemia Mista [1].
Il fenomeno della crioprecipitazione
I meccanismi della crioprecipitazione non sono ancora chiaramente
definiti. Nelle crioglobuline di tipo I la crioprecipitazione sembra essere
una caratteristica intrinseca delle immunoglobuline monoclonali,
frammenti Fc e Fab separati perdono solitamente la precipitabilità alle
basse temperature. Il processo di crioprecipitazione potrebbe essere
innescato da modificazioni della composizione aminoacidica o del
contenuto in carboidrati delle catene leggere e pesanti delle
immunoglobuline. Ne deriverebbe un complessivo aumento della
idrofobicità delle molecole con perdita della loro solubilità.
Nelle CM di tipo II e III la crioprecipitazione appare legata più
all'interazione fra immunoglobuline che alle caratteristiche delle singole
componenti immunoglobuliniche. Nelle crioglobulinemie miste IgG-IgM
la specifica componente che determina la crioprecipitazione è l’IgM
anti-IgG. Nessuna delle due globuline può crioprecipitare isolatamente,
tuttavia la componente IgM si comporta come una crioglobulina
incompleta, essendo in grado di crioprecipitare IgG di soggetti normali,
mentre non si osserva crioprecipitazione quando la componente IgG è
fatta reagire con un’IgM normale.
Un possibile ruolo crioprecipitante è stato attribuito alla fibronectina,
una proteina della fase acuta della flogosi, che è frequentemente ritrovata
nelle CM, specialmente in quelle associate a processi flogistici
autoimmuni, nelle quali le crioglobuline sono per lo più di tipo III.
Sembra, tuttavia, che tale glicoproteina, pur potendo svolgere un'azione
1.1.2 Crioglobulinemia Mista
La Crioglobulinemia Mista (CM) è inquadrata tra le vasculiti sistemiche,
nel sottogruppo delle vasculiti a carico dei piccoli vasi mediate da
immunocomplessi. Questo tipo di vasculiti sono anche chiamate
leucocitoclastiche per le caratteristiche dell’infiltrato flogistico formato
principalmente da polimorfonucleati con nuclei in carioressi. Ne fanno
parte, oltre alla CM, la porpora di Shonlein-Henoch, l’angioite cutanea
leucocitoclastica, vasculiti associate a connettiviti ed altre.
La CM viene ulteriormente suddivisa in secondaria, associata cioè ad
altre condizioni patologiche, e in essenziale, senza correlazione con altre
patologie.
La dizione di essenziale non ha più ragione di essere dalla scoperta,
nell’anno 1990, della correlazione molto stretta con l’infezione da virus
dell’epatite C (HCV).
Il quadro clinico della CM, descritto per la prima volta da Meltzer e
Franklin [4] nel 1966 come sindrome caratterizzata da porpora, astenia
ed artralgie, non si limita a questa triade, ma assume connotati più vasti,
comprendendo numerose patologie d’organo come la nefropatia,
l’epatopatia, la neuropatia ed altre, visto il carattere sistemico della
Nella trattazione della seguente tesi verrà presa in considerazione proprio
questa forma di crioglobulinemia [1].
1.2 Epidemiologia
La CM è un’affezione con una particolare distribuzione geografica,
essendo maggiormente frequente nell’Europa meridionale. Questo fatto,
assieme al frequente coinvolgimento del fegato e alla possibile
associazione con un ben determinato aplotipo HLA, hanno suggerito che
un fattore ambientale fosse l’evento scatenante la patologia. Sebbene il
primo candidato eziologico fosse il virus dell’epatite B (anni ’70), a
seguito di numerose ricerche il fattore ambientale è stato individuato nel
virus epatotropo HCV. Infatti, in una percentuale maggiore del 95% di
soggetti affetti da CM sono dimostrabili anticorpi rivolti contro vari
costituenti del virus e nel 90% dei pazienti HCV-RNA, indice di
infezione in atto ed inoltre anticorpi anti-GOR, proteina prodotta
dall’epatocita in risposta all’infezione. Quindi, quando andiamo a
considerare l’incidenza della CM, è giusto considerare lo stato endemico
I portatori di HCV, infatti, sono stimati essere a livello mondiale pari a
250 milioni, mentre in Italia ammontano a circa 2 milioni.
La presenza di crioglobuline è rilevabile in circa un terzo dei pazienti
affetti da infezione da HCV, ma le manifestazioni cliniche compaiono
solo nell'1-2% dei casi [1].
1.3 Eziopatogenesi
Nell’eziologia di questa vasculite un ruolo importante è svolto quindi dal
virus C dell’epatite [6] [7] [8]. Le possibili cause sono state ricercate
soprattutto nelle specifiche caratteristiche dell’agente infettivo, cioè nei
suoi diversi genotipi, e/o in una particolare predisposizione genetica
dell’ospite. Per quanto riguarda l’espressione genotipica dell’HCV nella
CM, è stata dimostrata una prevalenza significativa del genotipo 2a,
presente nel 40% dei pazienti. Per quanto riguarda invece l’influenza del
terreno genotipico del soggetto è stata evidenziata la prevalenza
significativa dell’aplotipo HLA B8/DR3. E’ stato inoltre valutata la
variabilità della risposta immune dell’ospite nei confronti del virus come
degli anticorpi rivolti contro la proteina virale NSA potrebbe essere
correlata con le manifestazioni cliniche della malattia (impegno epatico).
La patogenesi della vasculite è mediata da immunocomplessi; sono,
infatti, quest’ultimi i responsabili del danno vascolare. Il punto di
partenza nella patogenesi della CM è rappresentato dal virus dell’epatite
C. Difatti l’HCV è un virus epatotropo e linfotropo. L’interazione tra
l’HCV e il linfocita B avviene mediante il legame tra la proteina
dell’envelope virale E2 e il recettore cellulare CD81 del linfocita B. I
linfociti così infettati vanno incontro ad espansione policlonale. Si
assiste, infatti, ad un rimaneggiamento genetico durante lo sviluppo
precoce delle cellule B ed in particolare si verifica una traslocazione (14;
18) che conduce all’attivazione del gene bcl-2 con conseguente
inibizione dell’apoptosi dei linfociti B che vanno quindi a produrre
un’ampia quantità di immunoglobuline [9]. Le immunoglobuline così
prodotte si legano tra loro e vanno a formare immunocomplessi
(crioglobuline miste). La deposizione intravasale degli
immunocomplessi porta quindi al processo vasculitico. A seguito di tale
deposizione, viene attivato il complemento prevalentemente secondo la
via classica e vengono rilasciati fattori chemiotattici per i
radicali liberi dell’ossigeno, proteasi ed enzimi lisosomiali rilasciati da
parte dei leucociti stessi [1].
1.4 Quadro clinico
La storia naturale della malattia è caratterizzata di solito da una lenta
progressione, con periodi di riacutizzazione e periodi di remissione; solo
raramente si riscontrano delle emergenze cliniche. Il quadro
sintomatologico è assai variabile, potendo palesarsi con fenomeni
attenuati (scarse lesioni purpuriche, saltuarie artralgie) o manifestazioni
cliniche severe, come la glomerulonefrite rapidamente progressiva e la
vasculite sistemica.
L’età di insorgenza più comune è in genere la quinta decade di vita. E’
una malattia che interessa più frequentemente il sesso femminile, con un
rapporto F/M di 5/1.
Il quadro clinico si caratterizza per uno spiccato polimorfismo tanto che
la diagnosi è spesso tardiva o misconosciuta. La reale prevalenza di
questa patologia è dunque sottostimata.
Le principali manifestazioni cliniche sono costituite da astenia, porpora,
si riscontrano in associazione ad una malattia linfoproliferativa benigna
che si presenta sotto forma di aggregati linfocitari a livello epatico,
splenico e del midollo osseo [5] [6].
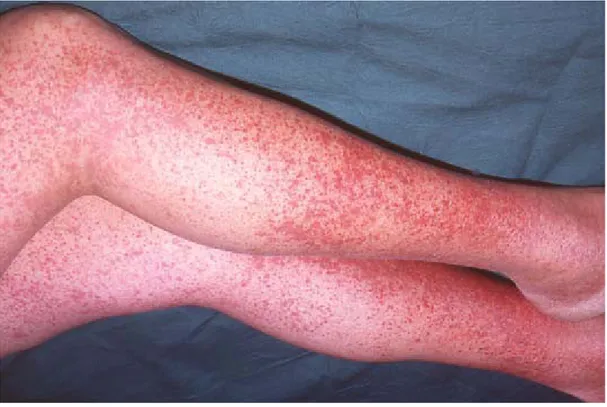
1.4.1 Porpora
La porpora rappresenta una delle manifestazioni più precoci e frequenti
della crioglobulinemia mista, essendo rilevabile in oltre l’80% dei
pazienti e rappresenta spesso proprio la prima manifestazione della
malattia. Intermittente, palpabile, non pruriginosa, ha carattere
ortostatico, localizzandosi preferenzialmente agli arti inferiori con la
caratteristica disposizione “a calzino”. Può estendersi anche alle cosce e,
seppur raramente, al tronco soprattutto in sedi oggetto di compressione
elastica da parte degli indumenti. Si sussegue in poussées, generalmente
ad intervalli variabili di 7-10 giorni. Le aree in cui le gittate purpuriche
tendono a ripetersi assumono col tempo una pigmentazione
bruno-ocracea.
Le caratteristiche localizzazioni sono dovute probabilmente alla più
In una certa percentuale di pazienti si possono presentare, come segno
iniziale di malattia, ulcere alle gambe associate alla porpora, che spesso
mostrano un carattere ingravescente e sono di difficile guarigione.
La biopsia cutanea dimostra una vasculite leucocitoclastica dei capillari
e delle venule post-capillari del derma superficiale con variabile
coinvolgimento dei vasi sottocutanei. L'immunofluorescenza rivela
depositi vascolari d’immunoglobuline (IgG, IgM) e/o complemento
(C4). Nei pazienti crioglobulinemici con infezione da HCV la vasculite
cutanea si caratterizza per la deposizione di immunocomplessi costituiti
da HCV, IgM FR e IgG [5].
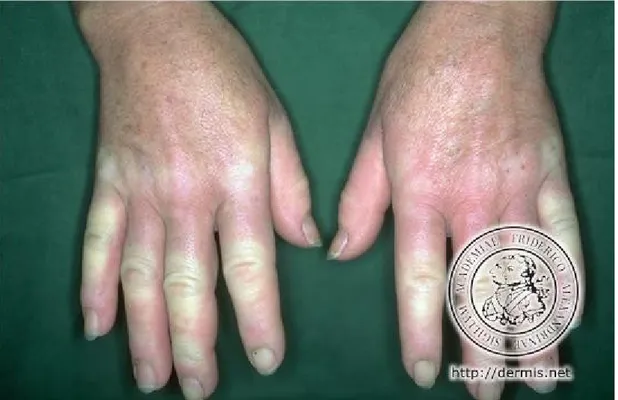
1.4.2 Fenomeno di Raynaud
Il fenomeno di Raynaud rappresenta un’altra manifestazione della
malattia, riscontrabile nel 25% dei pazienti al momento della diagnosi. Si
presenta di lieve intensità e seppur coinvolgendo tutte le estremità, solo
raramente può portare a disturbi distrofici fino ad una vera e propria
gangrena delle dita delle mani e/o dei piedi [10].
Si tratta di un’ischemia acrale parossistica, scatenata dal freddo o dalle
brusche riduzioni della temperatura, che si manifesta con una variazione
del colorito cutaneo. In genere compare dapprima il pallore, seguito dalla
cianosi e quindi dalla comparsa di un colorito rosso cupo (presentazione
a “bandiera francese”), ma possono manifestarsi anche la sola fase di
pallore (fase sincopale pura) o la cianosi in assenza della fase di
Fig. 2.Fenomeno di Raynaud con la caratteristica presentazione “a bandiera francese”.
1.4.3 Artralgie e artrite
L’interessamento articolare è presente in oltre il 70% dei casi. Le
artralgie hanno un carattere intermittente, prive di ritmo notturno e
rigidità mattutina, a scarsa o nulla obiettività flogistica. Interessano
maggiormente mani, ginocchia, caviglie e gomiti.
L'artrite colpisce essenzialmente le articolazioni "satelliti" della porpora,
quindi ginocchia e caviglie; non è erosiva e non porta a deformità
1.4.4 Interessamento renale
Le manifestazioni renali [12] sono presenti nel decorso della
crioglobulinemia in oltre il 50% dei casi. Nel 30-40% dei casi si assiste
ad un esordio con sindrome nefritica acuta, talora di tipo rapidamente
evolutivo, nel 20% si tratta di una sindrome nefrosica e nel 40-50% dei
casi si presenta proteinuria, microematuria, ipertensione ed insufficienza
renale progressiva.
Istologicamente la nefropatia presenta gli aspetti di una glomerulonefrite
membranoproliferativa di tipo I, caratterizzata quindi da depositi
elettrondensi subendoteliali.
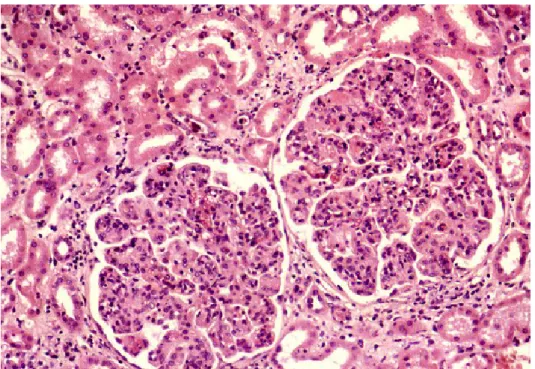
Alla microscopia ottica si rileva notevole infiltrazione intraglomerulare
di monociti e polimorfonucleati, trombi intracapillari, ispessimento della
Fig. 3.Glomerulonefrite crioglobulinemica: lesioni membranoproliferative con notevole ipercellularità, aumento di volume e lobulazione glomerulare (in M.O.)
Fig.4.Glomerulonefrite crioglobulinemica: ipercellularità glomerulare, ispessimento della parete capillare e aumento della matrice con lobulazione. Trombi intracapillari di crioglobuline, presenti anche in un capillare interstiziale (frecce)(in M.O.)
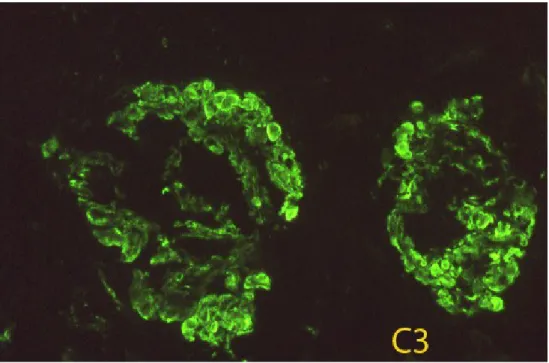
All’immunofluorescenza si repertano depositi contenenti le
immunoglobuline presenti nelle crioglobuline circolanti, complemento
(C3) a minore intensità e C1q nel 30% dei casi.
fig. 5.Depositi di C3, prevalentemente sulle anse periferiche (Immunofluorescenza)
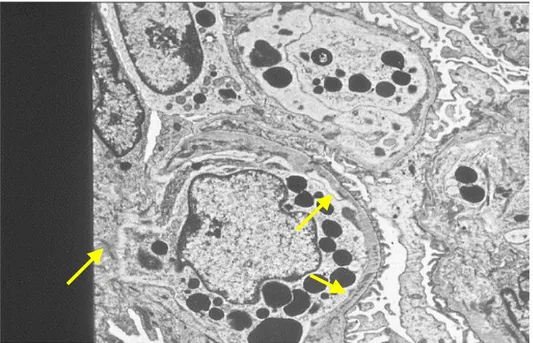
Alla microscopia elettronica si evidenziano depositi subendoteliali
amorfi od organizzati in microtubuli, monociti e cellule endoteliali
contenenti corpi lisosomiali elettrondensi.
fig. 7.Piccoli depositi elettrondensi subepiteliali e mesangiali (frecce). Macrofagi contenenti vacuoli elettrondensi .
La patogenesi del danno renale rimane al momento non ancora chiara.
Possono essere chiamati in causa due possibili meccanismi di danno
glomerulare [13]. Il primo è rappresentato dalla deposizione a livello
renale di immunocomplessi circolanti; il secondo dalla formazione di
direttamente con gli antigeni tissutali intrinseci o con antigeni circolanti
“impiantati” nel glomerulo.
Diversi fattori influenzano la localizzazione glomerulare di antigeni,
anticorpi e immunocomplessi. La carica e la dimensione delle molecole
sono naturalmente importanti. Sostanze immunogene altamente
cationiche tendono ad attraversare la membrana basale del glomerulo ed
i complessi risultanti si localizzano in sede subepiteliale. Macromolecole
altamente anioniche, invece, non riescono ad attraversare la membrana e
pertanto vengono intrappolate a livello subendoteliale oppure non sono
affatto nefrolesive. Molecole con una carica neutra ed immunocomplessi
contenenti queste molecole tendono ad accumularsi nel mesangio.
Grandi complessi circolanti, come riscontriamo nella CM, non sono di
solito nefritogeni poiché vengono eliminati dagli elementi
monocito-macrofagici al contrario di quelli di più piccole dimensioni che sfuggono
alla clearance e vanno a depositarsi a livello renale. Da questo si evince
che teoricamente, e spesso anche in pratica, l’impegno renale esclude
quello epatico e viceversa. Difatti nella CM l’impegno epatico è tre volte
più frequente di quello renale in accordo al fatto che gli
immunocomplessi che si formano sono di grosse dimensioni, essendo
1.4.5 Interessamento del sistema nervoso periferico
Un coinvolgimento nervoso periferico è abbastanza comune nei soggetti
crioglobulinemici anche se la frequenza effettiva viene sottostimata per
il fatto che il quadro clinico è spesso sfumato.
Una compromissione delle fibre sensitive è la manifestazione clinica
neurologica più frequente. Sintomi clinici suggestivi per un danno
neurologico sono presenti nella maggior parte (91%) dei pazienti tuttavia
dati clinici obiettivabili, come una riduzione della velocità di
conduzione, si riscontrano solamente nella metà dei pazienti. Una
neuropatia motoria è molto più rara, essendo riscontrata solo nel 5% dei
casi.
Il danno neurologico può essere causato da una demielinizzazione
mediata da immunocomplessi o autoanticorpi, da una vasculite dei vasa
nervorum o da un’ostruzione vascolare legata a crioprecipitati. Studi
istologici documentano un danno vascolare ed una degenerazione
assonale.
La correlazione esistente tra livelli di crioglobuline sieriche e varie
manifestazioni neurologiche suggerisce che un meccanismo
1.4.6 Interessamento epatico
Un coinvolgimento epatico è riportato in oltre i due terzi di tutte le
crioglobulinemie e virtualmente in tutte le CM di tipo II associate ad
infezione cronica da HCV. Generalmente l'epatopatia è clinicamente
asintomatica. I marcatori bioumorali di danno epatocitario sono normali
o moderatamente elevati, ma non risultano correlati con il quadro
istologico. Infatti, in tutti i casi si riscontrano vari gradi di danno
epatocellulare con infiammazione periportale, fibrosi, riarrangiamento
dell’architettura epatica e cirrosi in un terzo dei casi [5].
1.4.7 Malattia linfoproliferativa
I soggetti con CM presentano una più alta incidenza di disturbi
linfoproliferativi.
Nelle Crioglobulinemie miste di tipo II associate all'infezione da HCV
sono frequentemente documentati a livello epatico, splenico e midollare
infiltrati linfoidi benigni. Meno frequentemente, i pazienti possono
sviluppare un linfoma Non-Hodgkin a cellule B. L’incidenza di linfoma
pazienti a più del 40% con la comparsa a 5-10 anni dalla diagnosi di
crioglobulinemia [15] [16].
Il virus C dell’epatite è stato riscontrato in cellule mononucleari presenti
sia nel sangue periferico che nel midollo osseo e cosa molto interessante,
in cellule linfomatose di pazienti con crioglobulinemia mista di tipo II o
con infezione cronica da virus C dell’epatite in evoluzione verso un
linfoma Non-Hodgkin. Tali osservazioni suggeriscono un possibile ruolo
patogenetico del virus C dell’epatite in alcune malattie linfoproliferative.
Tale ipotesi è suffragata anche dal fatto che un’alta incidenza di
infezione cronica da parte del virus C dell’epatite è stata riscontrata in
almeno un terzo dei casi di pazienti non selezionati affetti da linfoma
Non-Hodgkin [5].
1.4.8 Sindrome di Sjogren
Una sindrome sicca con xerostomia e xeroftalmia è presente in una
significativa percentuale di pazienti [10]. Il virus C dell’epatite è infatti
scialotropo e può localizzarsi a livello delle ghiandole esocrine, in
particolar modo delle salivari. In questi pazienti può essere riscontrata
sierologico questi soggetti si caratterizzano, frequentemente, per la
presenza di anticorpi anti ENA di tipo SSA ed SSB. Quando la porpora e
l’interessamento epatico sono più sfumati, può risultare difficile una
diagnosi differenziale fra una crioglobulinemia con sindrome di Sjogren
secondaria ed una sindrome di Sjogren primitiva con manifestazioni
sistemiche.
Negli ultimi criteri classificativi della sindrome di Sjogren pubblicati, la
presenza di infezione da HCV esclude la diagnosi. Si tratta però di criteri
classificativi e non diagnostici. Si tende a formulare la diagnosi di
sindrome di Sjogren quando la sindrome sicca è prevalente, quando il
danno epatico è assente o moderato e quando si riscontrano anticorpi
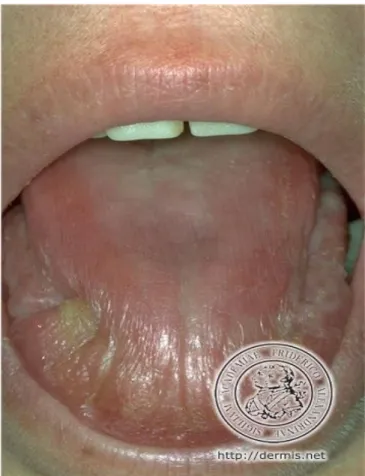
fig. 8.Secchezza ed arrossamento della mucosa orale in corso di sindrome sicca.
1.4.9 Altre manifestazioni
Tra i vari organi che possono essere interessati nella crioglobulinemia
sono da ricordare l’intestino, i polmoni, le sierose ed infine il SNC.
Per quanto riguarda il coinvolgimento gastroenterico, si possono
manifestare in una certa percentuale di pazienti dolori addominali talora
così violenti da configurare il quadro di addome acuto con ileo
paralitico. Alla base di tale patologia vi è una vasculite mesenterica che
pareti addominali oppure con un’estesa necrosi intestinale tale da
rendere necessaria una resezione chirurgica.
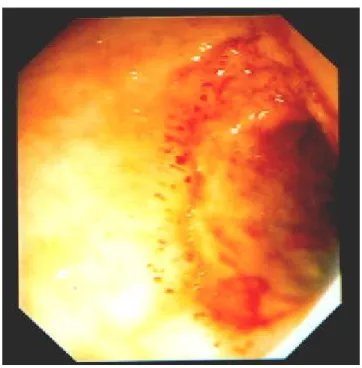
fig. 9. Petecchie emorragiche sulla mucosa intestinale di paziente con CM
L’interessamento polmonare [17] [18] si può presentare con un quadro di
interstiziopatia verosimilmente dovuta a deposizione di
immunocomplessi che raramente evolve verso la fibrosi.
In una percentuale molto esigua di pazienti si può riscontrare una
Rivestono inoltre notevole importanza le numerose malattie che possono
associarsi con la presenza di crioglobuline nel siero; si può trattare di
malattie linfoproliferative, infettive e molto frequentemente con altre
Malattie linfoproliferative
- Linfoma non-Hodgkin - Mieloma Multiplo
- Macroglobulinemia di Waldenström - Leucemia linfatica cronica
- Linfoadenopatia angioimmunoblasti-ca
Malattie infettive
Virali
- Epatite B e C
- Virus dell'immunodeficienza umana (HIV)
- Citomegalovirus (CMV) - Mononucleosi (EBV)
Batteriche
- Lebbra
- Endocardite batterica subacuta - Sifilide - Linfogranuloma venereo Parassitarie - Echinococcosi - Malaria - Toxoplasmosi - Leismaniosi - Schistosomiasi Fungine - Coccidioidomicosi Malattie autoimmuni e da immunocomplessi
- Lupus Eritematoso Sistemico - Artrite Reumatoide
- Sindrome di Sjögren - Sindrome di Felty - Sclerosi sistemica - Polimiosite
- Poliarterite nodosa (HBsAg positiva e negativa) - Sindrome di Behçet - Porpora di Henoch-Schönlein - Vasculite autoimmune - Glomerulonefrite - Tiroidite autoimmune - Sarcoidosi - Malattia celiaca - Pemfigo volgare
1.5 Diagnosi
Il sospetto diagnostico di crioglobulinemia deve insorgere in un paziente
che presenta i sintomi sistemici descritti in precedenza ed in cui
compaiono le manifestazioni cutanee agli arti inferiori associate a segni
d’interessamento renale ed epatico. L’aumento degli indici di flogosi
(VES e PCR) associato alla positività del fattore reumatoide, all’aumento
delle transaminasi ed eventualmente a segni di danno renale, suggerisce
l’esecuzione della sierologia per il virus C dell’epatite. Inoltre
l’ipocomplementemia (soprattutto della frazione C4) accompagnata dalla
negatività degli anticorpi anti-antigeni nucleari (ANA) e dalla positività
della determinazione qualitativa e quantitativa delle crioglobuline
indirizza correttamente la diagnosi.
Esistono dei criteri classificativi attraverso i quali è possibile fare una
diagnosi di certezza o di probabilità di crioglobulinemia. Sono suddivisi
in criteri maggiori e minori e questi a loro volta in criteri sierologici,
CRITERI MAGGIORI CRITERI MINORI CRITERI SIEROLOGICI • crioglobuline miste • ipocomplementemia (C4) • FR + • HCV + • HBV + CRITERI ISTOLOGICI • vasculite leucocitoclastica • Infiltrati B-cellulari • (epatici, midollari) CRITERI CLINICI
• porpora • epatite cronica
• glomerulonefrite membranoproliferativa • neuropatia periferica • ulcere cutanee
Tab 2.Criteri classificativi per la diagnosi di crioglobulinemia mista
DIAGNOSI DI CERTEZZA: 3 criteri maggiori oppure 1 criterio sierologico
maggiore + 2 minori clinici + 2 minori istologici/sierologici.
DIAGNOSI DI PROBABILITA’:
• 1 criterio sierologico maggiore + 1 clinico minore + 1 minore sierologico o istologico
• porpora o vasculite leucocitoclastica + 1 sintomo clinico minore + 1 minore sierologico o istologico
1.6 Prognosi
Il decorso clinico della CM è generalmente benigno: la malattia è spesso
oligosintomatica anche per lunghi intervalli di tempo, caratterizzati
primariamente da astenia, artralgie e saltuari episodi di porpora
ortostatica. Tuttavia, in alcuni pazienti la qualità della vita è spesso
compromessa a causa di un’intensa astenia e/o neuropatia periferica
generalmente di tipo sensitivo. In una percentuale inferiore di casi può
esordire od evolvere verso complicanze particolarmente gravi come la
glomerulonefrite, la neuropatia periferica sensitivo-motoria, la vasculite
diffusa, l’epatite cronica/cirrosi, le neoplasie. Come precedentemente
riportato, una percentuale tutt’altro che indifferente (40%) di pazienti
affetti da CM può sviluppare un linfoma maligno.
La sopravvivenza, valutata a 10 anni dalla diagnosi, risulta
significativamente ridotta rispetto alla popolazione generale. I principali
fattori prognosticamente negativi sono il sesso maschile, la presenza di
nefropatia cronica ed ovviamente l’insorgenza di complicanze
1.7 Trattamento
Lo scopo della terapia della CM è quello di:
1. contrastare gli agenti eziologici responsabili della CM;
2. inibire la sintesi delle crioglobuline da parte dei linfociti B;
3. ridurre la formazione degli immunocomplessi circolanti;
4. rimuovere gli immunocomplessi circolanti;
5. ridurre la componente infiammatoria.
La terapia della sindrome crioglobulinemica si avvale delle seguenti
opzioni terapeutiche:
1. Terapia di supporto;
2. Terapia eziologica;
3. Terapia immunosoppressiva;
4. Terapia antiproliferativa;
5.Terapia per la rimozione degli immunocomplessi circolanti
(plasmaferesi);
6. Terapia ipoantigenica;
1.7.1 Terapia di supporto
La terapia di supporto si avvale di semplici regole di vita, come ad
esempio evitare l’esposizione alle basse temperature o al freddo,
proteggendo le estremità del corpo con indumenti adeguati, evitare
un’eccessiva attività fisica ed evitare una stazione eretta per periodi
prolungati.
1.7.2 Terapia eziologica
L’impiego dell’interferone alfa (IFN) [19] [20] nella CM iniziò nel
1987 non appena questa classe di farmaci si rese disponibile. Non
essendo ancora nota l’eziologia della malattia, l’IFN veniva utilizzato
per la sua azione antiproliferativa e immunomodulante e il successo
terapeutico venne
attribuito alla capacità del farmaco di inibire selettivamente i cloni B
linfocitari produttori delle crioglobuline. Dopo la scoperta dell’HCV e i
successi ottenuti con l’IFN nella terapia dell’epatite cronica
HCV-positiva, è sembrato razionale l’impiego di tale farmaco nella CM.
L’IFN infatti costituisce la terapia d’elezione della malattia in quanto è
però non è da attribuire soltanto alla sua attività antivirale, ma
probabilmente anche alla sua azione immunomodulante, in quanto si
riscontra un miglioramento della sintomatologia anche nei soggetti in cui
non si ottiene l’eradicazione dell’HCV. Nei primi studi, la risposta
primaria dell’IFN in monoterapia variava, secondo i vari autori, dal 30 al
60% ma l’eradicazione dell’HCV si verificava soltanto in una piccola
percentuale di casi (15-20%), e inoltre, alla sospensione del trattamento,
la grande maggioranza dei pazienti presentava una recidiva clinica e la
ricomparsa dell’HCV-RNA. Anche se i successi con l’IFN in
monoterapia erano limitati, si intuì subito che l’IFN risultava comunque
l’unico trattamento in grado di portare a remissione completa la CM.
Dopo la dimostrazione che, nelle epatiti croniche da HCV, l’inserimento
di nuovo farmaco antivirale, la ribavirina, risultava particolarmente
utile nel trattamento dei soggetti non responsivi o ricaduti, la terapia di
combinazione è stata utilizzata, con le medesime indicazioni, anche nella
terapia della CM [21].
Il trattamento antivirale inoltre, contestualmente all’eradicazione
dell’HCV, determina una regressione della linfoproliferazione
monoclonale presente a livello del midollo o nel sangue periferico,
prevenendo l’ulteriore sviluppo di tale patologia verso malattie più
1.7.3 Terapia immunosoppressiva
L’uso degli steroidi costituisce la terapia tradizionale della CM. Questi
farmaci sono indicati nelle CM paucisintomatiche, oppure in quelle con
esteso e grave impegno viscerale. Infatti, anche a basso dosaggio, i
cortisonici sono in grado di controllare gran parte delle manifestazioni
cliniche della CM per periodi prolungati. Sono utili per controllare la
sintomatologia purpurica e artralgica, ma funzionano più per la loro
attività anti-infiammatoria che per l’inibizione della sintesi delle
crioglobuline, infatti il miglioramento clinico dei pazienti trattati non
sembra correlato con una riduzione della concentrazione delle
crioglobuline. Inoltre in nessun studio è stato dimostrato che tale classe
di farmaci sia in grado di modificare la storia naturale della malattia.
Anche questi farmaci presentano una serie di effetti collaterali importanti
(diabete, ulcera ed osteoporosi per citarne i più comuni) accentuati dal
fatto che vengono utilizzati per periodi molto lunghi. Vi sono
osservazioni di aumento della viremia nei pazienti trattati con steroidi e
pertanto questi vengono consigliati soltanto nelle forme in cui vi siano
manifestazioni vasculitiche acute o nella fase di acuzie della
glomerulonefrite crioglobulinemica. Recentemente sono stati introdotti
anticorpi rappresentano un’evoluzione “estrema” della terapia
immunosoppressiva in quanto in grado di distruggere le cellule B CD20
positive, che sono le cellule che producono anticorpi. Il meccanismo
d’azione comprende lisi complemento-mediata, citotossicità
anticorpo-dipendente ed induzione di apoptosi delle cellule suddette. Il grande
vantaggio di tale terapia è quello di non avere gli effetti collaterali degli
steroidi e di essere altrettanto efficace dei trattamenti immunosoppressivi
convenzionali. Vi sono 2 recentissimi studi sulla efficacia e tollerabilità
di tali anticorpi nella CM [22] [23]. Sebbene con sfumature diverse,
entrambi indicano l’ottima tollerabilità della terapia e la grande efficacia
nella risoluzione dei fenomeni vasculitici e della sintomatologia
soggettiva. Dibattuta è l’efficacia della terapia a lungo termine. Alcuni
autori [22] affermano che, nel tempo, la malattia tenderà sempre a
ripresentarsi, dal
momento che il trattamento non solo non elimina il virus, ma tende ad
aumentarne la replicazione. Altri autori [24] sostengono invece che il
rituximab sia un’opzione terapeutica sicura ed efficace nel trattamento di
pazienti sintomatici con glomerulonefrite e segni di vasculite sistemica.
Infatti si assiste, oltre alla scomparsa o al miglioramento della
sintomatologia, alla riduzione dei livelli di proteinuria, del criocrito e del
livelli di C4 da 2 a 6 mesi ma, cosa molto importante, il livello della
carica virale rimane stabile.
1.7.4 Terapia antiproliferativa
Nella terapia della CM si possono utilizzare anche farmaci citostatici
che, per la loro azione litica sulle cellule B, sono in grado di ridurre la
concentrazione plasmatica delle crioglobuline. I farmaci citostatici si
sono dimostrati particolarmente efficaci nelle CM di tipo I e II, dove in
effetti è quasi sempre presente una patologia linfoproliferativa
monoclonale. In assenza di studi clinici controllati, le terapie citostatiche
venivano in genere utilizzate quando la terapia steroidea non risultava
più efficace. I citostatici più utilizzati sono il clorambucil e soprattutto la
ciclofosfamide. Attualmente, vista la stretta associazione tra l’HCV e la
CM, l’uso di questi farmaci risulta ristretto solamente ai casi di CM di
tipo I, e a quelli in cui la patologia linfoproliferativa evolve verso un
linfoma conclamato, oppure ancora nei casi in cui è presente una
1.7.5 Terapia ipoantigenica
Una dieta a basso contenuto di antigeni alimentari si è dimostrata
efficace nel controllare le manifestazioni cliniche minori della malattia.
Il razionale della dieta consiste nel fatto che comporta la riduzione del
numero di macromolecole esogene che, tramite il sangue portale,
giungono al fegato, ove vengono processate dalle cellule di Kupfer,
riducendone la capacità di clearance nei confronti degli
immunocomplessi circolanti. Ecco allora che fornendo una dieta a basso
contenuto di macromolecole, risulta alleviata la funzione del sistema
monocitomacrofagico, con una migliore capacità di clearance degli
immunocomplessi, tra cui anche le crioglobuline. La dieta, basata
sull’assunzione di riso, pasta, carni bianche e poche verdure e
somministrata in modo intermittente, sembra determinare un beneficio
solo sulle manifestazioni minori della CM, ma gli effetti sui parametri di
laboratorio (criocrito e fattore reumatoide) sono modestissimi. La dieta è
efficace nei casi paucisintomatici, ma vi sono notevoli problemi di
1.7.6 Terapia per la rimozione degli immunocomplessi circolanti (plasmaferesi)
La plasmaferesi tradizionale (PE) o selettiva (DFPP), è una metodica
che consente la sostituzione del plasma del paziente con emocomponenti
o succedanei, permettendo la rimozione di sostanze patogene esogene
(tossici, veleni), o endogene (autoanticorpi, immunocomplessi, e
crioglobuline). La plasmaferesi presenta scarsi effetti collaterali, quali
modesta anemia e deplezione proteica, la quale può essere corretta
somministrando albumina o plasma a secondo delle diverse tecniche
usate. Vi sono una serie di studi non controllati che evidenziano come la
plasmaferesi sia di particolare utilità nella CM [27]. Il meccanismo
d’azione è ovviamente la rimozione delle crioglobuline assieme ad
un’azione favorente sulla attività del sistema reticolo-endoteliale. La
plasmaferesi ha efficacia limitata nel tempo e se non è associata ad altre
terapie farmacologiche fornisce risultati del tutto temporanei. In genere
durante o subito dopo le aferesi, il paziente viene trattato con
ciclofosfamide (2 mg/kg/die) o con una combinazione di ciclofosfamide
e corticosteroidi per ridurre l’effetto rebound provocato alla sottrazione
delle crioglobuline dal circolo [28]. Poiché si è dimostrata
della CM, le indicazioni attuali alla plasmaferesi sono la
glomerulonefrite crioglobulinemica, la sindrome da iperviscosità, la
neuropatia periferica sensitivo-motoria grave e le ulcere cutanee.
1.7.7 Terapia antinfiammatoria
Nella vasculite crioglobulinemica un’utile opzione terapeutica è
rappresentata dalla colchicina e dagli antinfiammatori non steroidei
(FANS). La colchicina è un farmaco usato nell’artrite acuta gottosa, in
cui ha un’efficacia straordinaria. Il farmaco ha molteplici azioni:
interferendo con la formazione dei microtubuli impedisce le mitosi dei
linfociti e dei monociti, riduce la chemiotassi e l’adesività dei granulociti
neutrofili e blocca la secrezione delle immunoglobuline. In
considerazioni di tali proprietà anche la colchicina è stata utilizzata in
passato nella CM. Si evidenziavano risultati soddisfacenti dal punto di
vista clinico, mentre scarsa era stata l’efficacia sui livelli di criocrito e di
fattore reumatoide. Poiché il farmaco presenta effetti collaterali non
trascurabili sia a livello gastroenterico (diarrea, epigastralgie, ecc.) che
ematologico (leuco-piastrinopenia) un trattamento con colchicina può
essere raccomandato solo nel caso di fallimento o di intolleranza verso
Gli anti-infiammatori non steroidei vengono usati dai pazienti nei casi
di riacutizzazioni delle artralgie a scopo esclusivamente antalgico.
Sicuramente un loro uso esteso e prolungato non è consigliabile stante il
frequente coinvolgimento renale in corso di CM. Inoltre i noti effetti
collaterali dei FANS a livello gastrico ne consigliano un uso molto
1.8 L’alfa-enolasi e gli anticorpi specifici per essa
Nei soggetti con CM è stata recentemente descritta una nuova specificità
anticorpale, gli anticorpi anti-alfa enolasi [30].
L’enolasi è un’enzima glicolitico, di peso molecolare di circa 50 kDa,
coinvolto nella deidratazione dell'acido 2-fosfoglicerico a
fosfoenolpiruvato.
Nella specie umana esistono 3 differenti isoenzimi dell’enolasi che
possono associarsi tra loro a formare omodimeri oppure eterodimeri
[31].
La beta-enolasi è associata al tessuto muscolare mentre la
L’alfa-enolasi è invece ubiquitaria, e sebbene sia virtualmente espressa
in ogni tessuto, essa è maggiormente espressa nel timo e nel tessuto
renale.
E' un enzima citoplasmatico, espresso inoltre sulla membrana di diversi
tipi di cellule comprese cellule endoteliali e cellule linfo-monocitarie
attivate.
L'alfa enolasi, oltre alla sua funzione principale nel ciclo glicolitico
agisce anche come heat shock protein (nel lievito) e come proteina
indotta dall'ipossia (nelle cellule endoteliali); come proteina strutturale
nella lente del cristallino; come fattore di virulenza capace di facilitare la
penetrazione di microrganismi (p.e. Streptococcus pneumoniae); come
recettore di membrana del plasminogeno quando espressa sulla
superficie delle cellule.
Infine, una forma troncata dell'alfa-enolasi di 38 kDa agisce come fattore
Scopo della tesi
Lo scopo della tesi è di analizzare le caratteristiche cliniche di un gruppo
di pazienti (n=100) seguiti presso gli ambulatori dell’U.O. di
Reumatologia ed Immunoallergologia dell’Università di Pisa in cui è
stata diagnosticata una crioglobulinemia mista. E’ stata ricercata, in un
sottogruppo di 22 pazienti, la presenza di anticorpi specifici per
l’alfa-enolasi con la metodica dell’immunoblot su un estratto renale e su
enolasi ricombinante e successiva rilevazione tramite
chemiluminescenza. Inoltre è stata indagata un’eventuale correlazione
Materiale e metodi
2.1 Lisato totale di rene umanoCorticale renale umana è stata ottenuta da reni rimossi a causa di
carcinoma renale. Il tessuto da noi utilizzato proveniva da zone non
interessate dal carcinoma.
Il tessuto ottenuto è stato ridotto in frammenti, congelato in azoto liquido
e omogenizzato in un "blender". Il tessuto polverizzato è stato poi
risospeso in Tris-HCl 50 mM pH 6.8, NaCl 150 mM, EDTA 20 mM,
Triton X-100 1% in presenza di inibitori delle protasi.
La concentrazione proteica delle varie frazioni è stata determinata con
metodo BCA (acido bicinconinico), basata sulla reazione delle proteine
con Cu++ che formano un complesso con il colorante BCA in ambiente
alcalino, mediante lettura spettrofotometrica a λ=562 nm; dal confronto dell'assorbanza dei campioni con quella di una curva standard è stata
2.2 Estrazione dell'alfa-enolasi
L'alfa-enolasi utilizzata in immunoblotting è una proteina ricombinante
prodotta da E. coli.
Il cDNA corrispondente al segmento 10-434 aa dell'alfa-enolasi umana è
clonato ed inserito nel vettore pGex.
Il DNA viene inserito a valle di una sequenza che codifica per la
Glutation-S-Trasferasi (GST), che viene indotta insieme all'alfa-enolasi
risultando in un unico prodotto di fusione di circa 75 kDa.
La presenza della GST permette la purificazione della proteina di fusione
mediante resina di Sepharoso-Glutatione ed eluizione con Glutatione.
L'espressione di alti livelli della proteina è resa possibile dalla presenza
nel plasmide del promotore T7.
Il vettore pRset. è transfettato in E. coli del ceppo BLRI(DE3)p LysS che
contiene un lisogeno esprimente la polimerasi T7 sotto il controllo del
promotore lacU5.
In presenza di iso-propil-tio-galactoside (IPTG) le cellule sono indotte
ad esprimere alti livelli di RNA polimerasi T7, che permette l'elevata
trascrizione della proteina ricombinante sotto la guida del promotore T7.
I batteri E. coli BLRI(DE3)p LysS transfettati sono prima piastrati su LB
Successivamente 3 ml di SOB (un terreno di coltura non selettivo)
contenente ampicillina 50 µg/ml e cloramfenicolo 35 µg/ml sono
inoculati con una singola colonia di batteri ricombinanti e fatti crescere
over night in agitazione.
Il giorno successivo i 3 ml sono diluiti con 250 ml di SOB contenente
ampicillina 50 µg/ml e fatti crescere a 30° C in agitazione fino ad una
OD600 =0,4 - 0,6.
A questo punto viene aggiunto IPTG che induce la produzione di
alfa-enolasi ricombinante e i batteri vengono lasciati a 30° C per 4 ore.
Trascorso il periodo di induzione il mezzo contenente i batteri indotti
viene centrifugato per 30 minuti a 2500 rpm a temperatura ambiente. Il
surnatante della centrifugazione viene eliminato e i pellet contenti i
batteri indotti vengono congelati a - 20 ° C.
Per la purificazione della proteina ricombinante, il pellet dei batteri
indotti è risospeso in NaH2PO4 50 mM, NaCl 500 mM,
ß-mercaptoetanolo 5mM + inibitori delle proteasi.
Vengono quindi effettuati 3 cicli di congelamento e scongelamento per
favorire la lisi dei batteri.
Al termine di tali cicli, i batteri vengono incubati 30' a + 4° C con
Tween-20 1%; il lisato batterico è, infine, centrifugato a 15000 rpm per
30' a + 4° C.
Poichè durante la lisi l'alfa-enolasi-GST precipita in strutture chiamate
"corpi di inclusione", che in queste condizioni di centrifugazione si
ritrovano nel pellet, e viene solubilizzata solo da forti condizioni
denaturanti, il surnatante viene eliminato ed il pellet è risospeso in
NaH2PO4 100 mM, Tris 10 mM, Guanidina 3 M pH 8 e dializzato tutta
la notte contro PBS.
Il dializzato è, quindi, caricato su una resina di Sepharoso-Glutatione che
interagisce con la GST, trattenendo la proteina di fusione.
Dopo alcuni lavaggi con NaH2PO4 20 mM (fino a che OD280 = 0.01) e
con NaH2PO4 20 mM, GST 60mM, per eliminare ciò che si lega in
modo aspecifico, la proteina viene eluita con Tris 50 mM, GST 15mM.
2.3 Elettroforesi
I campioni di alfa-enolasi e di lisato totale di rene prima di venire
sottoposti ad elettroforesi sono stati trattati con sodio dodecilsolfato
(SDS) e 2-beta-mercaptoetanolo. Il SDS, detergente fortemente anionico,
proteina una carica netta negativa; il 2-beta-mercaptoetanolo riduce i
ponti disolfuro tagliandoli. In questo modo le proteine tendono ad avere
lo stesso rapporto carica-massa e la stessa forma: infatti, si dissociano in
subunità acquisendo una conformazione a bastoncino, in cui il diametro
è costante, mentre la lunghezza varia in rapporto al peso molecolare, per
cui la separazione elettroforetica avverrà sulla base della loro massa. Il
peso molecolare può essere determinato comparando la mobilità
elettroforetica di una data proteina con la mobilità di proteine note usate
come markers: il logaritmo del peso molecolare è linearmente correlato
con la mobilità relativa. La densità delle maglie del gel varia a seconda
delle concentrazioni di acrilamide e del rapporto tra il monomero ed il
suo dimero che al momento della polimerizzazione forma dei legami
trasversali. Per separare le nostre proteine abbiamo usato un gel di
poliacrilamide secondo la tecnica descritta da Laemmli. Il gel è costituito
in realtà da due tipi di gel: stacking gel e separating gel. Il primo serve a
far arrivare le proteine alla stessa altezza; il secondo, le cui maglie
variano a seconda del tipo di proteine da separare, è il vero gel di
separazione. Un volume di estratto proteico è stato mescolato a metà
volume di "Laemmli sample buffer" (Tris HCl 0,25 M pH 6,8, SDS
20%, glicerolo 10%, 2-beta-mercaptoetanolo 5%, blu di bromofenolo
per favorire l'azione dell'SDS e del 2b-mercaptoetanolo, sono stati fatti
raffreddare e caricati sul gel. Al termine della corsa, la massa delle
proteine è determinata per confronto con la relativa mobilità delle
proteine standard.
2.4 Immunoblotting
Le proteine sono state trasferite dal gel alla nitrocellulosa mediante
"Western blotting". Il foglio di nitrocellulosa è stato posto a contatto con
il gel in un tampone di trasferimento (blotting buffer: Tris 50 mM,
glicina 4 mM, metanolo 20%) ed è stata effettuata una seconda
elettroforesi perpendicolare al gel (50 mA costanti per 2 ore). Al termine
dell'elettroblotting, l'avvenuto trasferimento delle proteine su
nitrocellulosa è stato controllato mediante la colorazione a base di Rosso
Ponceau. Quindi la nitrocellulosa è stata tagliata a strisce di 5 mm di
spessore e la residua capacità di assorbimento del supporto è stata
saturata con 5% latte in polvere magro in TBS 1X (Tris 10 mM, NaCl
150 mM pH 7,4). Lo stesso tampone è stata usato per diluire i sieri o gli
anticorpi purificati ed il secondo anticorpo marcato. Le strisce di
CM e con sieri di soggetti di controllo diluiti 1/250 in TBS, 5% FCS,
0.05% Tween-20 per tutta la notte a + 4 °C, in agitazione.
Al termine del periodo di incubazione sono stati effettuati tre lavaggi con
TBS 0.1% Tween-20 (T-TBS) e le strisce sono state incubate con un
anticorpo anti-human IgG marcato con Perossidasi di Rafano e poste in
agitazione a RT per 3 ore.
2.5 Chemiluminescenza
L'avvenuta reazione è stata evidenziata mediante chemiluminescenza
incubando le strisce con un substrato a base di luminolo e acquisendo la
luminescenza emessa mediante una fotocamera digitale (sistema di
acquisizione dell'immagine Versadoc 1000 - Biorad)
In ogni esperimento, oltre ai controlli negativi è stato inserito anche un
controllo positivo costituito da un anticorpo monoclonale
anti-alfa-enolasi.
La positività dei sieri è stata ottenuta grazie al confronto con la reattività
Risultati
3.1 Analisi della casistica clinica
Sono stati esaminati i dati clinici di un gruppo di 100 pazienti con
diagnosi di crioglobulinemia mista e positività per il virus HCV.
La distribuzione per sesso è la seguente:
maschi : 15% femmine : 85%
E’ stata fatta quindi una distribuzione dei pazienti in base agli elementi
clinici predominanti nel decorso della malattia.
Gli elementi presi in esame sono i seguenti :
- porpora - astenia - artralgie/artrite - interessamento epatico - interessamento renale - ipertensione arteriosa
- interessamento del sistema nervoso periferico (parestesie/disestesie)
- sindrome sicca
- fenomeno di Raynaud
- interessamento tiroideo
- ulcere agli arti inferiori
- linfoproliferazione/linfoma
I risultati ottenuti sono riportati nel grafico sottostante.
83 66 74 70 26 58 65 46 23 15 0 10 20 30 40 50 60 70 80 90 porpora astenia artralgie fegato rene ipertensione SNP s.sicca f.Raynaud tiroide
Dal grafico si può dedurre che l’elemento clinico predominante nella
rappresentato il segno d’esordio più frequente assieme alle artralgie e
all’astenia configurando la classica triade nella metà dei pazienti.
Molto importante è l’interessamento epatico che ricorre in circa il 70%
dei pazienti. In 54 pazienti, i valori di transaminasi sono pari al doppio
del normale; in 16 i valori di transaminasi sono 3-4 volte maggiori
rispetto al normale.
In 19 pazienti è stata eseguita una biopsia epatica che ha dimostrato
epatite cronica persistente in 12, cronica attiva in 5 e cirrosi in 2.
Ben rappresentato è anche l’interessamento del sistema nervoso
periferico (65%) che si presenta clinicamente come parestesie soprattutto
a mani e piedi. Nella maggior parte dei casi risulta confermato dalla
positività dello studio di velocità di conduzione del nervo. E’
prevalentemente se non esclusivamente la componente sensitiva del
nervo ad essere coinvolta.
In circa un quarto dei pazienti (22/100), si ha un coinvolgimento renale
più o meno importante.
Nell’interessamento renale, sono stati inclusi i pazienti con valori di
I valori di creatininemia si attestano in un range tra 1.4 mg % e 3.1 mg%
mentre i valori della proteinuria nelle 24 ore tra 0.2 g e 1.4 g. In 4
pazienti è stata eseguita biopsia renale che ha dimostrato una
glomerulonefrite membranoproliferativa.
Da non sottovalutare inoltre è la percentuale (58%) dei pazienti con
ipertensione arteriosa. Quest’ultima può far parte del quadro della
nefropatia oppure essere un’entità indipendente dall’interessamento
renale.
E’ stata anche indagata l’associazione con due patologie particolarmente
frequenti nel campo dell’immunologia clinica: la sindrome sicca ed il
fenomeno di Raynaud.
La sindrome sicca si presenta in una buona percentuale (46%) di pazienti
mentre il fenomeno di Raynaud è più scarsamente rappresentato (23%).
Nel coinvolgimento tiroideo, sono state riportate le seguenti patologie :
- gozzo multinodulare : 8/15 - nodulo tiroideo solitario : 3/15 - tiroidite di Hashimoto : 2/15 - ipotiroidismo : 2/15
E’ stata esaminata inoltre la presenza di altre manifestazioni cliniche
come le ulcere (localizzate prevalentemente agli arti inferiori), artriti,
linfoproliferazione fino ad un vero e proprio linfoma.
Le ulcere sono state riportate in 15 pazienti, segni di franca artrite in 6
pazienti, segni di linfoproliferazione in 3 pazienti mentre 7 pazienti
hanno sviluppato un linfoma nel decorso della malattia.
Nel gruppo di pazienti che hanno sviluppato un linfoma, si è trattato di
linfoma Non Hodgkin a basso grado e in un caso di linfoma cutaneo.
3.2 Ricerca di anticorpi anti-enolasi
Abbiamo misurato gli anticorpi anti-alfa enolasi nei sieri di 22 dei 100
pazienti mediante immunoblot su un estratto di rene umano e su
alfa-enolasi ricombinante.
Complessivamente sono risultati positivi 10/22 sieri (45.4%).
Dei 10 sieri positivi per anti-enolasi, 1 reagiva sia con l’enolasi da
estratto renale sia con l’enolasi ricombinante, 4 solo con l’enolasi da
In 6/22 pazienti era presente interessamento renale al momento del
prelievo; 4/6 pazienti hanno anticorpi anti-alfa enolasi.
Anticorpi anti-enolasi sono presenti inoltre in 6 dei 16 senza
interessamento renale. Non esiste quindi associazione tra presenza di
anticorpi anti-enolasi e coinvolgimento renale (χ2 = 1.49, p>0.05)
Per valutare se potesse esistere associazione tra coinvolgimento renale e
forma di enolasi riconosciuta (ricombinante vs. estrattiva) abbiamo
suddiviso ulteriormente i pazienti.
Dei 4 con nefrite ed anticorpi anti-enolasi, 2 reagivano con l’alfa enolasi
ricombinante, 1 con l’enolasi da rene ed 1 con entrambe. Dei 6 pazienti
senza nefrite, 3 riconoscevano l’enolasi ricombinante e 3 l’enolasi da
rene.
Tali risultati suggeriscono che non c’è associazione tra presenza di
nefrite e la forma di enolasi riconosciuta dagli anticorpi.
Di interesse appare, invece, la possibile associazione con forme
linfoproliferative: 3/22 pazienti presi in esame risultavano affetti da
linfoma e tutti presentavano anticorpi anti-alfa enolasi. La bassa
ma i risultati ottenuti suggeriscono un’associazione, da confermare con
Discussione
La casistica di CM da noi studiata è paragonabile, dal punto di vista
epidemiologico e per quanto concerne il tipo e la frequenza
dell’interessamento d’organo e delle differenti manifestazioni cliniche
con quanto riportato in letteratura.
L’incidenza della porpora, delle artralgie, dell’interessamento epatico,
dell’interessamento del sistema nervoso e l’associazione con la sindrome
sicca ed il fenomeno di Raynaud sono del tutto simili a quanto descritto
in altri lavori in cui la numerosità dei pazienti sia simile. Leggermente
inferiore appare invece la frequenza di coinvolgimento renale e la
prevalenza di linfoma.
Per quanto riguarda gli aspetti sierologici, alla fine degli anni ’90 è stata
descritta la presenza in sieri di pazienti con CM di anticorpi anti-alfa
enolasi. Mediante esperimenti di immunoblot su estratti tissutali di rene,
tali anticorpi risultarono presenti nel 30% dei pazienti con CM ed
interessamento renale, mentre erano assenti nei pazienti con CM senza
I risultati ottenuti in questo studio, effettuato su un gruppo indipendente
di pazienti, differiscono dai risultati del lavoro precedente sotto diversi
punti di vista.
La frequenza degli anticorpi anti-enolasi è in questo studio molto più
elevata (45% vs 18%): questo risultato è in parte dovuto all'utilizzo
dell'enolasi ricombinante, non impiegata in precedenza. Alcuni sieri
reagiscono infatti con l'enolasi ricombinante ma non con quella estratta
da tessuto. E' quindi evidente che gli epitopi presenti sulle due molecole
sono almeno in parte distinti.
Le molecole ricombinanti prodotte nei batteri, come l'enolasi
ricombinante impiegata in questo studio, non contengono le modifiche
post-traslazionali presenti sulle proteine "naturali"; possono quindi
esprimere epitopi, non tutti necessariamente lineari ma comunque
dipendenti dalla struttura primaria della proteina, non mascherati dalle
modifiche post-traslazionali.
L'enolasi estratta da tessuti porta invece una serie di queste modifiche
che danno origine a più isoforme (5-7 a seconda dei tessuti) con uguale
peso molecolare e differente punto isoelettrico. La natura delle
modifiche post-traslazionali che generano queste isoforme dell'enolasi
non è ancora stata stabilita, ma è noto che anticorpi presenti nei sieri di
Studi preliminari indicano che le quantità relative delle varie isoforme
differiscono da soggetto a soggetto: l'uso di tessuto renale di altro
donatore potrebbe avere quindi influenzato il risultato del test,
consentendo di determinare anticorpi in un numero di pazienti più
elevato. Gli anticorpi che sono stati misurati sono però differenti anche
dal punto di vista qualitativo, poiché in questo studio non è stata trovata
una correlazione fra anticorpi anti-enolasi e danno renale. Ulteriori studi
sono quindi necessari per meglio caratterizzare la specificità di questi
anticorpi e sviluppare metodi semplici e riproducibili per la loro misura.
Di interesse appare l'associazione fra presenza di anticorpi anti-enolasi e
malattia linfoproliferativa, che deve essere confermata in una casistica
più ampia di pazienti. Studi di follow-up sarebbero di estremo interesse,
per stabilire se la comparsa di questi anticorpi è temporalmente legata a
segni di linfoproliferazione. La produzione di una nuova specificità
anticorpale potrebbe essere l'espressione di un'attivazione policlonale (se
associata all'aumento di titolo di altri anticorpi) o invece essere
dipendente dall'espansione dei cloni neoplastici.
Nel complesso, possiamo quindi concludere che la determinazione degli
autoanticorpi anti-alfa enolasi può essere utile nel follow-up di pazienti
reumatoide. Ulteriori studi sono però necessari per chiarirne il valore
Bibliografia
1. Ferri C, Zignego A L, Pileri S A. Cryoglobulins. J Clin Pathol. 2002;55:4-13
2. Wintrobe M, Buell M. Hyperproteinemia associated with multiple
myeloma. With report of a case in wich an extraordinary
hyperproteinemia was associted with thrombosis of the retinal veins and
symptoms suggesting Raynaud’s disease. Bulletin of the John Hopkins
Hospital. 1933;52:156-65
3. Brouet JC, Clouvel JP, Danon F, et al. Biologic and clinical significance of cryoglobulins. Am J Med 1974;57:775–88
4. Meltzer M, Franklin EC, Elias K et al. Cryoglobulinemia. A clinical and laboratory study II. Cryoglobulins with rheumatoid factor
activity. Am J Med. 1966;40:837-56
cryoglobulinemia. Diagnostic and therapeutic considerations. Clin Rev
in Allergy and Immunol 16: 249-264, 1998
6. Dammacco F, Sansonno D, Piccoli C, et al. The cryoglobulins: an overview. Eur J Clin Invest 2001; 31(7): 628-38
7. Abel G, Zhang QX, Agnello V. Hepatitis C virus infection in type
II mixed cryoglobulinemia. Arthritis Rheum 1993 Oct; 36(10): 1341-9
8. Ferri C, and Zignego AL. Relation between infection and autoimmunity in mixed cryoglobulinemia. Curr. Opin. Rheumatol.
2000; 12: 53-60
9. Zignego AL, Ferri C, Giannelli F et al. Prevalence of bcl-2 rearrangement in patients with hepatitis C virus-related mixed
cryoglobulinemia with or without B-cell lymphoma. Ann Med
2002;137(7):571-82
10.Gorevic PD. Connective Tissue Disease associated with other
Arthritis and Allied Conditions: A Textbook of Rheumatology. 13th
ed. Philadelphia, Pa: Lippincott Williams & Wilkins; 1997: 1572-8.
11.Weinberger A, Berliner S, Pinkhas J. Articular manifestations of
essential cryoglobulinemia. Semin Arthritis Rheum 1981 Feb; 10(3):
224-9
12.Beddhu S, Bastacky S, Johnson JP. The clinical and morphologic spectrum of renal cryoglobulinemia. Medicine (Baltimore) 2002 Sep;
81(5): 398-409
13.Migliorini P, Pratesi F, Bongiorni F, et al. The targets of nephritogenic antibodies in systemic autoimmune disorders.
Autoimmun Rev 2002; 1(3): 168-73
14.Gemignani F, Pavesi G, Fiocchi A, et al. Peripheral neuropathy in essential mixed cryoglobulinaemia. J Neurol Neurosurg Psychiatry 1992
Feb; 55(2): 116-20
15.Invernizzi F, Pioltelli P, Cattaneo R, et al. A long-term follow-up study in essential cryoglobulinemia. Acta Haematol 1979; 61(2): 93-9
16.La Civita L, Zignego AL, Monti M, et al. Mixed cryoglobulinemia as a possible preneoplastic disorder. Arthritis Rheum 1995 Dec; 38(12):
1859-60
17.Bertorelli G, Pesci A, Manganelli P, et al. Subclinical pulmonary involvement in essential mixed cryoglobulinemia assessed by
bronchoalveolar lavage. Chest 1991 Nov; 100(5): 1478-9
18.Bombardieri S, Paoletti P, Ferri C, et al. Lung involvement in
essential mixed cryoglobulinemia. Am J Med 1979 May; 66(5): 748-56
19.Bonomo L, Casato M, Afeltra A, et al. Treatment of idiopathis mixed cryoglobulinemia with alfainterferon. Am J Med 1987;83:726-31
20.Ferri C, Marzo E, Longobardo G, et al. Alpha -interferon in mixed cryoglobulinemia patients: a randomized crossover controlled trial.