1
INTRODUZIONE
La sempre maggiore diffusione di tecniche diagnostiche e terapeutiche di tipo invasivo e la loro estensione anche a pazienti non collaboranti, ha comportato negli ultimi anni il moltiplicarsi di richieste di intervento anestesiologico anche al di fuori dei reparti operatori (Non Operating Room Anaesthesia N.O.R.A.).
Sempre più frequentemente l’anestesista è chiamato a prestare la propria opera in radiologia, pronto soccorso, sala travaglio, ambulatori di endoscopia, stanze di degenza ecc..per eseguire uno spettro di prestazioni che spazia dalla semplice ansiolisi sino all’anestesia generale.
Lo standard di cura e di sicurezza per il paziente deve essere garantito sia che la prestazione venga effettuata nel blocco operatorio, che in sedi inusuali.
Per questo motivo il Gruppo di Studio SIAARTI per la Sicurezza in Anestesia e Terapia Intensiva ha ritenuto opportuno elaborare un documento con lo scopo di fornire ad anestesisti e rianimatori uno strumento utile alla realizzazione di attività anestesiologiche in aree convenzionalmente non deputate all’esecuzione di tali procedure,in analogia con quanto effettuato da altre società scientifiche internazionali.
CAPITOLO 1
ANESTESIA E SEDAZIONE FUORI DALLA SALA
OPERATORIA
(NON
OPERATING
ROOM
ANESTHESIA)
1.1 Livelli di sedazioneIl termine “sedazione/analgesia” identifica una condizione farmacologicamente indotta di ansiolisi, amnesia, analgesia e attenuazione del disagio procurato da una procedura invasiva, in assenza di depressione respiratoria e cardiovascolare.
E’ possibile individuare vari livelli di sedazione in base alla capacità di mantenere l’integrità dei riflessi protettivi delle vie aeree e della funzione respiratoria, valutando la risposta del paziente al contatto verbale e agli stimoli nocicettivi.
• Sedazione conscia o vigile: la risposta ai comandi verbali è presente
e congrua. I riflessi protettivi delle vie aeree sono preservati e la funzione respiratoria è indenne.
• Sedazione profonda: la risposta ai comandi verbali è torpida,
incongrua o assente, ma è evocabile quella riflessa agli stimoli nocicettivi. I riflessi protettivi delle vie aeree sono inefficienti e la funzione respiratoria compromessa.
• Anestesia generale:non è evocabile neppure la risposta riflessa agli
stimoli nocicettivi. I riflessi protettivi delle vie aeree sono assenti e la funzione respiratoria compromessa.
3 Nel 2001 la Joint Commission on Accreditation of Healthcare Organizations JACHO, che ha incluso la sedazione nei criteri di accreditamento nelle strutture sanitarie, ha usato le seguenti definizioni:
• Minimal sedation (anxiolysis)
• Moderate sedation/analgesia
• Deep sedation (può richiedere intervento sulle vie aeree)
• General anestesia
Mentre l’ansiolisi e la sedazione/analgesia possono essere somministrate dai non anestesisti, la sedazione profonda e l’anestesia generale sono appannaggio dell’anestesista.
La sedazione comunque è un continum verso l’anestesia e in alcuni casi, anche se le dosi di sedativo somministrate sono nel range terapeutico, il paziente può andare incontro lentamente verso l’anestesia generale, con tutti i rischi che ne conseguono se a gestirlo non sono anestesisti.
1.2 Rischio, sicurezza e mortalità
Negli ultimi dieci anni (1998-2007) il numero delle procedure effettuate al di fuori della sala operatoria è raddoppiato,quindi identificarne i rischi è molto importante sia per prevenire gli eventi avversi, che per minimizzare il loro impatto.
Per questo motivo sono stati sviluppati dei protocolli che forniscono informazioni e notifiche a riguardo e su diversi fronti:
• Ambiente: è estremamente importante che sia adeguato ad accogliere sia i macchinari che l’equipe per evitare un sovraffollamento in stanze con spazi limitati in modo che la procedura non venga ostacolata o resa difficoltosa in nessun caso.
• Equipment: i monitors necessari devono registrare l’elettrocardiogramma, la saturazione di ossigeno, la pressione
sanguigna, end-tidal CO2, la frequenza cardiaca e respiratoria. Altrettanto necessari sono le apparecchiature per l’accesso venoso, quelle per la gestione delle vie respiratorie e i farmaci anestetici.
• Competenza dell’equipe: il personale che svolge le attività ambulatoriali ha generalmente minor familiarità con i pazienti anestetizzati. Per questo è importante, specialmente in situazioni di emergenza, un’adeguata preparazione e competenza di tutta l’equipe.
• Screening pre-procedura: la valutazione anestesiologica è la stessa alla quale vengono sottoposti i pazienti di chirurgia generale, perché problemi o sindromi associate all’anestesia richiedono un’accurata valutazione.
• Ipotermia: molti ambienti nei quali viene effettuata l’anestesia sono dotati di impianti di condizionamento,per evitare il surriscaldamento dei macchinari. Se non vengono prese precauzioni,il risultato è una seria ipotermia. Ciò comunque si verifica maggiormante nei pazienti pediatrici e per procedure prolungate (più di un’ora).
• Scelta della tecnica e dell’anestetico: nella scelta di entrambi è importante tenere in considerazione i seguenti punti:
v la maggior parte delle procedure diagnostiche sono brevi, inoltre la rapidità d’azione del farmaco è richiesta.
v La maggior parte delle procedure non evoca dolore né durante né dopo l’esame. Pertanto solo raramente vengono utilizzati oppioidi potenti con una più lunga durata d’azione.
v Farmaci che inducono il blocco neuromuscolare sono richiesti solo nell’intubazione endotracheale; comunque si preferisce usare quelli a breve durata d’azione.
v L’associazione di patologie è il più importante fattore nella scelta della tecnica anestesiologica.
5 Tutti questi fattori contribuiscono al mantenimento di una buona qualità della procedura, rendendo facilmente intuibile come in passato sia per una minor avanguardia dei macchinari e degli ambienti,sia per le limitate conoscenze e l’inesperienza manuale,le complicanze e il tasso di mortalità fossero maggiori.
Nel 2002 Kawashima et al. in uno studio riguardo le procedure effettuate al di fuori della sala operatoria, ha riportato una mortilità di 0.7 su 10.000 pazienti. L’incidenza degli arresti cardiaci attribuibili all’anestesia rappresentano la metà delle complicazioni e il 65% delle morti che si verificano entro la prima settimana. Le cause principali sono rappresentate dall’overdose da farmaci, da un uso improprio dei farmaci e dallo scambio di siringhe conteneti farmaci differenti.
1.3 Morbidità
La morbidità correlata alla sedazione o all’anestesia eseguita in sedi diverse dalla sala operatoria non sono ancora state studiate in maniera approfondita, ma rappresentato un problema rilevante a causa dell’aumentata necessità di somministrare sedazione/analgesia in luoghi disagiati per un’ampia gamma di procedure diagnostiche e operatorie (endoscopia, radiologia, risonanza magnetica) e per la mancanza di monitoraggio, inadeguato addestramento del personale e carenza dello staff.
Molte sono le complicanze che possono sorgere con NORA: ipotermia, aspirazione del contenuto gastrico, ipovolemia, difficoltà respiratorie, anafilassi, nausea e vomito,dolore, effetto della sedazione sulla perforazione intesinale durante la colonscopia.
Sebbene la lista delle complicazioni sia illimitata, è possibile selezionare le problematiche che ricorrono più frequentemente e che richiedono una gestione leggermente diversa.
Aspirazione del contenuto gastrico
I pazienti che si sottopongono alla colonscopia in sedazione devono bere da 2 a 4 litri di un preparato fino a poche ore prima dell’anestesia, risultando così a rischio, anche se non ben quantificato, di aspirazione del contenuto gastrico.
Ipovolemia
I pazienti preparati per la colonscopia sono sottoposti ad una dieta restrittiva e a purghe ripetute nei giorni precedenti all’esame;in questi casi il potenziale rischio di una severa ipotensione in seguito all’introduzione degli anestetici che hanno effetti vasodilatatori o un’azione depressiva sul cuore,possono essere anticipati ed evitati mediante prevenzione. Una lenta infusione del farmaco, insieme alla reidratazione, è generamlmente sufficiente e consigliata per mantenere una buona idratazione.
Gestione delle vie aeree
I potenziali problemi riguardano un’inefficiente valutazione preoperativa delle vie aeree, l’inesperienza del personale nella gestione di situazioni critiche e l’assenza della strumentazione necessaria come il laringoscopio,broncoscopio,ecc.
L’identificazione del rischio e la cautela nella gestione delle vie aeree è fondamentale, inoltre qualsiasi anestesista deve essere preparato ad attuare una procedura alternativa nel caso che l’intubazione o la ventilazione fallisca.
Allergie e shock anafilattico
le reazioni ai farmaci sono ben documentate e i livelli di gravità sono diversi: si passa da lievi reazioni avverse che si possono manifestare mediante vasodilatazione (3% dei casi),a severe allergie/reazioni anafilattiche che però possono essere talvolta difficilmente diagnosticate per la simultanea presenza di fattori confondenti, come il ritardo dell’evento stesso, la mancanza di segni
7 di reazione allergica acuta (broncospasmo, rilascio di istamina)che rendono il riconoscimento dello shock anafilattico molto difficile. I pazienti con storia di allergie o atopia dovrebbero ricevere una profilassi con antiistaminici e cortisone, anche se non è scientificamente provato che questa pratica sia realmente protettiva per il paziente. Inoltre l’uso di questi farmaci può minimizzare la severità dell’anafilassi e mascherare la presenza dei segni rivelatori. Quindi è bene utilizzarli solo come trattamento precoce dell’anafilassi.
Altri incidenti riportati riguardano lo scambio di siringhe come nel caso dell’utilizzo di KCl al posto di NaCl; questo conferma ulteriormente la necessità di un’equipe adeguatamente preparata e competente.
Nausea e vomito post-procedura
Questo fattore è molto importante e incisivo sulla morbidità, perché diminuisce la soddisfazione del paziente e aumenta il tempo di degenza.
Nella quasi totalità dei casi l’anestesia intravenosa viene scelta a discapito degli agenti anestetici inalatori. L’associazione di un’adeguata idratazione, un’efficace analgesia e l’identificazione di pazienti ad alto rischio (sesso femminile, storia di nausea e vomito postoperatori, non fumatori) riducono considerevolmente l’incidenza di questo parametro.
Se però questi eventi si vengono a verificare, deve essere instaurata una terapia con antiemetici. Inoltre se un paziente è considerato ad alto rischio, l’uso profilattico di un antiemetico può risultare appropriato.
Awareness: l’incidenza dell’awreness è dello 0.1-0.2%.
Dolore: le procedure svolte in NORA generalmente non risultano nel postoperatorio essere caratterizzate dal dolore. Gli sviluppi sulla fisiopatologia del dolore acuto hanno permesso di incrementare il numero di strategie a nostra
disposizione sulla gestione dei pazienti ambulatoriali e di adattarle ad ognuno di loro, al fine di ottenere un ottimo e individuale controllo del dolore.
Perforazione intestinale durante colonscopia: l’incidenza totale della perforazione intestinale come complicanza della colonscopia è dello 0.1%. Quando l’esame viene eseguito da un chirurgo esperto, l’anestesia non incrementa il rischio di perforazione intestinale.
1.4 Ruolo dell’anestesista
NORA richiede spaciali abilità e attitudini, sia tecniche che non; infatti è importante anche sottolineare le altre qualità, tra cui i compiti gestazionali, la coordinazione e capacità del team-working, l’awareness e la responsabilità decisionale.
Per questa necessità di riconoscere sotto un’unica figura tutti i requisiti sopra elencati, molti centri hanno adottato la terminologia di “sedationist”.
In Italia questo compito è spesso affidato al medico che esegue l’esame o al personale infermieristico,con eccellenti risultati sulla sicurezza e qualità della procedura, che però risulta essere incrementata grazie all’utilizzo della tecnica anestesiologica. Dato che questa è una disciplina che richiede un costante monitoraggio da parte di personale esperto, la sicurezza deriva proprio dall’alto livello di assistenza ed competenza dell’equipe.
Evidenze cliniche supportano la tesi che il team di anestesisti garantisca una maggiore sicurezza e un più efficace costo del metodo di praticare questo genere di anestesia. Infatti sono stati riscontrati decessi e fallimenti nei casi in cui l’anestesista non era presente durante l’esecuzione dell’esame.
Dato che le condizioni dei pazienti possono rapidamente cambiare, evolvere in complicanze e divenire instabili,ogni singola analgo-sedazione praticata in NORA dovrebbe essere quindi gestita dall’anestestista.
9 1.5 Aumento della domanda in vari settori
Quando le prime linee guida riguardo la sedazione in NORA furono pubblicate nel 1994 da un gruppo di ricercatori dell’università di Boston, queste procedure erano essenzialmente limitate alle semplici endoscopie e ai cateterismi cardiaci, e venivano raggruppate sotto il nome di “sedazione cosciente”.
In breve tempo gli ambiti di queste procedure si sono progressivamente espansi.
Con l’aumento della domanda (come per lo screening colonscopico al posto della sigmoidoscopia) da parte dei pazienti che spesso devono sottoporsi a valutazione medica, gli anestesisti sono richiesti per offrire il loro servizio anche lontano dalla sala operatoria.
I dipartimenti presso i quali si effettuano procedure in sedazione al di fuori della sala oparatoria sono vari.
La cardiologia (angiogramma, cardioversione, chiusura dei difetti del setto atriale ecc..), la radiologia interventistica (tecniche di embolizzazione per il trattamento di emorragie sub aracnoidee e shunt porto-sistemici, inserzione di stent endovascolari ecc..), la neuroradiologia (angioplastiche cerebrali, embolizzazione di malformazioni vascolari o di aneurismi), la diagnostica per immagini (MRI e TC sono spesso effettuate in pazienti pediatrici o pazienti in condizioni cririche o ancora in soggetti claustrofobici) e l’endoscopia gastrointestinale( EGDS, ERCP e colonscopie).
1.6 Linee guida nazionali e internazionali nell’endoscopia digestiva
La Società Italiana di Endoscopia Digestiva (SIED), in collaborazione con anestesisti, gastroenterologi endoscopisti, esperti e consulenti per la metodologia, ha creato le linee guida per la sedazione in endoscopia digestiva. Le raccomandazioni di questa linea guida (revisione gennaio 2006 delle linee guida per la sedazione cosciente e il monitoraggio durante l’endoscopia
gastrointestinale; Gastrointestinal Endoscopy 2003) sono quindi state elaborate da un gruppo di lavoro multidisciplinare che ha condotto una ricerca sistematica in letteratura utilizzando una scala di grading (tabella 1) e confrontando le raccomandazioni con la pratica corrente.
Questa ricerca è stata effettuata utilizzando le banche dati Medline ed Embase (letteratura primaria) e Cochrane e DARE (revisioni sistematiche). Le linee guida sono state eleborate grazie alla banca dati della National Guidelines Clearinghouse e produttori di Linee Guida quali CMA e SIGN. E’ stata poi condotta una ricerca sistematica di linee guida prodotte da Società Scientifiche. Per l’esecuzione delle procedure endoscopiche dell’apparato digerente in sedazione esistono Linee Guida delle Società Scientifiche di Endoscopia Digestiva di altri Paesi europei e dell’American Society for Gastrointestinal Endoscopy (ASGE).
La valutazione del paziente deve precedere la somministrazione intravenosa della sedazione al fine di identificare quali aspetti della storia clinica potrebbero influire sul risultato dell’indagine endoscopica.
Gli elementi oggetto di valutazione sono: patologie cardiache e polmonari; alterazioni neurologiche; stridore, russamento o apnea notturna; reazioni
Tabella 1
Livello 1 Studi clinici randomizzati controllati e/o loro revisioni sistematiche
Livello 2 Trial prospettici con o senza controlli con ampie casistiche
Livello 3 Case report, parere di esperti (consensus conference, survey dalle Società
11 avverse alla sedazione o all’anestesia; medicinali assunti, allergie a farmaci o alimentari; abuso di droghe o alcool. In aggiunta dobbiamo tener conto della comorbidità, che viene classificata secondo la American Society for Anesthesiology (ASA) in base allo stato di salute del paziente (tabella 2).
I pazienti di classe I-III sono candidati appropriati alla sedazione endoscopica. Le classi IV e V invece, racchiudono pazienti che necessitano di un maggior grado di sedazione, di procedure endoscopiche in regime di emergenza o procedure endoscopiche complesse (come per es. ERCP, endoscopie con ultrasuoni), pazienti con reazioni avverse alla sedazione o che vi rispondono inadeguatamente alla somministrazione, pazienti che abusano di alcool o di altre sostanze.
Tabella 2 ASA classification
Classe I Nessuna alterazione organica, biochimica, psichiatrica
Classe II Modesto disturbo sistemico che non limita le attività del paziente (ipertensione,
diabete controllato, cardiopatia in compenso, obesità moderata)
Classe III Grave malattia sistemica che limita le attività del paziente (ipetensione, diabete
non controllato, IRC, IMA recente 3mesi) Classe IV Grave malattia che pregiudica la sopravvi_
venza del paziente (insufficienza cardiaca congestizia, stadio
uremico dell’insufficienza renale) Classe V Paziente moribondo con considerevole
rischio di morte entro 24h Classe E Emergency status
Obiettivi della sedazione in endoscopia
Ø Abolizione/riduzione del disagio (discomfort) del paziente
Ø Garanzia di una maggiore sicurezza per il paziente in relazione alla protezione analgesica
Ø Garanzia di una più facile e accurata esecuzione della procedura endoscopica
Chi sedare
E’ raccomandata la sedazione e/o analgesia a seconda delle caratteristiche dei pazienti o dei fattori di rischio:
Ø pazienti i età pediatrica in cui è decisivo ottenere una collaborazione efficace e un minimo disagio per traumatizzare il piccolo paziente il meno possibile
Ø pazienti in età avanzata in cui può essere necessario valutare l’opportunità di una protezione analgesica al fine di evitare possibili complicanze algomadiate
Ø pazienti in età intermedia in cui è necessario valutare caso per caso il livello di ansia e la capacità soggettiva di autocontrollo del paziente Ø pazienti in cui sono compromesse le funzioni della vita di relazione
(malattie psichiatriche, sindrome di Down, cerebrolesi ecc.)
Ø pazienti affetti da stati morbosi concomitanti quali: grande obesità, importanti cardiopatie, gravi malattie broncopolmonari, patologie neuromuscolari e anemia significativa ( 8g Hb). Tali pazienti quando vengono sottoposti a sedazione sono predisposti ad una ridotta ventilazione alveolare: è pertanto utile monitorarli attentamente.
13 Quando sedare
La sedazione è raccomandata per le seguenti procedure:
• ERCP e manovre sulle vie bili-pancreatiche
• Endoscopie pediatriche
• Endoscopie operative
• Ecoendoscopie
• Pazienti non collaboranti e ansiosi
• Tutti coloro che la richiedono
• Indagini eseguite in urgenza (per es. in caso di ematemesi in cui oltre all’insensibilità emodinamica esiste anche il rischio di ab-ingestis)
• Pan colonscopie diagnostiche
La sedazione è invece raccomandata ma non indispensabile.
• EGDS diagnostiche (soprattutto se previste di lunga durata) Valutazione del paziente
E’ necessaria una valutazione complessiva del paziente da parte del personale sanitario che lo accoglie in relazione all’impiego di farmaci depressori di funzioni vitali, in modo da acquisire elementi utili a ridurre l’incidenza di eventi avversi.
Prima di procedere alla sedazione/analgesia, ricercare e valutare gli elementi di rilievo della storia clinica, la funzionalità dei principali organi e apparati, la tollerabilità della posizione supina durante il sonno e l’eventuale insorgenza notturna di stridore laringeo o apnea, precedenti esperienze di anestesia o di sedazione/analgesia ed eventuali effetti collaterali, le terapie farmacologiche in atto, eventuali allergie e l’uso /abuso di sostanze voluttuarie.
Durante l’esame obiettivo porre particolare attenzione allo stato delle vie aeree (dimorfismi facciali, apertura della bocca, mobilità del collo e dell’articolazione temporo-mandibolare ecc.).
Procedere alla rilevazione basale di frequenza cardiaca, pressione arteriosa sistemica e saturazione in O2.
In caso di fondato sospetto per patologie diverse da quella oggetto di indagine, procedere ad approfondimenti diagnostici, ed eventualmente richiedere le opportune consulenze.
Consenso informato
È diritto del paziente ed un dovere del medico fare in modo che l’esame a cui il paziente deve sottoporsi risulti il meno fastidioso possibile, più sicuro e più accurato perché non condizionato dal disagio derivante dagli stimoli emotivi e algici che vengono procurati durante l’esame.
Come ogni atto medico anche la pratica della sedazione/analgesia richiede una preventiva informazione del paziente sulla procedura e sugli eventuali rischi ed un successivo consenso informato.
Il consenso informato è incentrato sul rapporto Medico-Paziente.
A completamento dell’informazione è buona norma assicurarsi che il paziente sia accompagnato durante il ritorno il domicilio e che all’accompagnatore vengano fornite tutte le indicazioni utili per gestire ogni eventuale problema che si dovesse presentare.
15
CAPITOLO 2
FARMACOLOGIA DELLA SEDAZIONE
Il sedativo ideale dovrebbe assicurare livelli misurabili di ipnosi, ansiolisi, amnesia e analgesia tutto ciò in assenza di depressione cardiorespiratoria clinicamente significativa e di effetti irritativi locali.
Dovrebbe inoltre possedere un’ampia finestra terapeutica, una correlazione dose-effetto, un onset rapido e un offset compatibile con procedure ambulatoriali di breve durata.
Naturalmente un farmaco del genere non esiste, ma l’obiettivo terapeutico può essere raggiunto associando in modo sinergico farmaci diversi.
Si possono infatti associare farmaci appartenenti alla famiglia degli oppiacei (analgesici) con farmaci GABA mimetici (amnesici e ansiolitici).
Purtroppo l’associazione è sinergica anche in termini di depressione cardiorespiratoria ed il sinergismo è tanto più marcato quanto maggiore è la potenza dei farmaci utilizzati.
La potenza e la rapidità sono dipendenti dalla lipolificità; quindi chi privilegia un composto a cinetiche rapide, come Propofol e Fentanyl, perché più adatto alle esigenze gestazionali endoscopiche, mette in conto l’amplificazione dei rischi di depressione delle funzioni vitali.
La procedura può anche essere effettuata utilizzando farmaci meno potenti, come meperidina e midazolam, che garantiscono un rapporto rischio/beneficio più favorevole.
2.1 Oppiacei
La necessità di abolire il dolore e il disagio evocati dalla procedura endoscopica impone l’utilizzo di un oppiaceo.
Gli oppiacei esercitano il loro effetto farmacologico legandosi a specifici recettori che sono presenti in tutto il sistema nervoso centrale e nei tessuti periferici. La differenza di struttura chimica tra i vari agenti oppiacei, determina la differenza dei parametri farmacocinetici e dell’effetto analgesico.
Meperidina: è l’oppiaceo universalmente più utilizzato in endoscopia digestiva, in virtù di un onset relativamente graduale, assenza di effetto spastico sullo sfintere di Oddi e una più soddisfacente azione residua.
Si tratta infatti del primo oppioide si sintesi utilizzato nella pratica clinica, sintetizzato come anticolinergico.
E’ un analgesico ipnotico blandamente sedativo. Il picco di efficacia si verifica entro 10 minuti, ed esplica un effetto analgesico di durata relativamente breve, da un minimo di 30 minuti ad un massimo di 2 ore, a causa della rapida ed intensa distribuzione tissutale. Per quanto concerne le posologie, per la via di somministrazione ev il range di dose sedativa è compreso tra 0,04 e 0,08 mg/kg; quello analgesico tra 0,5 e 1 mg/kg. La diluizione del farmaco può facilitarne la somministrazione lenta.
Sebbene strutturalmente diverso dalla morfina, in dosi equipotenti (meperidina 0,1 mg/kg pari a morfina 0,01mg/kg) esercita identici effetti analgesici, depressivi respiratori ed emetici; ma essendo più liposolubile della morfina, attraversa prima la barriera ematoencefalica e, di conseguenza, la correlazione tra concentrazione plasmatica ed effetti clinici è più lineare.
Il più frequente effetto collaterale di dosi terapeutiche di meperidina è un’ipotensione ortostatica, riconducibile a interferenze con riflessi simpatici compensatori.
Sia gli effetti terapeutici che quelli collaterali sono prontamente antagonizzati dal naloxone, ma è utile tener presente che una fiala (0,4 mg) ha un’emivita di eliminazione (60/90 minuti) e una durata d’azione (circa 45 minuti) nettamente più brevi di quella dell’oppiaceo. Pertanto è possibile il reinstaurarsi della
17 depressione respiratoria, specie se impiegato in associazione con benzodiazepine (BDZ), per riduzione della frequenza respiratoria indotta dagli oppioidi; infatti è buona norma somministrare la meperidina circa 10 min prima delle BDZ.
La meperidina si differenzia dalla morfina prevalentemente per l’attività anticolinergica intrinseca e infatti la miosi è meno marcata, in virtù dell’effetto atropino-simile sullo sfintere pupillare, e determina secchezza della fauci e tachicardia.
L’effetto sedativo è meno marcato di quello della morfina, in assenza di apprezzabili modificazioni EEG, e talvolta associato a distorsioni percettive di tipo allucinatorio.
La meperidina viene metabolizzata pressoché completamente da reazioni di fase I a livello epatico. Circa il 70% della dose viene escreta con le urine sottoforma di metaboliti entro le 24 ore, con eliminazione facilitata dall’acidificazione delle urine.
La clearance è ovviamente ridotta in caso di insufficienza epatica, nel soggetto anziano e nel periodo post-operatorio.
Questo farmaco è assolutamente controindicato in pazienti sotto trattamento con I-MAO: tale reazione infatti, è causa di coma, convulsioni, iperpiressia e marcata destabilizzazione emodinamica.
Fentanyl: è un oppioide narcotico sintetico, un potente analgesico (circa mille volte più potente della meperidina).
Presenta un’alta liposolubilità e raggiunge rapidamente il proprio sito recettoriale. Il picco d’azione si ha entro 5-8 minuti, con una durata media di circa 30-45 minuti.
La dose analgesico-ipnotica è di circa 0.1 mg/kg, da somministrare in bolo lento, titolando la dose in base all’effetto. Se associata, va sempre
somministrato prima delle BDZ. Posologie ridotte anche del 50% o più, sono indicate nei pazienti anziani.
Il maggior effetto collaterale è la depressione respiratoria, che persiste più a lungo dell’effetto analgesico (almeno 2 ore) a causa di imprevedibili picchi secondari di concentrazione plasmatica.
Ad alte dosi può indurre rigidità della gabbia toracica con conseguente compromissione della pervietà delle vie aeree e della meccanica respiratoria, chiusura della glottide e bradicardia per effetto vagotonico centrale.
L’incidenza di nausea e vomito è sovrapponibile a quella degli altri oppioidi.
2.2 Benzodiazepine
Gli effetti farmacologici delle BDZ includono ansiolisi, sedazione, amnesia, anticonvulsivanti, miorilassamento e anestesia. L’effetto amnesico può persistere anche dopo che la sedazione è svanita.
Le BDZ accrescono l’attività inibitoria di un neurotrasmettitore, l’acido γ -aminobutirrico (GABA), mediante il legame al recettore GABA-A localizzato per lo più sulla membrana post-sinaptica delle cellule nervose della corteccia cerebrale.
Le proprietà farmacologiche delle varie categorie di BDZ derivano dalla loro individuale affinità è specificità di legame alle diverse sub unità del recettore GABA-A.
Midazolam: fra le BDZ è uno dei più potenti sedativi-ipnotici non analgesici e la più idonea per la sedazione in endoscopia digestiva.
Cole et al hanno esguito uno studio random a doppio-cieco, comparando midazolam e diazepam nella sedazione endoscopica. Il midazolam si è rivelato più potente e con una più rapida velocità d’azione, riducendo il tempo di induzione della sedazione di circa 2 minuti e mezzo a procedura.
19 E’ una imidazo-BDZ idrosolubile e altamente lopofilica a pH fisiologico, tanto da garantire un rapido equilibrio sangue-encefalo e una rapida ridistribuzione dal compartimento centrale a quello periferico.
L’emivita di eliminazione e la clearance sono nettamente più rapide di quelle del diazepam: rispettivamente tra le 10/15 volte minore la prima e 27 volte più rapida la seconda.
È inoltre circa 4 volte più potente del diazepam in termini sedativi, ansiolitici, amnesici, miorilassanti e anticonvulsivanti.
Può determinare agitazione paradossa nelle fasce estreme di età. Riduce il volume corrente per ostruzione meccanica sovraglottica e depressione diaframmatica; riduzione della frequenza cardiaca e della pressione arteriosa. Non produce dolore in sede di inoculo, né causa flebiti.
Il picco di azione si ha entro 5 minuti, la durata è di circa 30 minuti. La dose ipnotica è compresa tra 0.05-0.1 mg/kg e.v.
Quando è necessario per la durata della procedura, possono essere ripetuti boli di circa 1 mg per volta; il rischio maggiore però nelle sedazioni protratte è il rallentamento delle cinetiche di eliminazione del farmaco.
Il modazolam non causa episodi di risedazione, osservati invece con il diazepam e riconducibili a picchi secondari di concentrazione plasmatica, da ritorno in circolo del farmaco depositato nel compartimento periferico.
La cinetica e la potenza del farmaco coincidono con le esigenze sedative in ambito endoscopico e anestesiologico.
L’azione antisterss madiata dalle BDZ, è data dall’up-regulation dei recettori GABA-A con potenziamento del controllo inibitorio GABAergico sul sistema dopaminergico mesolimbico frontale, attivato dall’ansia e dalla paura.
Le BDZ modificano i livelli cerebrali di molti neurotrasmettitori (noradrenalina, serotonina, dopamina, acetilcolina) potendo così indurre, talvolta, anche alterazioni comportamentali di natura disinibente. Tali “reazioni paradosse”, che si manifestano con ansia, irrequietezza fino all’agitazione
psicomotoria e confusione mentale, riconoscono alcuni fattori predisponenti quali: l’appartenenza alle fasce estreme di età, personalità con tratti di ostilità, aggressività o depressione, e situazioni preesistenti di stress.
Per quanto riguarda la farmacocinetica e farmacodinamica, è opportuno ricordare l’aumento della sensibilità al farmaco correlato con l’aumentare dell’età e il prolungamento dell’emivita di eliminazione nei soggetti obesi. Il midazolam viene metabolizzato prevalentemente dal CYP3A4, principale catalizzatore di molti farmaci di uso comune (eritromicina, verapamil, nifedipina, lidocaina, cortisonici, oppioidi ecc.). Ne consegue che gli effetti sedativi possono essere più intensi per aumento della concentrazione del picco, e persistenti per riduzione della clearance in pazienti in terapia con i farmaci citati. Un aumento della biodisponibilità, oltre che un rallentamento della clearance, si riscontra anche in cirrotici scompensati; dal momento che il farmaco si lega elettivamente all’albumina, una condizione ipoalbuminica (nefropatia cronica o cirrosi scompensata) può comportare un aumento della quota libera del farmaco e quindi un maggior rischio di depressione respiratoria.
Un’ultima avvertenza riguarda l’effetto ipotensivo del midazolam: viene generalmente compensato da un modico incremento della frequenza cardiaca, riconducibile a tre distinti meccanismi.
1. Mobilizzazione di massa volemica dal territorio splacnico che ripristina il precarico;
2. Relativa preservazione del baro riflesso e/o da effetto vago litico centrale; 3. Aumento della contrattilità miocardica da attivazione simpatica riflessa.
Diazepam: sedativo-ipnotico non analgesico.
Produce ansiolisi, scarsa amnesia, ha proprietà miorilassanti e anticonvulsivanti. Causa dolore e a volte flebiti in sede di inoculo. Determina agitazione paradossa nelle fasce estreme di età. Provoca ipotensione marcata.
21 Il picco di efficacia si verifica entro 5 minuti, la durata d’azione è di circa 30 minuti. A livello epatico viene convertito in un metabolita attivo che ha clearance lenta, responsabile della relativa lunga durata d’azione.
Se necessario per la durata della procedura si possono ripete boli si 2 mg per volta.
La dose sedativa è di 1:2 rispetto al midazolam.
Il midazolam possiede rispetto al diazepam i seguenti vantaggi: 1. Versatilità delle vie di somministrazione;
2. Compatibilità di diluizione e miscelazione; 3. Maggiore potenza sedativa e amnesia;
4. Più rapida regressione del deterioramento cognitivo e mnesico.
Il midazolam è paragonabile al diazepam in termini di insorgenza e regressione degli effetti ipnotici e sedativi.
Il maggiori effetti collaterali del diazepam sono la tosse, la dispnea e la depressione respiratoria. Quest’ultima è dose-dipendente e deriva dalla depressione dei centri ventilatori in risposta all’ipossia e all’ipercapnia. Si manifesta con maggior incidenza in soggetti affetti da patologie respiratorie di base o ai quali viene somministrata una combinazione di BDZ e oppiodi.
2.3 Propofol
È un sedativo molto potente che è in uso in ambito anestesiologico da circa vent’anni e di recente sta entrando nella letteratura specialistica con discreta autorevolezza.
Si tratta di un alchil-fenolo, dotato di spiccata attività sedativa, amnesica ed ipnotica, una potenza nettamente superiore a quella delle BDZ, un onset rapido (40-60 sec), una durata d’azione che non supera i 10 minuti dopo bolo singolo, e un risveglio pronto era abbinato a recupero in tempo reale delle funzioni intellettive e del coordinamento motorio.
La dose sedativa abituale è di 0.5-0.8 mg/kg, mentre la dose ipnotica è di 1-2 mg/kg in bolo seguito da infusione continua variabile da 3-6-9 mg/kg/h.
Queste, sono caratteristiche vantaggiose per la sedazione in ambito endoscopico.
La spiccata lipofilia gli consente un immediato attraversamento delle barriere biologiche, con rapido raggiungimento di una concentrazione clinicamente efficace nei siti d’azione cerebrali. La dose ipnotica è in correlazione inversa con l’età e nel sesso maschile e maggiore che nel sesso femminile, in media da 1.7 a 2.5 mg/kg nei maschi e da 1.5 a 2 mg/kg nelle femmine.
Altre variabili farmacocinetiche, come per es. la gittata cardiaca, la massa magra, volume ematico del compartimento centrale, flusso cerebrale, terapie concomitanti e temperatura corporea possono modificare significativamente il comportamento clinico del farmaco. Importante è individuare la dose caso per caso mediante somministrazione lenta, quasi a simulare un’infusione continua, e interrompendola una volta raggiunti i segni clinici indicativi di ipnosi (perdita del contatto verbale, ipotonia muscolare, ptosi palpebrale).
Il meccanismo d’azione del propofol è simile a quello delle BDZ, potenziando il tono inibitorio GABAergico per attivazione dei recettori GABA-A.
Mentre le BDZ reclutano solo il sottotipo A dei proprio recettori con il sito di riconoscimento per le BDZ, il Propofol recluta tutti i recettori GABA-A accessibili, anche quelli sprovvisti del sito BDZ. Da ciò deriva la sua maggiore potenza. Ma deriva anche, come risvolto negativo: una finestra terapeutica (ED50/LD50) più ristretta; una più marcata depressione respiratoria e cardiovascolare; l’assenza di antagonisti specifici.
Come il midazolam, anche il Propofol è privo di effetto analgesici e pertanto richiede l’associazione con un oppiaceo nelle procedure gravate da un’apprezzabile componente algica.
È un potente depressore respiratorio, riducendo il volume corrente, il volume minuto, la capacità funzionale residua, il flusso inspiratorio medio, la
23 frequenza respiratoria e compromettendo anche il drive chimico della ventilazione.
Il Propofol possiede un’intensa attività vagotonica, riducendo la frequenza cardiaca, fino a determinare anomalie della conduzione che a volte possono esitare in asistolia. È in grado di determinare ipotensione marcata per vasodilatazione arteriolare e venulare periferica.
La potenza e la rapidità cinetica del Propofol lo rendono più rispondente del midazolam alle esigenze sedative in ambito endoscopico; sembra anche garantire un risveglio più rapido, una migliore tollerabilità dello strumento e una minore persistenza di amnesia e compromissione psicomotoria. Però proprio la sua potenza, gli effetti depressivi respiratori e cardiovascolari che ne conseguono e l’impossibilità di interromperne gli effetti con un antagonista, lo rendono meno maneggevole e di competenza dell’anestesista.
Propofol: utilizzo singolo e associazione con altri farmaci
L’associazione con piccole dosi di farmaci che possiedono gli stessi effetti desiderati, rende possibile massimizzare l’azione terapeutica di ognuno, minimizzando contemporaneamente le probabili reazioni avverse dose-dipendenti.
Questo principio può essere ovviamente applicato anche alle procedure endoscopiche. Per esempio, quando il Propofol viene utilizzato da solo nella sedazione endoscopica, sono richieste alte dosi per produrre una sedazione profonda, e conseguentemente gli effetti collaterali dose-dipendenti come l’ipotensione, ipoventilazione o bradicardia, sono relativamente frequenti. Al contrario, quando il Propofol viene somministrato insieme a basse dosi di oppiodi e BDZ, l’analgesia e l’amnesia possono realizzarsi con dosi sub ipnotiche di propofol,eliminando la necessità di indurre una sedazione profonda. Inoltre questa associazione offre i benefici propofol-mediati mentre riduce il rischio rapido e irreversibile della oversedation.
I protocolli pubblicati relativi all’uso combinato del Propofol con altri agenti, include una dose pre-induttiva con un oppioide, una BDZ o entrambi:
Ø Fentanyl: 25-75 µg; Ø Meperidina: 25-50 mg;
Ø BDZ (midazolam): 0.5-2.5 m
La somministrazione di una dose induttiva di Propofol pari a 5-15 mg, seguita da boli aggiuntivi di 5-15 mg determinano il raggiungimento dell’effetto. La dose cumulativa media di propofol utilizzata durante le colonscopie è di circa 65-100 mg.
Tra i gastroenterologi c’è la diffusa convinzione che il Propofol offre una migliore sedazione nelle endoscopie rispetto alla combinazione oppioide/benzodiazepine.
I suoi benefici includono una superiorità in termini di tempistica e brevità del ricovero, un migliore effetto sedativo e soddisfazione fisica del paziente e una maggiore efficienza dell’indagine endoscopica.
2.4 Sinergismi e conseguenze dell’associazione Propofol - oppiacei
Le BDZ esercitano un potenziamento spinale e una inibizione sovra spinale dell’analgesia da oppioidi con il risultato che l’associazione realizza un sinergismo di 8 volte sia in senso sedativo, sia depressivo respiratorio; ne consegue che è obbligo ridurre la dose di BDZ, almeno inizialmente, a un quarto o un mezzo della posologia abituale.
Lo stesso sinergismo si verifica con l’associazione Propofol – oppiacei, dove episodi di depressione respiratoria rappresentanto la complicanza più importante e pericolosa.
25 2.5 Altre alternative
A fianco dei sedativi e degli oppiacei è segnalato un efficace uso di un agente neuroleptico, il droperidolo.
È però un farmaco che ha lente cinetiche redistributive e di eliminazione ed effetti collaterali extrapiramidali dose-indipendenti. Procure disforia ed una compromissione psicomotoria protratta che lo rende scarsamente maneggevole.
Non compromette il drive respiratorio ipercapnico e potenzia quello ipossico anche se provoca ipotensione. Può essere utilizzato con vantaggio nei pazienti affetti da BPCO.
La dose generalmente impiegata è di 1-2.5 mg fino a 5 mg.
2.6 Strategia di somministrazione dei farmaci: Target controlled infusion Oggi un gran numero di procedure chirurgiche vengono eseguite con tecniche meno invasive rispetto al passato e di conseguenza è necessario utilizzare tecniche anestesiologiche locali o loco-regionali associate a sedazione, invece che in anestesia generale.
Fino a pochi anni fa la sedazione veniva effettuata somministrando boli subentranti di sedativi fino ad ottenere un livello di obnubilamento del sensorio adeguato alla situazione, oppure somministrando infusioni continue degli stessi basandosi su dosaggi proporzionati al peso del paziente (mg/kg/h).
In procedure chirurgiche particolarmente cruente, in cui è difficile controllare il dolore con tecniche di anestesia locale o loco-regionale può essere aggiunto anche un oppiaceo, per ottenere un paziente calmo e tranquillo e un sonno facilmente risvegliabile a comando, che permette il mantenimento del controllo autonomo delle vie aeree e del respiro.
Questa sedazione ottimale non è facile da raggiungere, soprattutto quando vengono usati farmaci sedativi, come per es. il midazolam che ha una finestra terapeutica molto stretta e un tempo di effetto di picco ritardato.
In questo modo non è raro ottenere un sovradosaggio indesiderato nel tentativo di accelerare il raggiungimento del livello di sedazione desiderato, con presenza di apnea, pericolosa in assenza di monitoraggio adeguato dei parametri vitali.
Il Propofol è usato molto frequentemente a dosaggi subipnotici per la sedazione cosciente per le sue proprietà farmacocinetiche favorevoli che lo rendono facilmente adattabile alle esigenze individuali.
Ha un rapido onset e una breve durata d’azione, determina rapide risposte alle modificazioni della velocità di infusione con scarsi effetti collaterali.
L’infusione manuale è legata a maggiore probabilità di effetti collaterali che vanno da un eccessiva sedazione fino alla perdita del controllo della respirazione.
La migliore modalità di somministrazione continua di ipnotici (target controller infusion), infusione basata su un target plasmatico o meglio ancora su un target al sito effettore.
La TCI è una metodica basata sull’infusione di farmaci tramite l’utilizzo di pompe programmate, con appositi modelli matematici, in base ai dati del paziente. Tali dispositivi permettono al farmaco di raggiungere in modo ottimale la concentrazione nel plasma (target plasmatico) o nel tessuto cerebrale (target al sito effettore) stabilita dall’anestesista; ciò permette di ottenere in procedure brevi il giusto grado di profondità di sedazione, ottimizzando il recupero del paziente e evitando eccessive somministrazioni di farmaci.
Il sistema TCI è costruito su modelli farmacocinetici basati e regolati dalle caratteristiche dei singoli pazienti come l’età, il sesso, il peso, l’altezza e la comorbidità. Ciò consente di richiedere e ottenere facilmente una determinata
27 concentrazione nel plasma o meglio al sito effettore, mantenerla poi nel tempo senza pericolo di sovradosaggio e con la possibilità di effettuare rapidi aggiustamenti della concentrazione, in base alle esigenze del paziente nei diversi momenti della pratica chirurgica.
La TCI è stata ampiamente testata nell’endoscopia digestiva in sedazione e numerosi sono gli studi clinici che dimostrano il sempre maggiore interesse verso questi tipi di procedure.
Pompa a siringa Alaris PK
La pompa a siringa Alaris PK è un dispositivo di infusione utilizzabile per la somministrazione di anestetici. Il software incorporato nella pompa comprende modelli predittivi farmacocinetici a tre compartimenti e offre quattro modalità operative:
1. Infusione continua (ml/h)
2. Anestesia totale per endovena (TIVA)
3. Anestesia totale per endovena (TIVA) con modalità predittiva TCI 4. Modalità TCI
• Infusione controllata con target plasmatico: in questa modalità l’utente seleziona la concentrazione target desiderata nel plasma e il modello farmacocinetico viene utilizzato per calcolare le velocità di infusione necessarie per raggiungere la concentrazione specificata.
• Infusione controllata con target al sito effettore: in questa modalità l’utente imposta la concentrazione target nel sito effettore desiderata e il modello farmacodinamico viene utilizzato per calcolare le velocità di infusione necessarie per raggiungere la concentrazione specificata.
La pompa a siringa Alaris PK è caratterizzata da un’interfaccia di facile uso che visualizza la velocità di infusione, la quantità complessiva di farmaco
somministrata e la concentrazioni di farmaco stimate nel plasma e nel sito effettore.
L’utilizzo della pompa non limita le responsabilità dell’anestesista incaricato della somministrazione dei farmaci, anche perché le interazioni farmacocinetiche e farmacodinamiche tra i farmaci anestetici, pur essendo note, non vengono considerate per calcolare la concentrazione nel plasma e ne sito effettore.
L’avvio della pompa in modalità TCI provoca l’infusione automatica di una dose di bolo precalcolata, seguita da un’infusione, fino al raggiungimento della concentrazione target selezionata. È pertanto essenziale tener conto delle caratteristache del paziente e della velocità di infusione o della concentrazione nel plasma selezionate.
Descrizione della modalità TCI
Il modello tricompartimentale si riferisce al fatto che il rapporto dose/risposta può essere suddiviso in: rapporto tra dose somministrata e concentrazione nel plasma (fase farmacocinetica), rapporto tra la concentrazione nell’organo in cui il farmaco ha effetto e l’effetto clinico (fase farmacodinamica), e la combinazione tra farmacocinetica e farmacodinamica.
Lo scopo principale di somministrare un farmaco ad una dose specifica risiede nella necessità di ottenere un effetto clinico specifico, che si verifica solo somministrando una dose terapeutica specifica nel sito d’azione (recettore). Nel caso specifico degli anestetici, il sito effettore non è il plasma ma il cervello, dove non è possibile misurare direttamente le concentrazioni. Fino ai primi anni ’90 si riteneva che il bilanciamento della concentrazione nel sangue/cervello fosse virtualmente immediato. Per questo tutti i modelli TCI iniziali utilizzavano come target il plasma. Nel corso degli anni divenne, tuttavia, sempre più evidente che le variazioni della concentrazione nel plasma provocavano un ritardo temporale nel bilanciamento tra le concentrazioni nel plasma e nel sito effettore, e poichè l’effetto clinico varia
29 parallelamente alla concentrazione in quest’ultimo, la velocità di distribuzione del farmaco può essere specificata facendo riferimento all’effetto del farmaco stesso nel tempo.
Il modello TCI consente prima di calcolare il profilo della concentrazione nel plasma richiesto per ottenere la concentrazione target nel sito effettore il più rapidamente possibile, quindi le velocità di infusione richieste per ottenere un profilo di concentrazione nel plasma specifico. Il rapporto tra la concentrazione nel sito effettore e nel plasma genera una dose di induzione maggiore seguita da una pausa nell’infusione che consente al plasma di equilibrarsi in base alla concentrazione nel sito effettore.
Modalità TCI, modello Schnider
Esistono vari modelli della pompa a siringa Alaris PK (Marsh, Minto, Gepts, Schnider) tutti ampiamente utilizzati e certificati.
Quello da noi utilizzato e il modello Schnider (fig 1). È un modello a tre comparti con covariate multiple, rettificate per gli adulti per il Propofol, quali età, peso corporeo, altezza, sesso e la massa corporea minima. Presenta un volume di distribuzione centrale minore rispetto al modello Propofol-Marsh. Le concentrazioni di soluzione infusa consigliate in letteratura sono 10-20 mg/ml.
Vari studi hanno dimostrato che il bilanciamento del Propofol nel plasma/sito effetto è molto più veloce di quanto stimato nel modello Marsh. Il valore medio della velocità di bilanciamento tra i compartimenti del plasma e del sito effettore corrisponde meglio al decorso temporale dell’effetto del farmaco rispetto alla concentrazione nel sito effettore.
CAPITOLO 3
MONITORAGGIO DEL PAZIENTE
Il monitoraggio del paziente è un elemento essenziale della sedazione endoscopica e racchiude in sé la misurazione dei parametri fisiologici.
La sedazione deve garantire ansiolisi, amnesia, analgesia e attenuazione del disagio provocato dalla procedura, senza però penalizzare la sicurezza.
Le linee guida SIAARTI relative alla sedazione in N.O.R.A., in associazione alle Società Scientifiche delle diverse aree come la Società Italiana Endoscopica Digestiva (SIED), hanno sottolineato l’importanza di un monitoraggio clinico-strumentale del livello di coscienza, della ventilazione, dell’ossigenazione e dei parametri cardio-vascolari prima, durante e dopo la sedazione.
3.1 Monitoraggio dei parametri vitali
Dopo che il paziente è stato selezionato, si può procedere alla somministrazione dei farmaci in seguito al monitoraggio dei parametri basali:
Ø Frequenza cardiaca (ECG); Ø Saturazione di ossigeno (SpO2); Ø Pressione arteriosa.
Per un corretto monitoraggio è importante anche controllare la ventilazione mediante l’osservazione delle escursioni della gabbia toracica, la pulsossimetria, considerando critici valori di SatO2 90% per oltre 30 secondi con eventuale supplementazione di O2 a 2-3-L/min.
Oppiacei e BDZ rappresentano la scelta più logica per coprire le esigenze sedative anche in endoscopia digestiva, considerando però il rischio di sinergismo depressivo respiratorio tra le due categorie di farmaci. La
31 depressione respiratoria da BDZ presenta una componente meccanica e una funzionale; la prima è data da una ostruzione parziale o completa delle vie aeree per ipotonia dei muscoli oro-faringei che determina lo scivolamento della lingua in ipofaringe. Il respiro stertoroso o il russare sono segni di ostruzione parziale che possono essere risolti facendo estendere il collo, sollevando la mandibola o posizionando anche una canula oro-faringea.
La componente funzionale consiste nella riduzione del volume corrente data da una ipotonia del diaframma, per depressione del nervo frenico. A causa dell’effetto delle BDZ il lavoro respiratorio ricade sui muscoli intercostali e su quelli addominali.
La depressione respiratoria sostenuta invece dagli oppioidi è data da una riduzione della frequenza respiratoria, un ottundimento del drive chimico della ventilazione e una rigidità della gabbia toracica.
Quindi l’abbinamento con BDZ può aggravare l’ipoventilazione alveolare, compromettere la performance contrattile dei muscoli intercostali e deprimere il drive chimico della respirazione; è opportuno un controllo costante della frequenza respiratoria e l’auscultazione dei campi polmonari.
Anche il monitoraggio della funzione cardiovascolare è importante e si effettua attraverso il controllo della pressione arteriosa, della frequenza cardiaca e ECG nei pazienti con rischio cardiovascolare aumentato (età avanzata, ipertensione, diabete, coronaropatia), o con rischio carbossiemico aumentato (tabagismo, obesità, BPCO, apnee notturne e anemia).
3.2 Capnografia
Il monitoraggio della ventilazione è importante ai fini della prevenzione degli incidenti ipossici in corso di sedazione perché attenua il rischio di complicanze gravi e rende primariamente manifeste l’ipoventilazione alveolare e l’ipercapnia.
La capnografia è una metodica non invasiva, basata sulla spettrofotometria all’infrarosso. Viene usata per quantificare la CO2 nell’aria espirata, offrendo così una misura sensibile della funzione ventilatoria.
La misurazione avviene su campione di gas espirato e prelevato dalle vie aeree da un tubicino che lo trasporta alla cella del detector. Il valore di pressione parziale di CO2 al termine dell’espirazione è in correlazione diretta con la PaCO2 e si mantiene costante se non si modifica lo spazio morto alveolare e/o il rapporto ventilazione/perfusione.
La normale curva capnografica presenta il picco durante l’espirazione, mentre in inspirazione si verifica una depressione.
Cambiamenti in end-tidal CO2, denotano un’alterazione dello status ventilatorio, e offrono l’opportunità di riconoscere l’ipoventilazione prima della sua valutazione clinica o pulsossimetrica.
Quando la PaCO2 scende al di sotto del valore fisiologico di 38 ± 2 mmHg e il capnometro registra valori intorno a 30 mmHg le cause possono essere diverse: iperventilazione (per es. percezione del dolore), ridotta produzione metabolica di CO2 (per es. ipotermia), riduzione della gittata cardiaca ed embolia plmonare.
Invece quando la PaCO2 sale oltre il valore fisiologico e vengono registrati valori intorno a 45 mmHg le cause possono essere: ipoventilazione alveolare se l’aumento è graduale e l’aumento di produzione di CO2 (per es. febbre, somministrazione di bicarbonato) se l’aumento è brusco.
In caso di apnea l’incremento temporale di PaCO2 è di circa 6 mmHg nel primo minuto, di altri 3-4 mmHg nei minuti successivi.
La registrazione capnografica è considerata uno standard in sala operatoria, ma fuori da questo ambiente la sua misurazione non avviene ancora routinariamente in quanto la protezione delle vie aeree è spesso il fattore determinante il monitoraggio della CO2 di fine espirazione.
33 Attualmente esistono in commercio presidi specifici per permettere la rilevazione del parametro in respiro spontaneo.
3.3Pulsossimetria
La pulsossimetria è una metodica non invasiva per la misurazione continua della percentuale di Hb funzionale presente nel sangue arterioso (SpO2) sfruttando la combinazione di tecniche di spettroscopia e pletismografia . La relazione tra la saturazione di ossigeno e la pressione parziale di ossigeno è definita dalla curva di dissociazione dell’Hb (curva sigmoide). Durante la normale respirazione con livelli di saturazione di ossigeno prossimi al 100%, cambiamenti significativi di pressione parziale di ossigeno possono verificarsi con piccole alterazione della saturazione di O2.
Il pulsossimetro è in grado di identificare episodi di desaturazione prima della comparsa dei segni clinici dell’ipossemia. Il suo funzionamento si basa sulla presenza di un flusso pulsatile arterioso e di una pressione venosa non pulsatile nella sede del sensore.
È opportuno che tutti i pazienti a rischio ipossiemico (fasce estreme di età, apnea notturna, asma, BPCO, patologie infiammatorie acute delle vie aeree, anemia, cirrosi) ricevano O2 supplementare di 2-4 L/min attraverso canule nasali.
Dobbaimo però tener presente che l’ossigenoterapia, rallentando l’insorgenza di ipossemia, ritarda la segnalazione dell’apnea da parte del pulsossimetro e può mascherare una ritenzione di CO2, comportando l’insorgenza di acidosi, iperkaliemia, aumento della catecolamine circolanti, aritmie ventricolari, ipertensione o ipotensione, cefalea, edema cerebrale, ipertensione endocranica, agitazione psicomotoria e obnubilamento del sensorio fino al coma.
Valori di SpO2 inferori al 90% possono riconoscere come cause: basso valore di SatO2 e di PaO2 da bassa tensione alveolare di O2 o da shunt dx-sx, vasocostrizione nel sito di applicazione e mal posizionamento del sensore.
3.4Pressione arteriosa
Viene comunemente misurata in maniera non invasiva con un dispositivo oscillometrico dotato di un trasduttore elettronico di pressione che rileva le oscillazioni del flusso sanguigno.
3.5 Bispectral Index (BIS monitor)
E’ un metodo di valutazione non invasivo del livello di coscienza del paziente. Ciò è importante per prevedere un piano di sedazione adeguato a prescindere dalla procedura, dal paziente e dall’intensità degli stimoli.
Occorre un mezzo che possa aiutare a prevenire l’insorgenza di una fase di eccessiva superficializzazione o di eccessivo approfondimento. Un apparecchio di questo tipo è il Bispectral Index.
Attraverso la registrazione del segnale bi frontale EEG e il campionamento degli ultimi 30 sec di tracciato, il BIS è in grado di misurare l profondità del piano di sedazione quantificandola su una scala da 0 a 100, in base al grado di coerenza del segnale EEG.
Questo macchinario è in grado di calcolare vari indici comparando con un algoritmo ricavato da un database di migliaia di pazienti:
Ø Burst suppression: fasi di silenzio elettrico, indicativi di piani profondi di anestesia;
Ø Alfa/beta relativo: è il contributo relativo di tali bande do frequenza, spesso attive in corso di sedazioni superficiali;
35 Ø Bicoerenza: relazioni di accoppiamento di fase tra le basse e le alte
frequenze, indicative di livelli moderati di sedazione. Su questi indici il BIS costruisce una funzione probabilistica.
Il valore predittivo del BIS è fortemente influenzato dal tipo di farmaco usato; la corrispondenze tra i valori numerici ed effetti ipnotici (incapacità di rispondere ai comandi verbali) e amnesici di midazolam e propofol in soggetti non sottoposti a stimolazione nocicettiva, sono sufficientemente affidabili e riassumibili:
v 50: BIS95 perdita di coscienza v 63. BIS95 amnesia da propofol v 67: BIS50 perdita di coscienza v 70: BIS95 amnesia da midazolam
v 79: BIS50 sedazione conscia da midazolam v 84: BIS50 amnesia
v 90: BIS50 risveglio.
Quindi in linea di massima, un valore di BIS > 70 esprime un’alta probabilità di risposta al comando verbale, mentre un’alta probabilità di amnesia e ipnosi è correlata a un valore di BIS al di sotto, rispettivamente di 64 e 50.
La variabilità individuale è però ampia in corso di sedazione con midazolam o propofol, il valore di riferimento per la risposta al comando verbale in alcuni “no responders” è più alto della media dei “responders” e viceversa.
Gli oppiacei, che a dosi equisedative sono tre volte meno amnesici del midazolam, compromettono ulteriormente il valore predittivo del BIS.
I limiti più gravi sono la transizione dallo stato di vigilanza alla èerdita di coscienza e veceversa, non viene rilevata come un continum graduale, ma come una risposta binaria “tutto o nulla”; la variabilità individuale è troppo ampia perché il dato numerico sia indicativo del livello di sedazione.
3.6 Dimissibilità
Al termine della procedura è necessario continuare ad avere cura del paziente fino alla completa dimissibilità, al fine di ridurre i rischi di depressione cardio-respiratoria una volta cessata l’osservazione.
La durata del periodo di osservazione dipenderà dal tipo di sedazione, dalle condizioni generali del paziente e dalla natura dell’indagine effettuata.
Tempo di risveglio: è il tempo necessario affinchè si ripristini la persistente
stabilità dei parametri vitali, per es. frequenza cardiaca, pressione arteriosa, saturazione di O2, livelli di vigilanza, dell’orientamento temporo-spaziale e dell’autonomia riflessa. In genere in questo periodo, se la sedazione è stata ben dosata, si esaurisce nel giro di 5-10 min. Il paziente deve continuare ad essere monitorato e sotto costante osservazione.
Tempo di recupero: è il tempo che serve al paziente per recuperare il
coordinamento psico-motorio, che gli consente di allontanarsi deambulando autonomamente anche se deve essere accompagnato da un soggetto adulto. In genere è variabile da paziente a paziente e richiede in media 30-40 min. Il paziente non potrà guidare l’automobile, né svolgere attività nelle quali è richiesta concentrazione o prontezza dei riflessi per le successive 12-24 h, anche se sarà autonomo e cosciente.
È quindi importante assicurarsi che il paziente venga riaccompagnato durante il ritorno al proprio domicilio.
Esistono dei protocolli anestesiologici nei quali vengono definiti i criteri di dimissibilità di pazienti sottoposti ad analgosedazione:
Ø Il paziente deve essere sveglio e ben orientato; i bambini e i pazienti con stato mentale primitivamente alterato devono ritornare allo stato mentale precedente all’indagine;
37 Ø I parametri vitali devono essere stabili e nei liniti accettabili;
Ø Deve passare un lasso di tempo sufficiente (almeno 1h) dall’ultima somministrazione di agenti antagonisti delle BDZ e/o oppioidi, per avere la certezza che il paziente non sia nuovamente sotto sedazione/analgesia alla fine dell’effetto dell’antagonista;
Ø I pazienti devono essere dimessi affidandoli ad un adulto responsabile, in grado di accompagnarli a domicilio e riferire ogni complicanza post-procedura;
Ø I pazienti devono avere istruzioni scritte riguardanti l’assunzione di alimenti, farmaci e attività consentite dopo la procedura.
CAPITOLO 4
ANALGOSEDAZIONE
IN ENDOSCOPIA DIGESTIVA
Sedazione ed analgesia sono considerate la migliore integrazione per una buona riuscita dell’esame endoscopico.
La sedazione deve per prima cosa ridurre l’ansia e il discomfort del paziente, e in secondo luogo aumentare la tollerabilità e la soddisfazione della procedura. Inoltre minimizza i rischi fisici durante l’esecuzione dell’esame fornendo all’endoscopista un contesto tale da consentirgli un’ approfondita e scrupolosa indagine.
Nonostante i benefici della sedazione, il suo uso rimane problematico.
La sedazione ritarda la dimissibilità del paziente, aumenta complessivamente il costo della procedura e il rischio di complicazioni cardiopolmonari.
Ciò però non costituisce un limite, infatti l’uso della sedazione nelle indagini endoscopiche continua ad essere incrementato in tutto il mondo.
La sedazione può essere definita anche come una depressione farmacologicamente indotta del livello di coscienza. Quindi la conoscenza della farmacocinetica e farmacodinamica degli agenti utilizzati è necessaria per definire al meglio e massimizzare la probabilità che il livello di sedazione desiderato sia accuratamente raggiunto, tenendo anche in considerazione la risposta individuale alla sedazione stessa.
BDZ e oppioidi sono le classi di farmaci più largamente utilizzati nella sedazione endoscopica.
Sebbene questi agenti producono effetti sedativi ed analgesici in molti pazienti, mancano delle proprietà farmacologiche necessarie per ottenere una sedazione ottimale durante la procedura. Per esempio, gli oppiodi analgesici sono
39 bradicardia, nausea e vomito. Inoltre, sia il fentanyl che la meperidina, i due oppioidi maggiormente utilizzati, hanno una relativa lunga durata d’azione e i loro effetti possono residuare per diverse ore dopo la fine dell’endoscopia. Similmente, l’effetto ipnotico delle BDZ può persistere per 4-6 ore . Il midazolam, la più importante BDZ idrosolubile, presenta dei vantaggi rispetto al diazepam, quali la minore durata d’azione e la più rapida eliminazione del dolore quando iniettata endovena.
L’amministrazione combinata di BDZ e oppiodi, producendo entrambi depressione respiratoria e ipotensione, accresce il potenziale di queste complicanze.
Di conseguenza, sia singolarmente che in associazione, BDZ e oppiodi mancano della sicurezza e del profilo farmacocinetico richiesto per una ottimale analgosedazione durante l’indagine endoscopica.
L’agente ideale dovrebbero possedere proprietà sedative, analgesiche e amnesiche, e un profilo farmacocinetico compatibile con un rapido onset (1-2 min), breve durata d’azione (5-10 min) e un rapido ricovero (15-20 min).
Dovrebbe inoltre possedere una prevedibile risposta farmacodinamica con un range di moderata sedazione, esercitare minimi effetti depressivi cardiopolmonari, ed avere un farmaco antagonista.
Infine, il suo utilizzo dovrebbe essere conforme alle regolamentazioni nazionali ed essere confrontato con le correnti metodologie in atto.
Ogni volta che è possibile, dichiarazioni e raccomandazioni vengono sviluppate sistematicamente dall’ analisi di evidenze base della letteratura, con l’intento di sviluppare protocolli che permettono di migliorare la qualità della procedura, di ridurre l’incidenza delle complicazioni relative alla sedazione e di tener conto delle necessità ed esigenze dei pazienti.
Dal punto di vista prospettico, per un costante miglioramento della sedazione nell’indagine endoscopica, sarà importante sia andare a valutare eventuali nuovi farmaci e attuare una rivalutazione di quelli attualmente utilizzati, sia
tenersi aggiornati sullo sviluppo di nuove ed efficaci metodiche utilizzabili in questo ambito.
41
CAPITOLO 5
STUDIO CLINICO
In questo capitolo verrà compiuta l’analisi dei dati relativi alla sedazione nell’endoscopia digestiva.
Lo studio è stato effettuato presso l’ambulatorio di endoscopia del Dipartimanto di Chirurgia presso la Clinica Chirurgica dell’Ospedale S. Chiara di Pisa dove viene offerta la procedura endoscopica in sedazione organizzata in una seduta settimanale o secondo eventuali necessità.
Questa rappresenta una proposta innovativa che permette e assicura, quando necessario o semplicemente quando il paziente ne faccia richiesta, di ridurre il dolore e discomfort grazie un efficace e sicuro livello di analgosedazione durante le procedure invasive.
L’attività è garantita dall’anestesista nell’ambito dell’Ospedale senza dolore.
5.1Scopo dello studio
Obiettivo generale: Valutazione di efficacia, sicurezza e gradimento del paziente sottoposto ad indagine endoscopica in sedazione effettuata dall’anestesista in regime ambulatoriale.
Obiettivo specifico: Valutazione di efficacia e sicurezza della sedazione nell’endoscopia digestiva nel sottogruppo sottoposto ad endoscopia del tratto digestivo inferiore con metodica TCI sia con somministrazione di solo ipnotico (Propofol), sia di ipnotico (Propofol) associato ad oppioide, considerando il monitoraggio del paziente durante la procedura, i tempi di recupero e le necessità farmacologiche atte a garantire la completezza dell’esame.
5.2Obiettivo generale 5.2a Materiali e metodi
Lo studio retrospettivo analizza le informazioni raccolte e il gradimento in un arco di tempo di circa un anno e mezzo, da marzo 2008 a settembre 2009. Sono stati presi in considerazione 172 pazienti (gruppo 0), 128 femminee 44 maschi, sottoposti a endoscopia in sedazione, di età compresa tra i 22 e gli 88 anni (età media = 57,97; età media femmine = 58,22; età media maschi = 57,75).
Tutti i pazienti, ASA I, II e III, sono stati sottoposti ad una valutazione anestesiologica e selezionati mediante la compilazione di un questionario anamnestico (fig 2) che raccoglie le principali informazioni sullo stato di salute del paziente da sottoporre ad indagine ed eventuali terapie assunte a domicilio che potrebbero interferire con i farmaci utilizzati durante l’analgosedazione; sono stati informati della tecnica anestesiologica utilizzata durante la procedura e dei suoi possibili effetti collaterali, ed infine è stato validato un consenso informato (fig 3).
Prima dell’inizio della procedura in tutti i pazienti sono stati monitorizzati i parametri vitali (pressione arteriosa, ECG, SpO2, frequenza cardiaca e respiratoria) ed in 13 è stato anche utilizzato il monitoraggio dello stato di coscienza (BIS).
I pazienti sono stati sottoposti a gastroscopia e a colonscopia, entrambe in sedazione, come segue:
Ø Gastroscopie: 11; Ø Colonscopie: 164.
Per quanto riguarda le gastroscopie in sedazione,i pazienti esaminati sono stati 11, 9 femmine e 2 maschi, di età compresa tra i 36 e i 78 anni (età media = 58,24%).
43 Per quanto riguarda le colonscopie in sedazione, i pazienti esaminati sono stati 165, 122 femmine e 43 maschi, di età compresa tra i 22 e gli 88 anni (età media =57,97).
5.2b Farmaci e tecniche anestesiologiche
Le tecniche anestesiologiche utilizzate per la somministrazione dell’iponotico sono state due, a boli e in TCI, con somministrazione di ipnotico (Propofol) associato o meno alla somministrazione di oppioidi
e ansiolitici (tabella 3):
• Nella somministrazione a boli è stato utilizzato Propofol 1%, con eventuale associazione ad oppioidi (meperidina e fentanest), o a BDZ (midazolam);
• Nella somministrazione in TCI è stato utilizzato Propofol 2%, con eventuale associazione ad oppioidi (meperidina e fentanest).
5.2c Risultati
I 172 pazienti sono stati sottoposti sia a gastroscopia che a colonscopia con Propofol associato o meno ad oppioide, mediante l’utilizzo delle tecniche anestesiologiche sopra descritte (tabella 3):
Tabella 3 ,
Metodica Propofol Propofol + Oppioide Propofol BDZ Tot BOLI 16 8 Midazolam = 1 25 TCI 74 73 147 172
172 pazienti:
v Endoscopie diagnostiche: 169 (125 femmine e 44 maschi); v Endoscopie operative: 3 (femmine);
v Età media: 58,1 anni (22-88);
v Durata media della procedura endoscopica: 16,72 minuti (min 3’ – max 50’);
v Si riportano i dati relativi alla metodica TCI: 147 pazienti
° Media matematica del valore massimo al sito effettore di Propofol: 3,97γ/ml (min 1γ/ml – max 7γ/ml);
° Dose media di Propofol: 0,149 mg/kg/min; v Respiro assistito: 2 casi (2,90%);
v Risveglio prolungato: 2 casi (2,90%) dove c’è da segnalare un picco maggiore al sito effettore del propofol (6 e 7γ/ml);
v Utilizzo di atropina per insorgenza di bradicardia in 4 casi. v Monitoraggio emodinamico: tabella 4
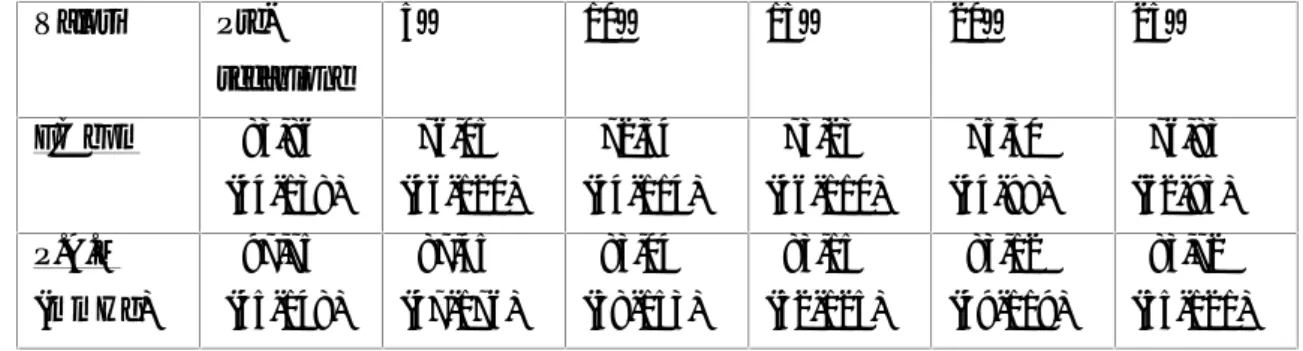
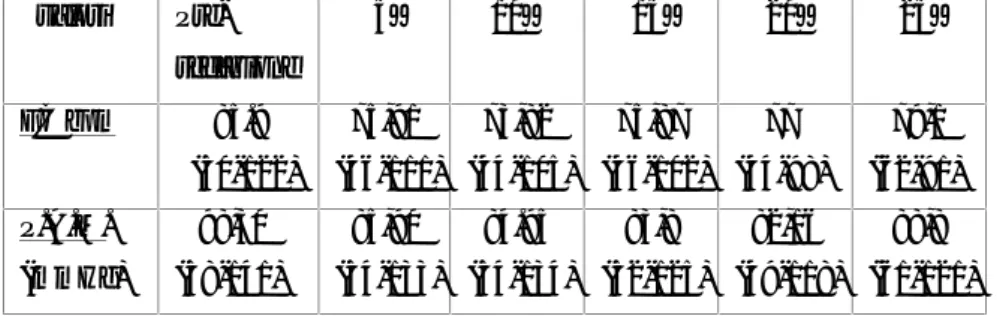
Tabella 4 Valori Pre-sedazione 5’ 10’ 15’ 20’ 25’ FC bpm 83,86 (44-138) 76,05 (46-120) 72,54 (44-114) 73,23 (46-110) 75,30 (44-98) 76,83 (62-93) P.A.M (mmHg) 97,75 (45-148) 87,45 (47-176) 83,04 (38-153) 83,15 (52-125) 83,12 (49-119) 83,72 (55-121)
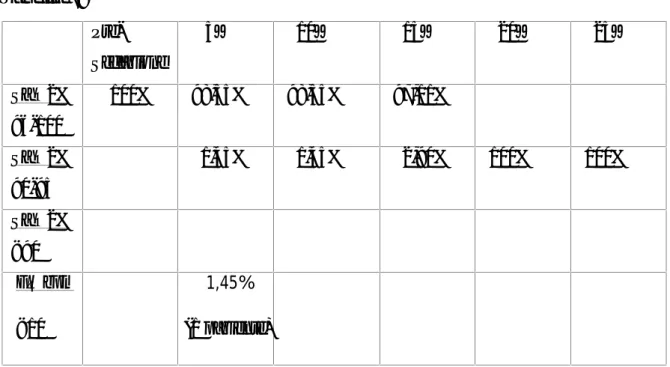
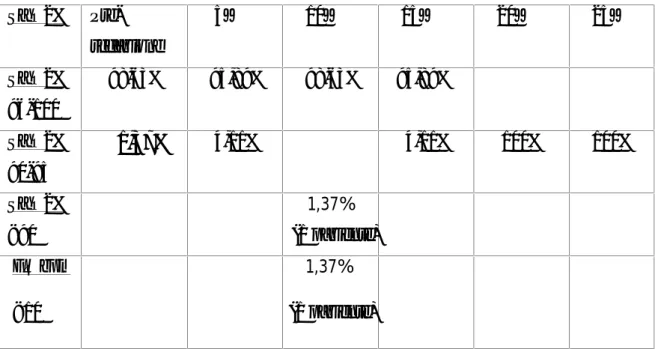
Sono state inoltre monitorizzate la saturazione di O2 e la frequenza respiratoria, al fine di individuare se e quanti casi di desaturazione e di depressione respiratoria si sono verificati (tabella 5).
45 Tabella 5: Pre-sedazione 5’ 10’ 15’ 20’ 25’ Sa O2% 96-100 98,84% 97,09% 98, 84% 98,84% Sa O2% 90-95 1,16% 2,91% 0,58% 2,91% 100% 100% Sa O2% < 90 0,58% (1 paziente) FR bpm <10 0,58% (1 paziente) 0,58% (1 paziente) 5.3 Obiettivo specifico 5.3a Materiali e metodi
Lo studio da noi effettuato riguarda i pazienti sottoposti a colonscopia in sedazione esaminati con la tecnica TCI.
Sono stati presi in considerazione 142 pazienti, 106 femmine e 36 maschi, di età compresa tra i 22 e gli 88 anni, classi ASA I,II e III, sottoposti a colonscopia in N.O.R.A., regime ambulatoriale. Tutti i pazienti sono stati sottoposti ad una valutazione anestesiologica e selezionati mediante la compilazione di un questionario anamnestico (fig 2) che raccoglie le principali informazioni sullo stato di salute del paziente da sottoporre ad indagine ed eventuali terapie assunte a domicilio che potrebbero interferire con i farmaci utilizzati durante l’analgosedazione; sono stati informati della tecnica anestesiologica utilizzata durante la procedura e dei suoi possibili effetti collaterali, ed infine è stato validato un consenso informato (fig 3). Prima dell’inizio della procedura in tutti i pazienti sono stati monitorizzati i parametri vitali (pressione arteriosa, ECG, SpO2, frequenza cardiaca e