Indice
Capitolo 1: la surrenectomia con tecnica mini-invasiva
1.1 Un po’ di storia
1.2 La surrenectomia laparoscopica
12.1 Aspetti tecnici
1.2.2 Confronto tra i diversi approcci
1.3 Indicazioni e controindicazioni
1.4 Complicanze intraoperatorie e postoperatorie
1.5 Surrenectomia robotica
1.6 Surrenectomia parziale
Capitolo 2: Obbiettivi dello studio
Capitolo 3: Materiali e Metodi
Capitolo 4: Risultati
Capitolo 5: Discussione e conclusioni
1. La surrenectomia con tecnica mini-invasiva
1.1 Un po’ di storia
Knowsley Thornton è ritenuto essere il primo ad aver eseguito con successo la prima surrenectomia per un tumore soprarenale a Londra nel 1889. Il paziente, una donna di 36 anni con irsutismo secondario al tumore, sopravvisse due anni, finché non ricomparse la malattia. Anche se Harvey Cushing definì il fondamentale ruolo delle cellule ipofisarie basofile nella malattia di Cushing, altri presto riconobbero che lo sviluppo della sindrome di Cushing richiede la presenza della corteccia surrenalica. Il ricorso alla surrenectomia per questa malattia fu quindi il passo successivo. I risultati di dieci surrenectomie per la sindrome di Cushing eseguite da Walters e Priestley furono pubblicate nel 1934. Essi riscontrarono quattro carcinomi, un adenoma, tre casi di iperplasia e due ghiandole normali. Anche quando veniva eseguita la surrenectomia subtotale, si aveva una mortalità del 30%. La prospettiva per questi pazienti sottoposti a surrenectomia per sindrome di Cushing cambiò drasticamente quando il cortisone divenne disponibile per la terapia sostitutiva. Il primo utilizzo del cortisone nella surrenectomia per la sindrome di Cushing è stato riportato nel 1949 alla Mayo Clinic, dove il tasso di mortalità crollò a zero per i successivi 18 casi. Questo ha avuto un grande impatto per la endocrinochirurgia, non solo rendendo la surrenectomia una procedura sicura ma anche facilitando l’operazione di ipofisectomia totale. Due anni dopo la scoperta dell’aldosterone fu descritta da Jerome Conn la sindrome dell’iperaldosteronismo primario, caratterizzata da ipertensione e ipokalemia. Si trattava di una donna di 34 anni che presentava tetania, paralisi periodiche, parestesia, poliuria, polidipsia e ipertensione. È stato ritenuto che fosse affetta da iperplasia surrenalica bilaterale, ma all’esplorazione del surrene destro, fu scoperto un adenoma della corticale di 4 cm, la cui rimozione permise la guarigione dell’ipertensione e dei disturbi metabolici. L’adrenalina è stato il primo ormone a essere scoperto, ma il suo ruolo cruciale nella clinica della sindrome causata dal feocromocitoma non è stato definito fino a molti anni dopo quando l’ormone fu estratto dai tumori surrenalici. Frankel nel 1886 riportò per primo di una paziente con un probabile feocromocitoma, una donna di 18 anni che
presentava palpitazioni intermittenti, tachicardia e attacchi d’ansia. La donna morì dopo un grave episodio di dolore toracico e dispnea, e all’autopsia fu descritta la presenza di una elevata vascolarizzazione di entrambi i surreni. Il termine di “feocromocitoma” fu coniato da Pick nel 1912 e la prima rimozione con successo del feocromocitoma fu eseguita da Cesar Roux a Losanna nel 1926, seguito dal Dr. Charles Mayo a Rochester nell’anno seguente. Presto diventò evidente che la chirurgia del feocromocitoma era estremamente rischiosa con una elevata mortalità legata all’incontrollata ipertensione perioperatoria, a picchi di ipertensione severa durante la manipolazione del tumore e all’ipotensione postoperatoria. Grazie al miglioramento delle tecniche anestesiologiche e alla maggiore comprensione della fisiopatologia della malattia, fu introdotto l’utilizzo di agenti come la fentolamina e la noradrenalina nel controllo della pressione arteriosa. Priestley riportò quindi nel 1956 di una serie di 51 pazienti sottoposti a chirurgia per feocromocitoma, senza nessuna mortalità.
La prima surrenectomia è stata eseguita attraverso una incisione sottocostale a forma di T, simile a quella descritta nel 1882 da Carl von Langenbuch per la colecistectomia. Molte delle iniziali operazione sul surrene furono eseguite per la rimozione di grandi tumori e tale approccio era frequentemente troppo basso per permettere un accesso adeguato. I chirurghi quindi cominciarono a porre l’incisione a un livello progressivamente più alto, spesso resecando l’undicesima o la dodicesima costa. Nel 1932 Lennox Broster di Londra ideò una operazione che permetteva l’accesso al surrene utilizzando un approccio tran pleurico, trans diaframmatico attraverso una lunga incisione posteriore intercostale. Nel 1927, Charles Mayo utilizzò una incisione a livello del fianco quando eseguì la prima surrenectomia negli Stati Uniti per feocromocitoma. Furono quindi provate incisioni anteriore, laterale e retroperitoneale, ognuna con i propri vantaggi e problemi.
L’inizio della chirurgia mini-invasiva si fa risalire al 1987, anno in cui Phillipe Mouret ha eseguito la prima colecistectomia laparoscopica a Lione. I benefici della chirurgia mini-invasiva ha fatto sì che rapidamente la colecistectomia laparoscopica sostituisse la tradizionale colecistectomia open come procedura standard nella chirurgia della colecisti. Questa evento ha dato inizio a una nuova era della chirurgia. Questo ha determinato infatti dei cambiamenti radicali nella pratica chirurgica, creando un impeto da parte dei chirurghi a puntare su questa nuova disciplina. Sempre più procedure chirurgiche vennero quindi prese in considerazione per essere eseguite laparoscopicamente.
La rimozione del surrene attraverso una chirurgia open fu incontestata fino al 1992. La surrenectomia laparoscopica è stata eseguita per la prima volta da Go e colleghi nel Gennaio 1992 su un paziente con un adenoma aldosterone-secernente (121). Suzuki e colleghi hanno
eseguito la stessa procedura nel Febbraio 1992 in un paziente con un feocromocitoma(121). L’approccio transperitoneale laparoscopico al surrene è stato descritto per la prima volta in letteratura da Gagner nel 1992(113). Questo nuovo approccio fu accettato con entusiasmo dalla comunità degli endocrinochirurghi e altri descrissero l’approccio endoscopico posteriore retroperitoneale.
Da allora, numerosi studi comparativi retrospettivi sono stati pubblicati, dimostrando tutti i benefici della tecnica mini-invasiva nella chirurgia del surrene. La surrenectomia laparoscopica è così diventata rapidamente il gold standard per il trattamento di numerose patologie del surrene. Questo successo non è sorprendente, considerando le somiglianze tra la surrenectomia laparoscopica e la colecistectomia laparoscopica e il travolgente successo della colecistectomia laparoscopica. In entrambe queste procedure infatti l’approccio laparoscopico permette di evitare un’importante incisone nei quadranti superiori dell’addome; entrambe sono procedure ablative e che quindi non richiedono nessuna fase ricostruttiva che può essere problematica da eseguire con l’approccio laparoscopico (come l’esecuzione di anastomosi); entrambe le procedure beneficiano della magnificazione della visione ottenuta grazie al laparoscopio, aspetto utile visto che sono regioni anatomicamente difficili e con il rischio che si verifichino delle lesioni alle strutture vicine durante l’esposizione delle strutture di interesse; entrambe sono comunemente eseguite per patologie benigne e con un pezzo operatorio di piccole dimensioni facilmente estraibile.
1.2 La surrenectomia laparoscopica
Il successo dell’approccio laparoscopico al surrene, che negli ultimi anni sta soppiantando sempre più la chirurgia open, è legato a molteplici vantaggi generici che questa tecnica offre sia in fase intra- che post-operatoria rispetto alla tecnica laparotomica. In oltre sono presenti anche numerosi vantaggi specifici della chirurgia laparoscopica del surrene. I surreni sono ghiandole piccole, friabili e altamente vascolarizzate e una meticolosa emostasi e una delicata manipolazione del tumore sono necessari affinché la chirurgia surrenalica sia un successo. A causa della loro anatomia, le ghiandole surrenaliche sono dal punto di vista chirurgico relativamente inaccessibili per la loro posizione profonda retroperitoneale. Per questa ragione diversi approcci chirurgici sono stati impiegati negli anni per la chirurgia open del surrene. Questi includono l’approccio anteriore, transperitoneale utilizzando un’incisione sottocostale; l’approccio posteriore, retroperitoneale con il paziente completamente prono e l’approccio
posterolaterale attraverso l’undicesima e la dodicesima costa, utilizzando anche in questo caso una via esclusivamente extraperitoneale. Tutte queste procedure necessitano di una larga incisione e sono associate a un importante dolore e morbidità postoperatoria. Frequentemente in questi pazienti l’entità del dolore postoperatorio preclude un rapido ritorno alle normali attività di routine. In alcuni casi si può avere un dolore cronico e prolungato associato alle resezione delle coste(119). L’approccio open transperitoneale permette una buona esposizione chirurgica del surrene, ma richiede una estesa dissezione degli organi adiacenti. Nel corso della surrenectomia destra, il duodeno è Kocherizzato, la flessura epatica del colon è riflessa medialmente e i ligamenti triangolare e coronarico vengono sezionati. Se è utilizzato l’approccio laparoscopico per il surrene destro, è sufficiente sezionare il ligamento coronarico e triangolare del fegato. Nella surrenectomia sinistra open transperitoneale è necessaria la dissezione della flessura splenica e del colon discendente e la mobilizzazione della coda del pancreas e della milza. La necessità di una larga incisione e la presenza di un trauma chirurgico intraaddominale conduce a un aumento del dolore postoperatorio, a un ileo prolungato, e a un prolungato periodo di ricovero(119).
Per questi motivi la surrenectomia laparoscopica rappresenta un’opzione allettante sia per il paziente sia per il chirurgo poiché riduce l’invasività ma senza compromettere la possibilità di visualizzare e rimuovere i surreni(20). I vantaggi della surrenectomia laparoscopica infatti consistono in una visione magnificata del campo operatorio permettendo quindi una precisa e emostatica dissezione. Le incisioni cutanee nel corso della procedura laparoscopica sono piccole in confronto alle larghe incisioni necessarie per la chirurgia open.
1.2.1 Aspetti tecnici
Quattro differenti approcci sono utilizzati nella chirurgia del surrene: l’approccio transperitoneale anteriore, l’approccio transperitoneale laterale, l’approccio retroperitoneale laterale e l’approccio retroperitoneale posteriore.
Nella surrenectomia laparoscopica con approccio transperitoneale laterale il paziente viene posizionato in decubito laterale, con il fianco corrispondente alla ghiandola da operare rivolto verso l’alto. Il fianco del paziente viene “spezzato” abbassando il tronco e gli arti inferiori, allargando in questo modo lo spazio situato tra la spina iliaca anteriore superiore e l’arcata costale. La posizione laterale di circa 50-60° per la surrenectomia destra e di 70-80° per la sinistra, associate alla posizione del tavolo operatorio in anti-Trendelemburg di circa 10-20°, facilitano l’esposizione del retroperitoneo determinando lo spostamento per gravità dalla loggia surrenalica dei visceri posti anteriormente, permettendo di ridurre il numero dei trocar
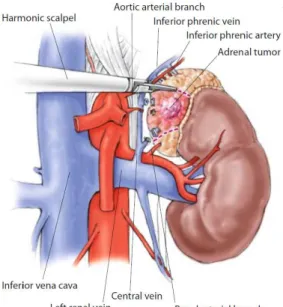
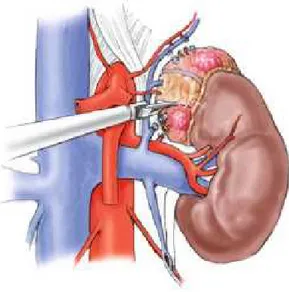
necessari. Il chirurgo si pone lateralmente di fronte al paziente, sul lato opposto a quello del surrene da asportare. Per la surrenectomia destra vengono quindi posizionati 4 trocar: il primo trocar, T1, viene posizionato 3 cm al di sotto dell’arcata costale a livello della linea ascellare anteriore ed è utilizzato per l’ottica a 30° e per l’estrazione del pezzo operatorio. Il secondo e il terzo trocar, T2 e T3, vengono posizionati a circa 4-5 cm sulla destra e sulla sinistra di T1, a 1-5 cm dall’arcata costale. Il T2 accoglie gli strumenti della mano destra dell’operatore (strumenti da dissezione, da taglio, da emostasi e da aspirazione) e T3 gli strumenti della mano sinistra (strumenti da presa e da aspirazione). Il T4, posizionato in sede paraxifoidea accoglie il divaricatore epatico. Nei casi più difficili può essere necessario un quinto trocar. Dopo la prima fase di esplorazione della loggia surrenalica per l’identificazione di aderenze e la loro lisi e l’identificazione di eventuali anomalie, l’intervento procede con l’esposizione del surrene destro. Questo necessità di una adeguata mobilizzazione del fegato, ottenuta mediante l’incisione del peritoneo parietale posteriore a livello dello spazio sottoepatico, proseguita poi verso il ligamento triangolare omolaterale. La mobilizzazione del fegato procede in direzione latero-mediale fino all’identificazione della vena cava inferiore, repere fondamentale per tutta la durata dell’intervento. Le manovre di sezione del peritoneo e dissezione sui tessuti retroperitoneali possono essere eseguiti con il bisturi elettrico monopolare o con quelli ad ultrasuoni o a radiofrequenze. Nella maggior parte delle surrenectomie è attualmente preferibile utilizzare il bisturi a ultrasuoni. Il bisturi a radiofrequenza è utile nei casi in cui si ritenga di dover eseguire emostasi di vasi neoformati e facilmente sanguinanti come nel caso di feocromocitomi o di metastasi. La dissezione procede poi verso il basso, lateralmente alla vena cava inferiore, fino a raggiungere la vena renale. Una meticolosa dissezione lateralmente alla vena cava permette di dissociare delicatamente il surrene, lisando le aderenze tra le due strutture, e di realizzare un’emostasi accurata dividendo i numerosi vasi arteriosi e venosi sottesi in questo spazio virtuale. Questa manovra permette l’identificazione della vena surrenalica media, la quale viene sezionata previa applicazione di due clips sul versante cavale e di una su quello laterale prossimo alla ghiandola. La legatura della vena media e di altri eventuali vasi accessori (nel 20% dei casi è presente una vena surrenale accessoria posta di solito cranialmente) permette di ottenere una ottima mobilità della ghiandola. Si procede così alla dissezione e al controllo del margine superiore dove sono facilmente identificabili i vasi surrenalici superiori provenienti dai vasi frenici. Questi vasi, fatta eccezione per il feocromocitoma, sono di piccole dimensioni e la loro sezione ed emostasi si può facilmente ottenere con il bisturi ad ultrasuoni. Una volta controllato i vasi surrenalici inferiori, provenienti dai vasi renali, anch’essi sezionati generalmente mediante il
solo bisturi a ultrasuoni senza l’uso di clips, il surrene può essere facilmente mobilizzato in direzione supero-laterale mediante una pinza atraumatica e può essere sezionata mediante l’harmonic scalpel la giunzione tra il polo superiore del rene e il surrene. Una volta completata la dissezione sul margine esterno, il surrene completamente mobilizzato viene posto nell’Endobag per l’estrazione attraverso l’orifizio di T1, eventualmente ampliato mediante sezione della fascia muscolare.
Per la surrenectomia sinistra vengono generalmente utilizzati tre trocars, non essendo necessario il trocar aggiuntivo per l’introduzione del divaricatore epatico. All’interno della cavità addominale il chirurgo deve identificare la milza, il lobo sinistro del fegato, la flessura splenica e il colon discendente. L’intervento prosegue con la mobilizzazione della flessura colica sinistra e con la sezione dei ligamenti splenici, i quali devono essere sezionati completamente, compreso il legamento spleno-diaframmatico fino a vedere il fondo gastrico. Questa manovra permetta la mobilizzazione del blocco spleno-pancreatico, rendendo così la milza e la coda del pancreas completamente mobile. Per la posizione del paziente, il blocco spleno-pancreatico cadrà per gravità medialmente al di fuori dell’area surrenalica. Viene quindi individuata nella parte inferiore del campo operatorio la vena renale sinistra nella quale sbocca la vena surrenale principale di sinistra che, previa l’applicazione di clip metalliche, verrà sezionata. La liberazione della ghiandola procede quindi medialmente e durante questa fase è possibile incontrare una o più vene accessorie, che se di calibro significativo, necessitano di un posizionamento di clip prima di poter essere sezionate. Viene quindi eseguita la graduale liberazione del surrene dal polo superiore del rene, controllando i vasi arteriosi inferiori, provenienti dai vasi renali. Proseguendo con la mobilizzazione superiore del surrene vengono quindi identificati i vasi surrenalici superiori, provenienti dalle arterie diaframmatiche, la cui emostasi è generalmente ottenuta con il solo bisturi ad ultrasuoni. Viene quindi completata la mobilizzazione della faccia posteriore e laterale del surrene e l’operazione si conclude con l’estrazione della ghiandola previa inserzione in un sacchetto laparoscopico.
Nell’approccio retroperitoneale laterale il paziente è posizionato in decubito laterale, con il fianco corrispondente al surrene da operare rivolto verso l’alto e il letto è “spezzato” per aumentare lo spazio tra l’arcata costale e la cresta iliaca. Il chirurgo è posto posteriormente al paziente e usa due trocar posti subito al di sotto dell’arcata costale. L’assistente è posizionato sul lato opposto e utilizza il laparoscopio. Nell’approccio retroperitoneale posteriore invece il paziente è posto in posizione prona, utilizzando il ponte di Wilson che sostiene il torace e l’addome. Una incisione di 1.5 cm è eseguita lunga la linea ascellare media, 2 cm al di sotto
della dodicesima costa. Il tessuto sottocutaneo viene quindi inciso e il piano muscolare viene aperto con una dissezione smussa. Superato il piano muscolare si accede allo spazio retroperitoneale. L’operatore crea quindi con il dito indice uno spazio nel retroperitoneo, rimanendo superficialmente alla fascia di Gerota, che non viene aperta. Tale spazio può essere espanso utilizzando un palloncino per dissezione, per ridurre il rischio di un danno vascolare o dei visceri. Dopo che lo spazio di lavoro retroperitoneale è stato creato, il palloncino può essere desufflato e sostituito con un trocar di Hasson di 10 mm. Lo spazio retroperitoneale viene quindi insufflato con CO2 a una pressione di 15mmHg. Solitamente a livello del
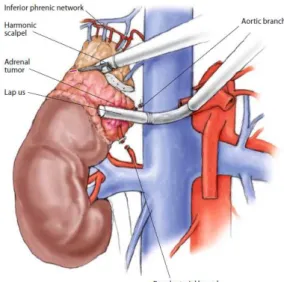
retroperitoneo possono essere utilizzate pressioni di insufflazione superiori a quelle del cavo peritoneale e anche pressioni di circa 25 mmHg possono essere ben tollerate. Pressioni elevate sono particolarmente utili in caso di pazienti obesi, per aumentare la camera di dissezione. I successivi trocar vengono quindi posizionati sotto la diretta visione o con la guida digitale. Poiché la cavità retroperitoneale è normalmente occupata dal rene, dal surrene e dal tessuto adiposo, è importante la creazione di un ampio spazio di lavoro. La fascia di Gerota viene quindi aperta permetto l’esposizione del grasso perirenale, del rene e del surrene. Dopo aver aperto la fascia di Gerota, il grasso retroperitoneale deve essere dissecato verso il basso, in modo da esporre medialmene i muscoli paravertebrali, cranialmente il diaframma, lateralmente il peritoneo (con la milza a sinistra e il fegato a destra). Questo step è di fondamentale importanza, in quanto serve a creare uno spazio adeguato per la successiva dissezione. Successivamente deve essere esposto e liberato il polo superiore del rene, che rappresenta il punto di repere più importante in questo intervento. La liberazione del polo superiore del rene deve essere quanto più completa possibile, ed in alcuni casi deve essere condotta fino all’esposizione dei vasi renali. Questa manovra consente un adeguato abbassamento del polo superiore del rene permettendo quindi la completa esposizione della porzione inferiore del surrene e l’identificazione e la dissezione della vena surrenalica. A questo punto la loggia surrenalica è completamente esposta, delimitata inferiormente dal polo superiore del rene, cranialmente dal diaframma, medialmente dalla colonna e dai muscoli paravertebrali e lateralmente dal peritoneo. La dissezione del surrene destro viene cominciato a livello della sua porzione caudale e mediale, utilizzando la coagulazione monopolare (uncino) o il bisturi ad ultrasuoni. Dopo aver effettuato l’emostasi dei piccoli rami posteriori del surrene destro, la ghiandola viene sollevata in modo da esporre la faccia posteriore della vena cava inferiore e mettere in tensione la vena surrenalica principale, permettendo così la sua identificazione. Si procede quindi alla sua sezione previo posizionamento di clip metalliche. La dissezione del surrene sinistro inizia con l’identificazione dell’ilo renale. La
retrazione verso il basso e lateralmente del rene permette di identificare la vena surrenalica principale, la quale viene sezionata previa applicazione di clip metalliche. Dopo aver sezionato la vena surrenalica principale la dissezione del surrene viene completata a livello della porzione laterale e, per ultima, della porzione craniale. Questa fase dell’intervento viene condotta utilizzando il bisturi a ultrasuoni. Il surrene, rimosso “en bloc” con il grasso perisurrenalico, viene quindi posto in un sacchetto laparoscopico e estratto attraverso il primo orifizio cutaneo.
Un approccio laparoscopico hand-assisted per la chirurgia del surrene può essere preso in considerazione per quei casi di tumori di grande dimensioni o in quelli in cui sono presenti delle difficoltà intraoperatorie come sanguinamento o una impossibilità a proseguire con la dissezione per via laparoscopica. Anche se l’esperienza con questa tecnica nei pazienti con tumori surrenalici è limitata, il suo uso in casi difficili di splenectomia suggerisce che esso può avere qualche utilità in casi selezionati di surrenectomia. Gli autori infatti la consigliano soprattutto nel caso di voluminose neoformazioni per lo più benigne (es. mielolipomi o cisti di dimensioni intorno ai 12 cm) in cui l’introduzione della mano favorirebbe la retrazione della massa dagli organi circostanti e renderebbe più agevole la sua manipolazione. Un altro vantaggio di questo approccio è che esso facilita enormemente l’estrazione del tumore di grandi dimensioni, poiché infatti sarebbe comunque necessario l’esecuzione di una mini-laparotomia per l’estrinsecazione di questi tumori anche nel caso di un approccio laparoscopico puro.
1.2.2 Confronto tra i diversi approcci laparoscopici
Non è chiaro quale di questi approcci sia superiore e ognuno di questi ha i propri vantaggi e svantaggi. L’approccio transperitoneale laterale sembra essere quello più comunemente utilizzato, essendo più semplice rispetto a quello retroperitoneale. Tra i vantaggi dell’approccio transperitoneale possiamo descrivere un maggior spazio di lavoro che permette una migliore esposizione dei tumori surrenalici più grandi (>5cm) e nel caso dei feocromocitomi una minima manipolazione del tumore prima del controllo della vena surrenalica. Infatti, un altro importante vantaggio di tale approccio è che questo permette un rapido accesso alla vena surrenalica, che può quindi essere legata e sezionata precocemente durante la procedura chirurgica. L’approccio transperitoneale permette inoltre una più semplice dissezione grazie alla migliore conoscenza dell’anatomia, a una maggiore familiarità con la chirurgia laparoscopica intraperitoneale nell’individuare, dissezionare e mobilizzare gli
organi intra-addominali, e una più facile identificazione dei landmarks anatomici, che possono aiutare il chirurgo a orientarsi all’interno della cavità peritoneale. Nell’approccio retroperitoneale invece può essere difficile mantenere l’orientamento nel retroperitoneo, dove ci sono meno landmarks anatomici visibili e una quantità significativa di grasso retroperitoneale, specialmente nella sindrome di Cushing. Per l’approccio transperitoneale laterale il paziente è posto in decubito laterale. La gravità aiuta a retrarre medialmente la milza dopo la sua mobilizzazione o il fegato, permettendo un’ampia esposizione del surrene e facilitando la dissezione di neoformazioni surrenaliche di grandi dimensioni. Per la rimozione del feocromocitoma, questa ampia esposizione permette al chirurgo di legare la vena surrenalica con la minima manipolazione e retrazione della ghiandola surrenalica. In oltre, l’approccio transperitoneale permette l’accesso agli organi adiacenti. Può quindi essere eseguita un’ulteriore procedura chirurgica ipsilaterale elettiva insieme alla surrenectomia, quale l’esecuzione di una colecistectomia. Tenendo in considerazione tutti questi aspetti, i vantaggi dell’approccio transperitoneale laterale rendono questa tecnica più versatile e facile da imparare rispetto all’approccio retroperitoneale. Tuttavia, l’approccio transperitoneale richiede la mobilizzazione delle strutture intra-addominale e questo porta a un maggior rischio di un danno vascolare e degli organi intra-addominali, di un ileo prolungato, di irritazione del peritoneo e della formazione di aderenze. Altri svantaggi di questo approccio comprendono le difficoltà per la dissezione in pazienti con adesioni intra-addominali. In oltre, nel caso di una surrenectomia bilaterale nell’approccio transperitoneale laterale è necessario il riposizionamento del paziente.
L’approccio transperitoneale anteriore è l’approccio meno frequentemente descritto in letteratura, a causa dei numerosi inconvenienti e dei pochi vantaggi tipici di questa tecnica. L’esposizione della ghiandola surrenalica utilizzando tale approccio è infatti difficoltosa e offre uno spazio di lavoro limitato. È necessario infatti la creazione a sinistra di una finestra al di sotto del pancreas e del colon trasverso-flessura sinistra con necessità di divaricazione del corpo-coda pancreatici. A destra è invece necessario sollevare il fegato e spostarlo medialmente, mobilizzare inferiormente il colon trasverso e la flessura epatica e di kocherizzare il duodeno. Confrontando tale approccio con quello transperitoneale laterale e quello posteriore, sono necessari quindi ulteriori trocars per introdurre multipli retrattori. In questo approccio infatti il chirurgo si trova a operare contro la gravità, ed è costretto a retrarre gli organi adiacenti piuttosto che a liberare questi dai propri sistemi di sostegno e sfruttare la gravità per liberare la loggia surrenalica. Un altro problema con l’approccio transperitoneale anteriore è legato alla localizzazione del letto delle ghiandole surrenaliche, che è localizzato
nella posizione più declive nel paziente supino. Questo facilita il raccogliersi di sangue, fluido linfatico, oscurando il campo operatorio e allungando il tempo operatorio. Vantaggi di questo approccio comprendono la chiara visione “anatomica” dell’addome e quindi una buona esplorazione addominale complessiva e la chiara visione dei landmarks anatomici. Altro vantaggio è la possibilità di asportare in un solo tempo entrambe le ghiandole surrenaliche nel caso di patologie bilaterale (bisurrenectomia) senza la necessità di riposizionare il paziente al termine della prima surrenectomia. Per questo motivo, tale metodica è utilizzata nei rari casi in cui sia indicata la bisurrenectomia simultanea, poiché questo approccio permette una riduzione sensibile dei tempi morti intra-operatori, eliminando la necessità di riposizionare il paziente al termine della prima surrenectomia. Possibili indicazioni per questo approccio comprendono quindi quei casi in cui è necessario una bisurrenectomia quale una sindrome di Cushing paraneoplastica da neoplasia extra-ipofisaria a sede non identificata o da neoplasia extra-ipofisaria a sede metastatica o non aggredibile chirurgicamente, oppure una sindrome di Cushing da adenoma ipofisario con persistenza di ipercortisolismo residuo malgrado il successo del’intervento ipofisario o con refrattarietà alla terapia medica soppressiva dopo chirurgia trans-sfenoidale. Anche nel caso di tumori primitivi del surrene quali adenomatosi bilaterale con ipercortisolismo cronico, malattia primitiva nodulare pigmentaria del surrene, iperplasia surrenale corticale macronodulare e iperplasia surrenale bilaterale da anomalie dei recettori per l’ACTH o altri recettori (es. sindrome di Mc-Cunn-Albright), essendo indicata una bisurrenectomia, può essere utilizzato l’approccio transperitoneale anteriore.
La difficoltà di raggiungere il retroperitoneo utilizzando la tecnica laparoscopica transaddominale, ha indotto gli Autori a cercare, come già accaduto per la laparotomia, metodiche di approccio alternative. Alla descrizione dell’approccio transperitoneale è seguito così a distanza di un anno la descrizione dell’approccio endoscopico retroperitoneale. La localizzazione retroperitoneale del surrene rende infatti questo approccio anatomicamente ideale permettendo un accesso diretto alla ghiandola, non richiedendo la mobilizzazione delle strutture adiacenti poiché il surrene è una delle prime strutture che si incontrano nel corso della dissezione chirurgica a partenza posteriore. Dopo l’introduzione della tecnica retroperitoneale da parte di Gaur nel 1992 (98), la surrenectomia retroperitoneoscopica laterale è stata sempre più utilizzata per pazienti con piccoli tumori surrenalici unilaterali. Uno svantaggio di tale approccio infatti è rappresentato da uno spazio di lavoro leggermente più piccolo e questo limita la dimensione del tumore che può essere rimosso con sicurezza con la LRA. L’approccio retroperitoneale infatti tipicamente non è indicato per tumori di grandi dimensioni (>5cm). Anche se tumori più grandi sono stati rimossi con l’approccio
retroperitoneale, questo è risultato essere associato con un tempo operatorio più lungo e un maggior tasso di conversione alla chirurgia open. La principale ragione è stata l’anatomia non facilmente riconoscibile in presenza di tumori di grande dimensioni, i quali occupavano la maggior parte dello spazio operatorio. Un altro limite dell’approccio retroperitoneale consiste nel fatto che la dissezione della ghiandola surrenalica e l’accesso iniziale alla vena surrenalica sono più difficoltose rispetto all’approccio trans peritoneale, e questo può essere un importante limite nella chirurgia del feocromocitoma dove è fondamentale il precoce isolamento e sezione della vena surrenalica principale. Tuttavia la LRA può essere una procedura più sicura e meno invasiva poiché permette un accesso diretto alla ghiandola surrenalica, senza la limitazione causata dal fegato e dalla milza che si ha nella LTA, che può essere a volte importante e richiedere un’attenta retrazione, specialmente del fegato. In oltre l’approccio retroperitoneale evita l’irritazione del peritoneo, la manipolazione dell’intestino e i potenziali danni agli organi intraaddominali. Si ritiene quindi che possa essere associata a un recupero più rapido della funzione intestinale, potendo quindi portare a una degenza ospedaliera più breve e ricoveri più rapidi. In oltre l’accesso diretto al surrene, senza una dissezione intraaddominale, fa sì che tale approccio possa essere preferibile nei pazienti con una precedente chirurgia addominale. La necessità di lisare le aderenze, di mobilizzare le strutture intraaddominali e la retrazione del fegato e della milza vengono infatti evitati. Come risultato, diverse serie riportano un tempo operatorio più breve con l’approccio retroperitoneale. Sebbene l’obesità rappresenti spesso un problema con l’approccio transperitoneale, questa è meglio tollerata durante la chirurgia retroperitoneale poiché la fossa lombare rimane superficiale e accessibile in questi pazienti.
In modo simile agli altri approcci, anche l’approccio retroperitoneale ha i suoi limiti. Un elemento fondamentale per l’esecuzione della LRA è la familiarità con l’anatomia retroperitoneale che il chirurgo deve possedere, e l’avere una guida per i casi iniziali può essere cruciale per evitare catastrofi. La procedura laparoscopica retroperitoneale richiede una maggiore esperienza tecnica rispetto all’approccio transperitoneale. La learning curve per tale approccio infatti è maggiore rispetto a quella per la tecnica transperitoneale. Secondo Berber et al. (123), questa comprende almeno 20 pazienti. Diversi autori inoltre consigliano di avere una iniziale esperienza con la laparoscopia transperitoneale prima di utilizzare l’approccio retroperitoneale, soprattutto in pazienti obesi (123,124). Altro limite dell’approccio retroperitoneale, oltre al già citato limitato spazio di lavoro che può rendere la dissezione più difficoltosa per i chirurghi poco esperti, è il limitato numero di siti utilizzabili per i trocars, che sono in oltre posti in stretta vicinanza fra loro. Il piccolo spazio disponibile limita quindi
la disposizione degli strumenti e il loro incrocio può verificarsi facilmente (effetto “ferri da calza”). Un altro importante difetto dell’approccio retroperitoneale consiste nel fatto che qualora si verifichi nel corso dell’intervento la lacerazione del peritoneo questo condurrebbe al passaggio dell’aria insufflata all’interno della cavità peritoneale con la conseguente espansione di quest’ultima e come risultato lo spazio di lavoro retroperitoneale diventerebbe estremamente limitato.
Il miglioramento degli strumenti e modifiche alla tecnica hanno aumentato le indicazioni per l’approccio retroperitoneale nel trattamento delle masse solide surrenaliche. L’utilizzo della RLA è indicata nelle lesioni di piccole dimensioni (<6cm) che necessitano quindi di un limitato spazio di dissezione. In tale gruppo rientrano peraltro la maggior parte dei tumori del surrene, sia funzionanti (adenomi cortisolo-secernenti, iperplasia macro e micronodulare cortisolo-secernente, aldosteronomi, feocromocitomi), che non funzionanti (incidentalomi). La maggior parte delle lesioni surrenaliche sono infatti benigne, di piccole dimensioni e localizzate in profondità nello spazio retroperitoneale, lesioni ideali quindi per la loro rimozione mediante un approccio laparoscopico retroperitoneale. Secondo alcuni autori non è presente un limite assoluto di dimensioni per l’approccio laparoscopico retroperitoneale; tuttavia, la rimozione di lesioni surrenaliche di dimensioni maggiori ai 3cm o feocromocitomi di qualsiasi dimensione possono essere considerate procedure maggiormente impegnative e dovrebbero essere tentate solo da chirurghi con una considerevole esperienza laparoscopica(126). Un’altra indicazione al ricorso alla surrenectomia laparoscopica con approccio retroperitoneale comprende la presenza di esiti cicatriziali e/o infiammatori intraperitoneali che controindicano l’approccio laparoscopico transperitoneale. Questo approccio è quindi indicato in pazienti in cui è previsto che siano presenti adesioni intra-addominali a livello dei piani di dissezione perisurrenalici. Questo può verificarsi nei pazienti sottoposti a diversi precedenti interventi addominali o con una incisione nel quadrante superiore ipsilaterale. Secondo alcuni autori (123), procedure laparoscopiche minori, come la colecistectomia laparoscopica, non costituisce una controindicazione all’approccio transperitoneale. Un aspetto che dovrebbe essere tenuto in considerazione nella selezione dei pazienti appropriati per la RLA è la relazione della dodicesima costa con il surrene(123). Quando la ghiandola surrenalica è troppo cefalica in confronto alla dodicesima costa, questo riduce l’accortezza a livello della punta dello strumento laparoscopico rigido e potrebbe rendere difficoltosa la procedura. Controindicazioni alla RLA consistono in lesioni maligne con evidente infiltrazione delle strutture adiacenti (al pari della TLA), e anche lesioni sospette, nelle quali potrebbe essere indicato una tempo esplorativo laparoscopico.
Controindicazioni relative alla RLA comprendono una coagulopatia non corretta, obesità, pielonefrite, un precedente trauma o chirurgia retroperitoneale che potrebbe essere responsabile della presenza di aderenze nel retroperitoneo.
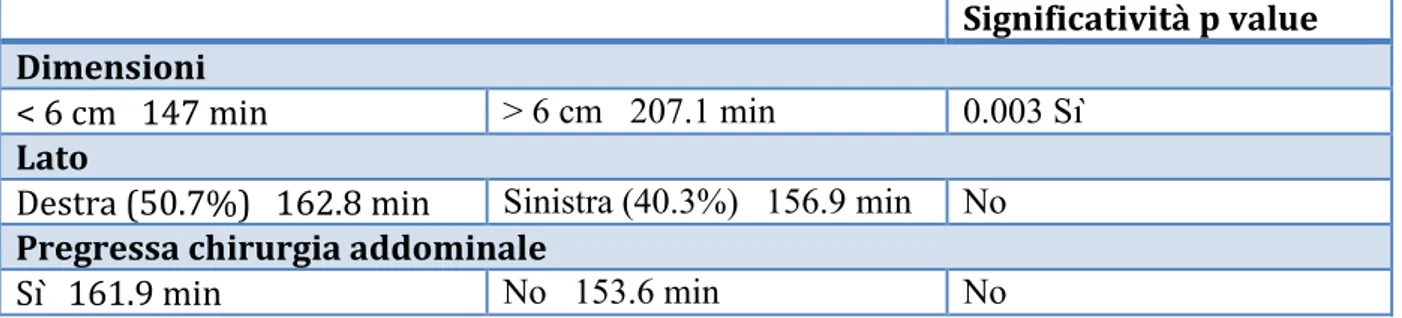
I risultati della surrenectomia laparoscopica retroperitoneale sono in miglioramento, come risultato dell’aumentata familiarità con l’anatomia retroperitoneale. Diversi autori hanno descritto l’efficacia della RLA per tumori surrenalici di piccole dimensioni. Recenti serie riguardo la RLA forniscono una preliminare evidenza che questa tecnica possa infatti essere confrontata favorevolmente con la laparoscopia transperitoneale e la chirurgia open riguardo alla sicurezza, efficacia, outcome e complicanze. Gasman et al. (97) hanno riportato la loro esperienza con 23 pazienti sottoposti alla RLA. Questa serie ha compreso due feocromocitomi e una metastasi surrenalica. La dimensione media delle neoformazioni è risultata 2.6 cm (range 1-4 cm), il tempo operatorio 97 minuti (range 45-160 min), la perdita ematica 70 ml (range 0-400 ml), e la degenza ospedaliera media di 2 giorni. Solamente un paziente ha sviluppato un ematoma retroperitoneale che ha necessitato un prolungamento della degenza ospedaliera. Non si sono verificate altre complicanze e nessuna conversione alla chirurgia open. In questo studio controindicazioni alla RLA hanno compreso lesioni maggiori di 5cm o una precedente incisione lombare. Gli autori hanno attribuito la loro bassa morbidità e il breve tempo operatorio all’approccio retroperitoneale e hanno asserito che questo approccio sia meno traumatico rispetto all’approccio transperitoneale. Bonjer et al. (96) hanno riportato su 111 casi consecutivi di RLA. In questa serie la dimensione del tumore varia da 1 a 8 cm e comprende 19 pazienti con feocromocitoma e 16 pazienti con malattia surrenalica bilaterale. Il tempo operatorio medio per la surrenectomia unilaterale è risultato 114 minuti con una perdita ematica media di 121 ml. Un tempo significativo maggiore è stato necessario per i tumori di dimensioni maggiori ai 6 cm. Il tasso di conversione alla procedura open è stato del 4.2% (cinque pazienti) e la degenza ospedaliera media di 2 giorni. Il tasso di complicanze dell’11% ha compreso tre ematomi e tre infezioni delle vie urinarie. Tre dei 19 pazienti con feocromocitoma hanno sviluppato una temporanea instabilità emodinamica intraoperatoria che è stata gestita con successo con nitroprussiato endovena. Gli autori conclusero che la RLA è sicura e valida nei pazienti con una lesione benigna più piccola di 6 cm. Soulie et al. (128) hanno riportato di 56 RLA con una dimensione media del tumore di 3.2 cm (range 1-6.3 cm), tempo operatorio di 135 minuti (range 75-240 minuti), e una perdita ematica di 80 ml (range 30-200 ml). Si è verificata una sola conversione in un paziente con una storia di pielonefrite e dense adesioni. Le complicanze hanno compreso due complicanze vascolari intraoperatorie, che sono state gestite con successo laparoscopicamente, e un ematoma postoperatorio, gestito
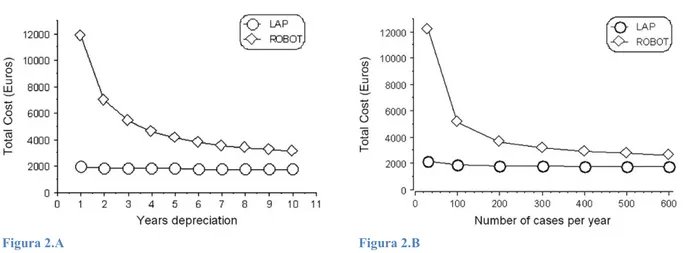
in maniera conservativa. Questa serie ha compreso 13 pazienti con feocromocitoma, quattro dei quali hanno sviluppato una temporaneo instabilità emodinamica intraoperatoria, efficacemente trattata con nicardipina intravenosa. In base ai loro risultati, gli autori hanno enfatizzato la sicurezza e validità della RLA per lesioni più piccole di 7 cm e hanno attribuito il breve tempo operatorio all’approccio diretto retroperitoneale. Salomon et al. (129) hanno riportato su 115 surrenectomie laparoscopiche retroperitoneali. La dimensione media del tumore era di 3.1 cm (range 1-6.5 cm), il tempo operatorio 118 minuti (range 45-240 min), e la perdita ematica di 77 ml. C’è stata solo una conversione alla chirurgia open in un paziente con una storia di pielonefrite. Queste serie sulla RLA suggeriscono che l’approccio retroperitoneale sia comparabile con l’approccio transperitoneale riguardo al tempo operatorio e la perdita ematica. Il tasso di morbidità è simile o inferiore e il tasso di conversione alla chirurgia open sembra essere simile nei due approcci. Rubinstein et al.(122) hanno eseguito uno studio prospettico randomizzato confrontando 25 pazienti sottoposti alla surrenectomia laparoscopica transperitoneale e 32 operati con l’approccio retroperitoneoscopico. Questo studio ha dimostrato che non era presente una differenza significativa tra i due approcci in termini di tempo operatorio, perdita di sangue intraoperatoria e percentuale di complicanze. I due gruppi inoltre sono risultati simili in termini di necessità di analgesia, ripresa della deambulazione e dell’alimentazione orale, e durata della degenza postoperatoria. Questi autori hanno osservato come, in contrasto con la loro idea e di altri autori, l’approccio transperitoneale non è risultato associato con una maggiore incidenza di ileo paralitico o una maggiore degenza ospedaliera. Tuttavia la convalescenza è risultata significativamente più rapida nel pazienti sottoposti all’approccio retroperitoneale (da 2 a 3 settimane contro 4.7 settimane, p=0.02). Berber et al. (123), confrontando 69 pazienti sottoposti alla LTA con 90 pazienti sottoposti alla PRA hanno osservato come nel secondo gruppo la perdita di sangue e il tempo operatorio sono risultati inferiori (35ml vs 25ml e 157min vs 137min, rispettivamente). In oltre la degenza ospedaliera è risultata essere leggermente minore nei pazienti sottoposti alla PRA. Guazzoni et al. (23) hanno eseguita una meta-analisi nel corso della quale hanno anche confrontato i due approcci laparoscopici, transperitoneale e retroperitoneoscopico. Sono stati valutati i seguenti parametri: durata media dell’intervento (minuti), conversione alla chirurgia open, trasfusione, degenza ospedaliera e complicanze verificatesi durante e dopo l’intervento. I dati sono riportati in tabella.
N. di casi Tempo operatorio Conversione alla Trasfusione (%) Degenza postoperatoria Complicanze (%)
(min) chirurgia open (%)
(giorni)
Approccio trans peritoneale
DeCanniere et al. 1997 54 80 4 1.8 4 1.8 Filipponi et al. 1998 50 111 0 0 2.5 0 Gagner et al. 1997 97* 123 3 2 2.7 12 Guazzoni et al. 2001 145 160 2.7 3 2.8 5.5 Henry et al. 2000 169 129 5 0.5 5.4 7.5 Ishikawa et al. 2000 55 143 0 0 - 0 Lezoche et al. 2000 108+ NA 0.9 0 2.5 1.9 Porpiglia et al. 2001 72 135 4 - - 8 Schichman et al. 1999 50 217 0 2 3 10 Terachi et al. 1997 100 240 3 0 - 0 Approccio retroperitoneale Siperstein et al. 2000 31 176 0 0 1.4 10 Bonjer et al. 2000 111 114 4.5 0 2 11 Walz et al. 2001 142 101 5 0 3 13 Salomon et al. 2001 115 118 0.8 - 4 12.1
Tabella X, Casi relativi all’approccio transperitoneale e retroperitoneale per la surrenectomia laparoscopica. * Otto casi sono stati bilaterali; + Sei casi sono stati bilaterali
Si può osservare come la durata dell’intervento risulti leggermente maggiore nell’approccio transperitoneale (148.6 vs 127.25 min), mentre la percentuale di conversione alla chirurgia open è leggermente minore nell’approccio transperitoneale (2.26 vs 2.57%). La percentuale di trasfusione può essere considerata trascurabile in entrambi i gruppi (1% nella tecnica transperitoneale e 0% in quella retroperitoneoscopica). Esiste invece una certa differenza nella durata della degenza ospedaliera, cioè circa 1 giorno in più nel caso della chirurgia
transperitoneale (3.27 vs 2.6). Questo potrebbe essere legato al dolore o al fastidio addominale descritto dai pazienti sottoposti alla laparoscopia transperitoneale, come conseguenza o dell’insufflazione intraperitoneale di CO2 o della mobilizzazione dell’intestino. Si può anche osservare una differenza tra i due gruppi per la percentuale di complicanze, maggiore nel gruppo sottoposti all’approccio retroperitoneoscopico (4.7 vs 11.3%). Questo è probabilmente il risultato di una dei seguenti tre fattori: una minore familiarità con l’anatomia dello spazio retroperitoneale da parte del chirurgo nella fase iniziale dell’utilizzo di questo approccio; uno spazio di lavoro limitato; e che ci sono meno accessi disponibili rispetto all’approccio transperitoneale.
Da tutti questi studi tuttavia si evince come non possa essere dimostrata la chiara superiorità di un approccio rispetto agli altri. Ognuno ha dei specifici vantaggi e svantaggi. L’approccio LT e l’approccio PR possono quindi essere considerati complementari l’un l’altro, non in concorrenza fra loro, quando vengono seguiti dei determinati criteri di selezione dei pazienti nella scelta del tipo di approccio da utilizzare.
Le caratteristiche dei tre differenti approcci per la surrenectomia endoscopica sono riportate in tabella.
Caratteristica ATA LTA LRA
Spazio di lavoro Ampio Ampio Piccolo Identificazione del
surrene
Facile Ottima Difficile
Accesso iniziale alla vena surrenalica
Molto facile Facile Difficile
Danno agli organi Raro Molto raro Molto raro Adesioni intestinali Occasionale Occasionale Nessuna Convalescenza Buona Buona Eccellente
Gumbs e Gagner, in un articolo del 2006, hanno eseguito una review delle serie pubblicate più grandi, comprendenti almeno 100 casi di LA (112). In totale, sono stati riportati 2565 casi. Essi hanno osservato come la maggior parte dei centri (70%) ha eseguito la surrenectomia laparoscopica transperitoneale laterale, mentre nel 20% dei casi è stata eseguita la surrenectomia endoscopica retroperitoneale posteriore, e meno frequentemente la surrenectomia laparoscopica transperitoneale anteriore. Quest’ultima generalmente richiede una maggiore dissezione in confronto alla LTA, e molti studi riportano una maggiore durata
del tempo operatorio. Anche se alcuni studi riportano una maggiore sanguinamento e una maggiore durata di degenza con la ATA, altri autori invece non riportano delle differenze statisticamente significative. Nell’ ampia casistica di 2565 casi il tempo operatorio medio è di 137 minuti (65-240 minuti). Il valore medio della stima della perdita di sangue è di 81 ml (20-106 ml). La durata di degenza media è di 3.3 giorni (1-5.8 giorni). La conversione alla procedura open si è verificato approssimativamente nel 2% dei casi, con un range di 0-13%, ed è stato riportato in tutti le casistiche, eccetto una. La principale indicazione per la conversione è risultato un incontrollato sanguinamento che nella maggior parte dei casi originava dai vasi più piccoli, ma che includeva anche un danno alla vena cava inferiore o vasi renali, soprattutto la vena renale sinistra. La seconda causa più frequente di conversione a una tecnica open è risultata la presenza di una lesione maligna con il riscontro all’esplorazione laparoscopica della presenza di invasione locale e vascolare. Altre motivi citati per la conversione alla tecnica open comprendono adesioni, obesità, danno a organi, ernia diaframmatica, fegato di grande dimensioni e tumori benigni di grande dimensioni. Il tasso di mortalità è risultato 0.2% a 30 giorni dall’intervento, con 15 centri che riportano nessuna mortalità e i rimanenti quattro una mortalità dello 0.8-1.2%. Le cause di morte dopo la LA comprendevano emorragia massiva, pancreatite necrotizzante, embolia polmonare, sepsi e insufficienza cardiopolmonare.
Studio No. di procedure Approccio Tempo operatorio (min) Perdita di sangue (ml) Tasso di conversione (%) Tasso di complicanze (%) Durata di degenza Mortalità (%) Gagner et al. 1997 100 LTA 123 70 3 12 2.4 0 Terachi et al. 1997 100 36ATA 240 77 3 12 NR 0 Heniford et al. 1999 110 LTA 188 125 2.7 16 1.9 0 Mancini et al. 1999 172 LTA 132 NR 7 8.7 5.8 1.2 Lezoche et al. 2000 108 ATA 99 NR 1 2.9 2.5 0.9 Henry et al. 2000 169 LTA 129 NR 5 7.5 5.4 0 Guazzoni et al. 2000 161 LTA 160 NR 2.5 5.1 2.8 0 Salomon et 115 REA 118 77 0.8 15.5 4 0
al. 2001 Suzuki et al. 2001 118 46 ATA 32 LTA 166 92 5 12.7 4.6 0 Miccoli et al. 2002 137 NR 111 NR 4.3 3.9 3.8 0 Porpiglia et al. 2002 125 LTA 139 100 3.2 11.2 4 0.8 Chiu 2003 120 REA 100-210 20-100 5 NR 2 0 O’Boyle et al. 2003 172 TA 65 80 7 5 3 0 Zeh et al. 2003 100 TA NR NR 13 6 1 0 Prager et al. 2004 102 TA NR NR 5 9 NR 0 Walz et al. 2004 325 REA 80 33 <1 14.5 NR 0 Poulouse et al. 2005 100 TA 150 NR 1 14 2.6 1 Naya et al. 2005 127 TA 179 53 0 NR NR 0 Ramacciato et al. 2005 104 TA/REA 108 106 4.8 4.8 NR 0 Total Mean 2565 137 81 2 8.9 3.3 0.2
Guazzoni et al. (23) hanno eseguito una meta-analisi di studi che confrontano la surrenectomia laparoscopica con la surrenectomia open.
N. di casi Tempo operatorio (min) Transfus. (%) Sanguinamento intraoperatorio (ml) Degenza postoperat. (giorni) Complicanze (%)
LA Open LA Open LA Open LA Open LA Open LA Open
Dudley et al. 1999 36 23 158 85 5.5 8.6 194 426 3.5 8.5 5.5 52 Hazzan et al. 2001 28 24 188 139 - - 4 7.5 16 39 Imai et al. 1999 41 40 180 127 2.4 2.5 40 162 12 18 0.5 50
Liao et al. 2001 31 21 203 123 0 0 71 124 4.9 7.6 Linos et al. 1997 18 147 116 155+ 108* 5.5 6.1 - 2.2 8+ 4.5* 0 13.9+ 9.8* Thompson et al. 1997 50 50 167 127 4 0 - - 3.1 5.7 6 18 Vargas et al. 1997 20 20 193 178 5 15 245 283 3.1 7.2 10 25 Winfield et al. 1998 21 17 219 140 0 5.8 183 266 2.7 6.2 14 5.8
Tabella X, Studi comparativi tra la surrenectomia open e la surrenectomia laparoscopica. + approccio anteriore; * approccio posteriore
Dalla tabella si evince come la laparoscopia, quando confrontata con la surrenectomia open, può talvolta necessitare di una maggiore durata dell’intervento, tuttavia la perdita di sangue, la durata della degenza postoperatoria, le complicanze sono minori nel gruppo della laparoscopia.
1.3 Indicazioni e controindicazioni
All’inizio degli anni ’90 le indicazioni per la LA comprendeva lesioni benigne di piccole dimensioni, mentre le lesioni più grandi o il feocromocitoma venivano approcciati laparoscopicamente con molta cautela, e lesioni maligne erano considerate una controindicazione assoluta (23). Le indicazioni alla LA comprendevano alcuni condizioni quali adenoma aldosterone-secernente, sindrome di Cushing, adenomi non funzionanti e altre rare patologie come cisti surrenaliche e mielolipoma. Gruppi a favore della chirurgia laparoscopica guadagnarono rapidamente esperienza e molte controindicazioni iniziali (come obesità, feocromocitoma, grandi neoformazioni surrenaliche, una precedente chirurgia addominale e una neoformazione maligna) furono dimostrati essere non controindicazioni assolute, ma piuttosto legate alla abilità del team chirurgico.
Frazeli-Matin et al. (130) ha riportato che la LA era migliore della tradizionale chirurgia laparotomica in un gruppo di pazienti con obesità patologica. In questi soggetti la laparoscopia causò meno complicanze, un più basso tasso di morbilità e fu più veloce della
chirurgia open. Tuttavia, la laparoscopia in pazienti patologicamente obesi dovrebbe essere considerata un intervento più impegnativo rispetto a pazienti con un normale IBM e dovrebbe essere riservata a quei chirurghi con una grande esperienza con la LA.
Il feocromocitoma inizialmente veniva considerato una controindicazione alla laparoscopia. La produzione delle catecolamine da parte del feocromocitoma può rendere difficile il trattamento chirurgico per il rischio di importanti complicanze quali un episodio ipertensivo acuto causato dalla manipolazione del tumore o un’improvvisa ipotensione immediatamente dopo la legatura della vena surrenalica(68). La rimozione chirurgica del feocromocitoma richiede quindi una meticolosa tecnica operativa poiché una eccessiva manipolazione del tumore può portare a un rilascio di catecolamine e una conseguente instabilità emodinamica. Inizialmente alcuni chirurghi non erano sicuri se questa procedura potesse essere eseguita con l’approccio laparoscopico. Erano presenti anche alcuni dubbi su potenziali cambiamenti emodinamici che potevano verificarsi nel corso dell’induzione dello pneumoperitoneo con CO2. In oltre, alcuni ritenevano che l’assorbimento della CO2, producendo una acidosi
metabolica, potesse avere un effetto avverso sul miocardio già esposto a elevati livelli di catecolamine(67). Tuttavia con il crescere dell’esperienza con questa tecnica si è visto che tutti questi dubbi erano infondati e oggi è accettato che la surrenectomia laparoscopica possa essere eseguita con sicurezza e con efficacia nella chirurgia del feocromocitoma. I punti chiave per un trattamento chirurgico efficace del feocromocitoma consistono nell’accurata localizzazione del tumore, la preparazione preoperatoria, la gestione anestesiologica intensiva e la tecnica chirurgica di resezione con una minima manipolazione del tumore(73). Grazie alle indagini di imaging, quali la TC, MRI e la scintigrafia con MIBG, la localizzazione preoperatoria del tumore è diventato più accurata rispetto al passato(71). Il miglioramento della capacità di localizzare il tumore con successo prima della chirurgia ha contribuito all’accettazione dell’approccio laparoscopico. Nella chirurgia open infatti è possibile eseguire la palpazione del surrene controlaterale e della catena del simpatico per identificare possibili altre lesioni. La posizione in decubito laterale permette invece un approccio diretto a una sola ghiandola surrenalica(71) e l’esposizione del retroperitoneo può non essere così completo come nell’approccio open e tumori bilaterali possono verificarsi nel circa 10% dei casi(73). La preparazione preoperatoria nella chirurgia del surrene è fondamentale. L’induzione dell’anestesia prima della chirurgia, la manipolazione del tumore e le manovre per l’isolamento della neoformazione possono provocare un rilascio massivo di catecolamine da parte del tumore, potendo causare una crisi ipertensiva, un ictus, un’aritmia o un infarto del miocardio. Per prevenire questi problemi, i pazienti con feocromocitoma devono essere
sottoposti a un blocco farmacologico della sintesi delle catecolamine o dei loro effetti prima della chirurgia. Prima dell’introduzione del blocco adrenergico, il tasso di mortalità per la chirurgia del feocromocitoma variava dal 24% al 50% (61). Con un adeguato pretrattamento, la mortalità perioperatoria si è ridotta a meno del 3% (60). L’uso di fenossibenzamina, un alfa-bloccante, si oppone alla vasocostrizione indotta dalle catecolamine. Più recentemente altri farmaci alfa-bloccanti, come la prazosina, sono preferiti alla fenossibenzamina perché dotati della stessa efficacia ma con minori effetti collaterali. È utilizzato anche un bloccante per trattare la tachicardia riflessa spesso associata all’alfa-bloccante. Il solo beta-bloccante può essere pericoloso per i pazienti con feocromocitoma ed è controindicato in questa situazione poiché non previene e può accentuare l’effetto delle catecolamine sui recettori alfa-adrenergici. La combinazione di un alfa-bloccante, di un beta-bloccante e una introduzione libera di sale è iniziata 10-14 giorni prima dell’intervento e questo porta a un miglior controllo della pressione arteriosa e riduce il rischio chirurgico. Questo blocco farmacologico combinato permette inoltre il rilasciamento dell’albero vascolare costretto e l’espansione del ridotto volume plasmatico, prevenendo così lo shock dopo l’improvvisa vasodilatazione diffusa al momento della rimozione del tumore. Durante un intervento in laparoscopia l’insufflazione di CO2 causa un aumento della pressione intraaddominale e un
aumento dell’assorbimento di CO2, provocando una riduzione del ritorno venoso, una
ipercapnia e acidosi metabolica, un aumento delle resistenze vascolari sistemiche, una caduta dell’indice cardiaco e un aumento della pressione arteriosa media (MAP)(71). Generalmente questi cambiamenti sono ben tollerati dalla maggior parte dei pazienti, ma in quei pazienti con feocromocitoma gli effetti dello pneumoperitoneo non erano completamente noti (72). Alcuni autori hanno osservato che gli effetti emodinamici associati all’induzione dello pneumoperitoneo erano molto più importanti nel caso di feocromocitoma(68). Il meccanismo responsabile dell’eccessivo rilascio di catecolamine si pensa essere legato non solo al rilascio di catecolamine causato dall’aumento della pressione intraaddominale e dall’aumento del tono simpatico legato all’ipercapnia, ma anche alla diretta compressione meccanica del tumore da parte dello pneumoperitoneo (59). Si pensava inizialmente che lo pneumoperitoneo potesse essere causa di un rilascio significativo di catecolamine. Tuttavia si è visto come l’induzione dello pneumoperitoneo non fosse associato a un importante secrezione di catecolamine(73). Inabnet et al. hanno osservato come durante l’induzione dello pneumoperitoneo si verificasse solamente un significativo aumento della MAP, con un aumento della pressione venosa centrale e della pressione di riempimento capillare polmonare. Tuttavia queste alterazioni emodinamiche avevano un minimo significato clinico, poiché l’indice cardiaco e l’indice di
lavoro del ventricolo destro non erano compromessi in nessuna momento durante lo studio (72,73). Nei vari studi quindi non è stato riportato un aumento significativo degli episodi ipertensivi durante l’induzione dello pneumoperitoneo, e quando questi si verificano non sono più gravi e più difficili da trattare farmacologicamente rispetto a quanto avviene nella procedura open. È infatti la manipolazione del tumore la causa del maggiore aumento dei livelli plasmatici delle catecolamine. Durante l’intervento di surrenectomia open per feocromocitoma, è stato chiaramente dimostrato come la manipolazione del tumore sia associato a un marcato aumento del livello delle catecolamine circolanti (72) (vedi FigA).
Figura A Incremento dei livelli di Epinefrina e Norepinefrina nelle diverse fasi dell'intervento.
Anche durante l’approccio laparoscopico i livelli delle catecolamine circolanti aumentano, ma in misura minore rispetto a quanto si osserva nella chirurgia open (71). Il maggior aumento del livello plasmatico delle catecolamine nel corso della LA per feocromocitoma si verifica durante la dissezione del tumore. Fernandez-Cruz et al. hanno osservato come in questa fase dell’intervento si verificasse un aumento di 17.4 volte dei livelli plasmatici di adrenalina, in confronto all’aumento di 34.2 volte con l’approccio open (p=0,03), e un aumento della noradrenalina rispettivamente di 8.62 e 13.7 volte (p=0.01) (71). In oltre hanno anche osservato una maggiore incidenza di ipertensione, tachicardia e instabilità cardiovascolare nei pazienti sottoposti alla surrenectomia open, soprattutto durante la manipolazione del tumore, in contrasto con la stabilità cardiovascolare mantenuta durante l’approccio laparoscopico. Una dissezione con una minima manipolazione della neoformazione è molto importante nei tumori secernenti.
L’ottimale magnificazione e l’elevata risoluzione dell’approccio laparoscopico permette di eseguire una dissezione con alta precisione, con una emostasi quasi perfetta e un minimo trauma dei tessuti. Una tecnica paziente e meticolosa è fondamentale durante la divisione di tutte le vene che drenano il tumore per evitare un eccessivo rilascio di catecolamine in circolo (71). La legatura della vena surrenalica prima della manipolazione del tumore è stata raccomandata da diversi autori. La laparoscopia permette una migliore visualizzazione e un più rapido accesso alla vena surrenalica, riducendo ulteriormente il rischio del rilascio di catecolamine (76). Vari autori hanno osservato come il disconnettere precocemente il tumore dal principale drenaggio venoso evitava episodi di ipertensione durante la manipolazione del feocromocitoma nel corso della dissezione del tumore stesso dal tessuto circostante (68). In passato, il limite superiore per la resezione del feocromocitoma era di 6 cm. Tuttavia, con l’aumentare dell’esperienza, diversi centri oggi riportano rimozioni di feocromocitomi fino a 11cm di dimensioni. In un confronto tra 90 feocromocitomi maligni e 60 benigni, non è stata notata una differenza significativa per quanto riguarda la dimensione media del tumore tra il gruppo con lesione maligna e il gruppo con lesione benigna. In oltre i feocromocitomi con invasione locale sono risultati essere significativamente più piccoli rispetto a quelli con malattia a distanza(112). Come conseguenza, molti autori attualmente considerano come benigni tutti i feocromocitomi che non risultano maligni preoperatoriamente, da trattare laparoscopicamente anche se di dimensioni maggiori ai 10cm di diametro. Se c’è una evidenza della presenza di invasione locale, è raccomandato che la procedura venga convertita a una procedura assisted o un approccio open. La conversione alla procedura hand-assisted o open per un feocromocitoma maligno è consigliato perché sono riportati casi di recidiva dopo la LA, che si verificano per un aumentato rischio di frammentazione del tumore con il conseguente spillage, e per la difficoltà tecnica nel rimuovere la malattia localmente invasiva con la chirurgia miniinvasiva(112).
Il ruolo della laparoscopia nel trattamento di grandi neoformazioni surrenaliche e di tumori maligni è controverso. Un tumore di grandi dimensioni generalmente è definito come un tumore di diametro superiore ai 6 cm. Fortunatamente, tumori di queste dimensioni rappresentano una percentuale relativamente piccola di tutte le lesioni surrenaliche. Tumori surrenalici benigni, che possono raggiungere dimensioni superiori ai 6 cm includono feocromocitoma, mielolipoma, cisti e adenomi atipici. Tuttavia le masse surrenaliche maggiori di 6 cm di diametro possono rivelarsi all’esame istopatologico una lesiona maligna non riconosciuta: in questi pazienti un approccio laparoscopico potrebbe favorire una
diffusione delle cellule neoplastiche a livello intraperitoneale o degli accessi laparoscopici. Anche se è possibile rimuovere laparoscopicamente tumori larghi 15 cm, queste sono procedure tecnicamente più impegnative a causa delle dimensioni del tumore, l’aumentata vascolarizzazione, e la maggiore difficoltà con la retrazione e la manipolazione del tumore. Con l’aumentare delle dimensioni della neoformazione surrenalica, si ha un aumento delle difficoltà tecniche e dei rischi operatori associati alla sua rimozione. Queste è particolarmente vero per lesioni interessanti il surrene destro, dove lesioni di grandi dimensioni spesso crescono dietro la vena cava inferiore, rappresentando quindi una sfida laparoscopica. La rimozione laparoscopica di questi tumori in oltre comporta o la morcellazione del surrene o il creare una larga incisione per l’estrazione del pezzo operatorio. Un ulteriore fatto da considerare è che, poiché neoformazioni surrenaliche di grandi dimensioni sono poco comuni, l’esperienza del chirurgo con lesioni di tali dimensioni, al di fuori dei centri di riferimento, può essere limitata. Un aspetto importante da tenere in considerazione è che neoformazioni di grandi dimensioni presentano un aumentato rischio di malignità. Diverse variabili sono state associate con un aumentato rischio di carcinoma surrenalico primitivo. Età avanzata, tumori virilizzanti, evidenza di necrosi e di eterogeneità nell’imaging preoperatorio aumentano il rischio che la neoformazione sia maligna. In assenza di invasività locale, il più importante fattore è la dimensione del tumore, perché lesioni surrenaliche maggiori di 6 cm di diametro sono molto più probabilmente maligne. Questa relazione tra dimensioni del tumore e malignità è meno evidente nel feocromocitoma, poiché molti feocromocitomi di grandi dimensioni clinicamente si comportano come lesioni benigne. In fine, quando l’elemento dimensione è soppesato nella decisione dell’approccio per la surrenectomia, va considerato che le dimensioni riportate dall’imaging possono sottostimare la reale dimensione della massa surrenalica. Alcuni autori suggeriscono ancora che pazienti con lesioni surrenaliche benigne maggiori di 5-6 cm non dovrebbero essere trattati laparoscopicamente a causa del tempo operatorio più lungo e dell’elevato rischio di sanguinamento dovuto ai numerosi vasi che circondano la neoplasia. Recenti articoli, d’altro canto, dimostrano che la surrenectomia laparoscopica per tumori benigni di grandi dimensioni, scoperti radiologicamente, è tecnicamente possibile e sicura. Questi studi dimostrano che non è presente una correlazione tra dimensione e perdita di sangue, tasso di morbilità e mortalità, e durata del ricovero post-operatorio. Porpiglia ha dimostrato solamente una lieve correlazione tra dimensione e tempo operatorio. Il rischio reale nel trattare laparoscopicamente lesioni maggiori di 6 cm è la possibilità di trattare un carcinoma corticosurrenalico non riconosciuto. Ross e Aron hanno calcolato che, senza l’evidenza radiologica di malignità, meno di 1 su 10,000 lesioni
surrenaliche minori di 6 cm potrebbero essere carcinomi, e che tale probabilità è del 35-98% in masse maggiori di 6 cm. Diversi centri hanno riportato piccole serie di pazienti con neoformazione surrenalica di grandi dimensioni o maligna o potenzialmente maligna che è stata asportata laparoscopicamente.
Il tasso di conversione alla surrenectomia laparotomia varia dallo 0% al 14%, e molti dei casi convertiti hanno interessato pazienti con tumore maligno. Le dimensioni medie in questi reports vanno da 4,5 a 8 cm, e la percentuale di lesioni maligne va dal valore più basso di 12,5% nella casistica di Henry et al. alla percentuale del 100% nelle serie su metastasi surrenaliche. Il carcinoma corticosurrenalico primitivo, con una sopravvivenza a cinque anni che va dal 16 al 60%, presenta un alto tasso di recidiva locale. Tuttavia, risultati presenti in letteratura dicono come dopo resezione di un ACC, il tasso di recidiva locoregionale e il tasso di sopravvivenza libero da malattia dopo intervento laparoscopico è simile all’intervento di surrenectomia laparotomica. Nella serie di Kebebew et al. cinque pazienti con un insospettato carcinoma corticosurrenalico sono stati sottoposti a surrenectomia laparoscopica, i cui margini risultarono negativi. Di questi cinque pazienti, tre successivamente presentarono una recidiva locale o regionale che ha necessitato di un intervento open per la resezione. Poiché tutti e tre i pazienti erano stati sottoposti a una resezione con margini negativi, non è stato chiaro se la recidiva fosse legata all’approccio chirurgico o alla biologia del tumore. Kebebew ha osservato come il tasso di recidiva locoregionale del 60% era simile al tasso di recidiva locoregionale riportato per la surrenectomia laparotomica. Kebebew et al., in oltre, analizzando una serie di 20 surrenectomie laparoscopiche eseguite per sospetta e non sospetta lesione surrenalica maligna, hanno descritto un tasso di sopravvivenza libera da malattia del 65% in un follow-up medio di 3.3 anni. Henry et al. hanno riportato una serie di LA per tumori maggiori di 6cm che comprende sei casi di ACC. A un follow-up medio di 35 mesi solamente un paziente era deceduto, e gli altri cinque risultavano liberi da malattia. Henry, tuttavia, suggerì che il principale rischio durante la dissezione laparoscopica di una massa surrenalica potenzialmente maligna è la rottura della capsula; infatti, una volta che la capsula è stata violata, se la lesione surrenalica è un ACC o una metastasi, c’è un alto rischio di disseminazione intra-addominale di cellule neoplasiche. La stessa conclusione era stata data da Sturgeon et al., che suggerì di cominciare quasi tutte le operazioni surrenaliche laparoscopicamente allo scopo di individuare una inattesa malattia metastatica intra-addominale; aggiunse anche che se qualora sia presente l’evidenza di adesione del tumore, di invasione, linfadenopatia o una difficoltà nella dissezione che può comportare un rischio di incompleta resezione del tumore, è raccomandata la conversione alla chirurgia laparotomica o