MATERIALI E METODI
Dal Marzo 2007 al Dicembre 2012, presso l’U.O. di Chirurgia Vascolare dell’Azienda Ospedaliero Universitaria Pisana, sono stati trattati elettivamente 740 pazienti con patologia aneurismatica del distretto aortoiliaco di cui 573 (77,4%) con CO e 167 (22,6%) con EVAR.
Le diverse tipologie di intervento CO sono state: minilaparotomia in 380 casi (51,4%), HALS in 106 casi (14,3%) e accesso retroperitoneale lombotomico sinistro in 87 casi (11,8%).
I dati sono stati estrapolati da un’analisi retrospettiva delle cartelle cliniche dei pazienti sottoposti ad endoprotesi e raccolti in un database dedicato (Microsoft Excel®) includendo le caratteristiche demografiche, le comorbidità presenti, la classe di rischio anestesiologica (ASA), le caratteristiche morfologiche dell’aneurisma derivate dallo studio AngioTc, il tipo endoprotesi, la morbilità e la mortalità a 30 giorni ed il follow-‐up.
Caratteristiche demografiche, cliniche e studio preoperatorio
I pazienti comprendevano 161 maschi (96,4%) e 6 femmine (3,6%) con una età media di 75 + 7,13 anni (range 55-‐92 anni).
Tutti i pazienti sono stati sottoposti come protocollo preoperatorio a valutazione cardiologica con Eco Cardio, RX Torace, Prove di funzionalità respiratoria con eventuale valutazione pneumologica, Eco color Doppler dei vasi cerebroafferenti.
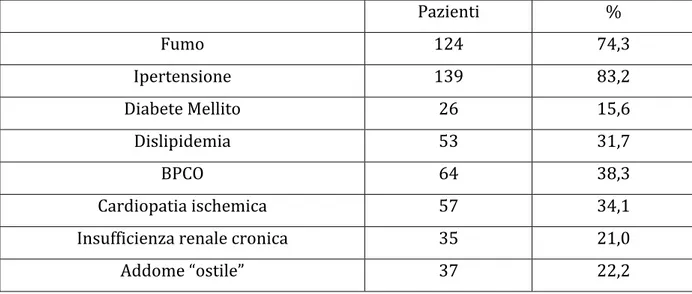
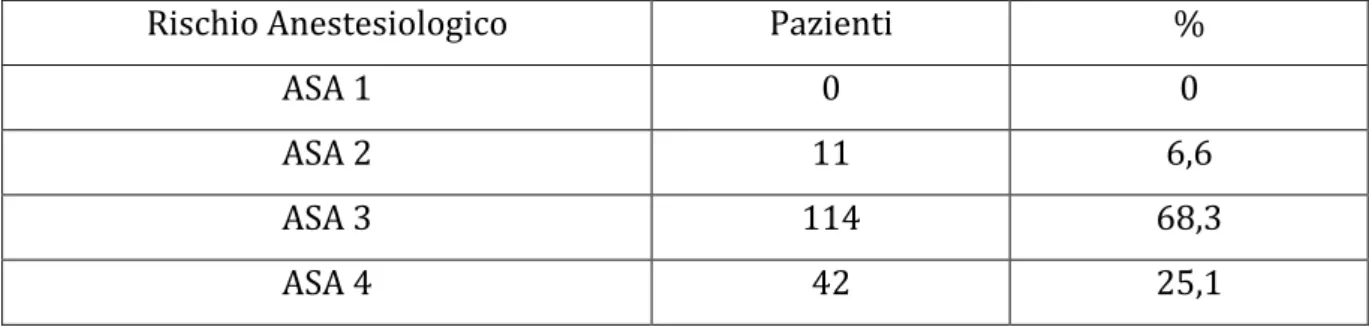
I fattori di rischio, la presenza di addome “ostile” (pregressa chirurgia addominale maggiore sottomesocolica, presenza di colostomie ed urostomie, pregressa radioterapia, marcata obesità), le morbilità associate e il rischio anestesiologico secondo l’American Society of Anesthesiology (ASA) sono riportati nella Tabella 1 e 2.
Pazienti % Fumo 124 74,3 Ipertensione 139 83,2 Diabete Mellito 26 15,6 Dislipidemia 53 31,7 BPCO 64 38,3 Cardiopatia ischemica 57 34,1
Insufficienza renale cronica 35 21,0
Addome “ostile” 37 22,2
Rischio Anestesiologico Pazienti %
ASA 1 0 0
ASA 2 11 6,6
ASA 3 114 68,3
ASA 4 42 25,1
Tabella 2 Rischio anestesiologico (ASA)
L’imaging preoperatorio è consistito nell’AngioTc spirale con ricostruzioni digitali (MPR, Volume Rendering e Vessel Analysis) utilizzando i software di ricostruzione vascolare Osirix® e Terarecon®. Mediante la vessel analysis è stata creata la center lumen line dell’aorta e degli assi iliaci e su di essa sono state effettuate le misurazioni dei diametri e delle lunghezze. Attraverso l’utilizzo di ricostruzioni multiplanari e volumetriche è stato creato un modello 3D dell’aneurisma su cui sono state valutate le angolazioni e le tortuosità dei vasi.
Tutte le misurazioni ottenute sono state coerenti con il Society for Vascular Surgery Reporting Standard[37].
Scelta terapeutica e dettagli operatori
I pazienti sottoposti ad EVAR presentavano: -‐ AAA in 129 pazienti (77,2%),
-‐ AAA associato ad aneurisma iliaco in 19 pazienti (11,4%),
-‐ ectasia dell’aorta addominale associato ad aneurisma dell’arteria iliaca in 17 pazienti (10,2%),
-‐ aneurisma paraanastomotico in pregressa chirurgia aortica in 2 pazienti (1,2%).
Gli AAA con morfologia sacciforme hanno rappresentato il 9,3% del totale degli AAA (12 pazienti).
La valutazione delle caratteristiche morfologiche dell’AAA, per l’idoneità al trattamento EVAR, è stata effettuata in base alle indicazioni presenti nelle linee guida e nelle IFU dei vari dispositivi in commercio (vedi
Cap. Trattamento endovascolare) (Tab.3).
La valutazione clinica ha permesso di identificare pazienti ad alto e basso rischio operatorio secondo la stadiazione ASA.
L’EVAR è stato proposto prevalentemente a pazienti ad alto rischio operatorio (ASA 3 e ASA 4). La presenza di un addome “ostile” o la richiesta esplicita del paziente (prevalentemente per il minor rischio di disfunzione sessuale) sono state discriminanti nell’indirizzare il paziente, anche a basso rischio, verso il trattamento EVAR (Tab 1-‐2).
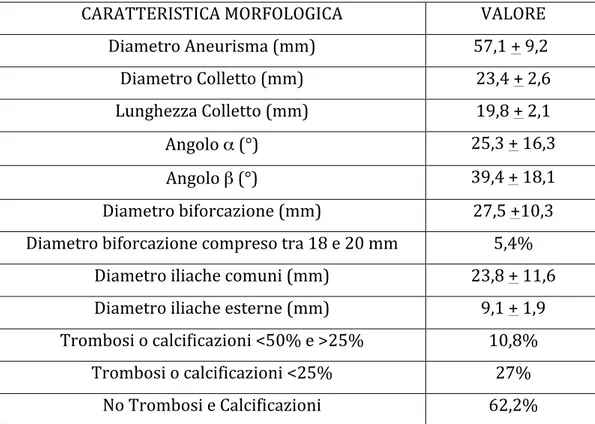
CARATTERISTICA MORFOLOGICA VALORE
Diametro Aneurisma (mm) 57,1 + 9,2 Diametro Colletto (mm) 23,4 + 2,6 Lunghezza Colletto (mm) 19,8 + 2,1 Angolo α (°) 25,3 + 16,3 Angolo β (°) 39,4 + 18,1 Diametro biforcazione (mm) 27,5 +10,3 Diametro biforcazione compreso tra 18 e 20 mm 5,4%
Diametro iliache comuni (mm) 23,8 + 11,6 Diametro iliache esterne (mm) 9,1 + 1,9 Trombosi o calcificazioni <50% e >25% 10,8%
Trombosi o calcificazioni <25% 27% No Trombosi e Calcificazioni 62,2%
Tabella 3. Caratteristiche morfologiche AAA
Valutando la percentuale di pazienti trattati con EVAR nel corso del periodo di studio abbiamo osservato un progressivo aumento dal 17,6% del 2007 al 30,8% del 2012 (Graf. 2).
Grafico 2. Percentuale di pazienti sottoposti a trattamento CO/EVAR
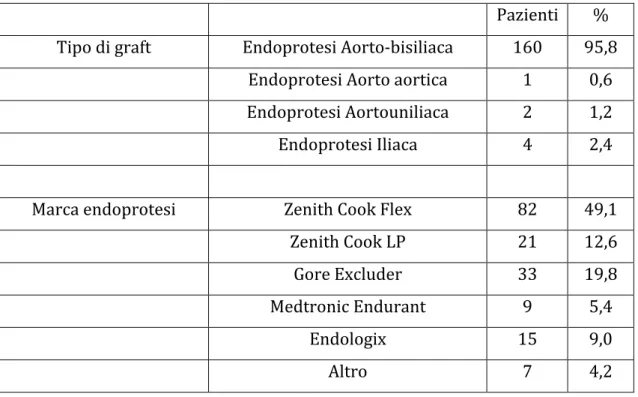
La scelta del tipo di endoprotesi si è basata sull’esigenza di raggiungere la maggiore esperienza possibile con un numero ristretto di device. Le protesi utilizzate sono state (Fig.13-‐14, Tabella 4):
-‐ la Zenith Cook Flex, protesi con aggancio soprarenale modulare con stent in acciaio
-‐ la Zenith Cook Low Profile, protesi con aggancio soprarenale modulare con stent in nitinolo a basso profilo
-‐ l’Endurant Medtronic, protesi con aggancio soprarenale modulare con stent in nitinolo a basso profilo
-‐ l’Excluder Gore, protesi con aggancio sottorenale modulare con stent in nitinolo
-‐ l’Endologix, protesi con aggancio sottorenale non modulare con stent in cromo-‐cobalto
Figura 13. Endoprotesi ad aggancio soprarenale modulari: Zenith Cook Flex, Zenith Cook Low Profile, Endurant Medtronic
Figura 14. Protesi ad aggancio sottorenale: Endologix (protesi non modulare), Gore Excluder (protesi modulare).
La scelta fra aggancio soprarenale e aggancio sottorenale è stata effettuata in base alle caratteristiche del colletto, in quanto nei colletti di lunghezza compresa tra i 15 e i 20 mm o con un’angolazione sottorenale compresa tra i 30 ed i 60 gradi è stato preferito un aggancio soprarenale con la Zenith Cook Flex e Low Profile (103 casi; 61,7%).
I casi con colletto di lunghezza maggiore di 2 cm e con angolazione ridotta (48 casi, 28,8%) sono stati trattati con aggancio sottorenale; prevalentemente è stata utilizzata la protesi Excluder Gore utilizzando l’Endologix nei pazienti con AAA sacciformi a livello della biforcazione aortica.
In 9 casi (5,4%), in cui il colletto presentava lunghezza compresa tra 10 e 15 mm in pazienti con rischio operatorio particolarmente elevato (addome “ostile”, grave BPCO), è stata utilizzata l’endoprotesi Medtronic che per le caratteristiche di flessibilità e l’aggancio soprarenale presenta una più ampia indicazione per tali tipi di colletti.
I pazienti con aneurisma delle arterie iliache bilaterali, che richiedevano l’embolizzazione o l’utilizzo di branch a carico delle ipogastriche bilateralmente, sono stati esclusi dal trattamento EVAR. I pazienti con presenza di aneurisma iliaco monolaterale sono stati sottoposti ad embolizzazione (22 pz; 13,2%) od utilizzo di branch (7 pz; 4,2%) a carico di un’arteria ipogastrica. L’embolizzazione delle arterie ipogastriche è stata eseguita preliminarmente all’impianto endoprotesico in 19 casi (11,4%), mentre in 3 casi (1,8%) è stata eseguita contestualmente: di cui 2 (1,2%) elettivamente ed 1 (0,6%) in urgenza in seguito a rottura a livello dell’iliaca comune distale con necessaria estensione in iliaca esterna. L’embolizzazione è stata effettuata in 17 casi (10,2%) mediante vascular plug ed in 5 casi (3%) mediante spirali metalliche.
I pazienti con aneurismi iliaci comuni con concomitante ectasia aortica sono stati trattati con impianto endoprotesico aortobisiliaco nei casi in cui era presente colletto iliaco prossimale inferiore a 2 cm e con branca protesica iliaca isolata in caso di colletto superiore a 2 cm.
Pazienti %
Tipo di graft Endoprotesi Aorto-‐bisiliaca 160 95,8
Endoprotesi Aorto aortica 1 0,6
Endoprotesi Aortouniliaca 2 1,2
Endoprotesi Iliaca 4 2,4
Marca endoprotesi Zenith Cook Flex 82 49,1
Zenith Cook LP 21 12,6 Gore Excluder 33 19,8 Medtronic Endurant 9 5,4 Endologix 15 9,0 Altro 7 4,2
Tabella 4. Tipologia di dispositivi utilizzati
Gli impianti endoprotesici sono stati effettuati in sala operatoria con utilizzo di angiografo portatile (GE-‐OEC 9900; GE Medical Systems®), l’anestesia è stata di tipo generale bilanciata nel 49,7% dei casi (83 casi), locale nel 38,9% dei casi (65 casi) e nel 11,4% (19 casi) anestesia spinale o epidurale.
L’accesso femorale è stato sempre chirurgico bilaterale, tranne che nei casi di utilizzo di endoprotesi monocorpo (Endologix) o endoprotesi iliache in cui uno dei due accessi, se necessario, è stato percutaneo.
Procedure aggiuntive intraoperatorie, precedentemente pianificate, sono state eseguite in 4 (2,4%) pazienti: fra cui 3 (1,8%) endoarteriectomie femorali con patch di allargamento in Dacron per la presenza di stenosi a livello della femorale comune, 1 (0,6%) stent renale eseguito per la presenza di stenosi dell’arteria renale principale in paziente con piccola renale polare sacrificata durante la procedura.
La durata dell’intervento è stata di 138+50 minuti (range 40-‐350 minuti), la durata della scopia è stata di 20+15 minuti ed il mezzo di contrasto utlizzato è stato 120+90 ml.
La degenza postoperatoria è stata di 2,6+4,6 giorni (range 1-‐58), 10 (6%) pazienti hanno necessitato di ricovero in UTI.
Protocollo di follow-‐up
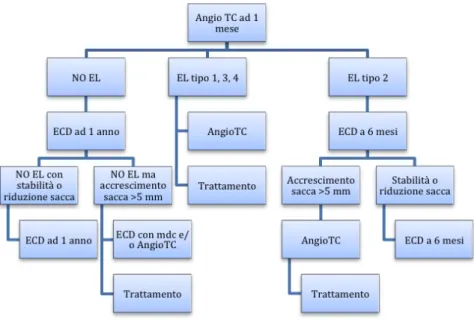
Il follow-‐up è consistito nell’esame AngioTc ad 1 mese dall’intervento, successivamente in assenza di complicazioni il follow up è stato con Eco Color Doppler annuale (Fig.15).
La presenza di endoleak di tipo II senza accrescimento ha richiesto l’esecuzione di Eco color Doppler semestrale.
La presenza di endoleak di tipo 1°, 3° o 2° con accrescimento ha rappresentato un indicazione ad esame AngioTc e successivo reintervento.
Nei casi di endoleak di difficile interpretazione è stato anche eseguito Eco Color Doppler con mezzo di contrasto.
Figura 15. Schema follow up (EL, endoleak; ECD, Eco Color Doppler)
Analisi statistica
I risultati precoci a 30 giorni sono stati analizzati e confrontati mediante Χ^2 test o test esatto di Fisher. I risultati a lungo termine sono stati analizzati mediante curve di Kaplan-‐Meier.